
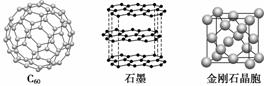
碳元素的单质有多种形式,下图依次是C60、石墨和金刚石的结构图:
回答下列问题:
(1)金刚石、石墨、C60、碳纳米管等都是碳元素的单质形式,它们互为____________。
(2)金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为________、________。
(3)C60属于________晶体,石墨属于________晶体。
(4)石墨晶体中,层内C—C键的键长为142 pm,而金刚石中C—C键的键长为154 pm。其原因是金刚石中只存在C—C间的________共价键,而石墨层内的C—C间不仅存在________共价键,还有________键。
(5)金刚石晶胞含有____________个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r=__________a,列式表示碳原子在晶胞中的空间占有率__________(不要求计算结果)。
答案 (1)同素异形体 (2)sp3 sp2
(3)分子 混合
(4)σ σ π(或大π或pp π)
(5)8 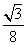
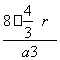 =
=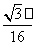
解析 (1)金刚石、石墨、C60、碳纳米管等都是碳元素的单质形式,它们的组成元素相同,结构不同、性质不同,互称为同素异形体。(2)金刚石中碳原子与四个碳原子形成4个共价单键(即C原子采取sp3杂化方式),构成正四面体;石墨中的碳原子采用sp2杂化轨道与相邻的三个碳原子以σ键结合,形成正六边形的平面层状结构。(3)C60中构成微粒是分子,所以属于分子晶体;石墨的层内原子间以共价键结合,层与层之间以分子间作用力结合,所以石墨属于混合晶体。(4)在金刚石中只存在C—C之间的σ键;石墨层内的C—C之间不仅存在σ键,还存在π键。(5)由金刚石的晶胞结构可知,晶胞内部有4个C原子,面心上有6个C原子,顶点有8个C原子,所以金刚石晶胞中C原子数目为4+6×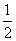 +8×
+8×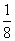 =8;若C原子半径为r,金刚石的边长为a,根据硬球接触模型,则正方体对角线长度的
=8;若C原子半径为r,金刚石的边长为a,根据硬球接触模型,则正方体对角线长度的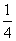 就是C—C键的键长,即
就是C—C键的键长,即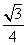 a=2r,所以r=
a=2r,所以r=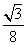 a;碳原子在晶胞中的空间占有率w=
a;碳原子在晶胞中的空间占有率w=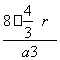 =
=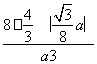 =
=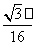 。
。


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
下列现象或事实可用同一原理解释的是( )
A.浓硫酸和浓盐酸长期暴露在空气中浓度降低
B.SO2和FeSO4溶液使酸性高锰酸钾的紫色褪去
C.漂白粉和水玻璃长期暴露在空气中变质
D.亚硫酸钠溶液和氯化铝溶液在空气中蒸干不能得到对应的溶质
查看答案和解析>>
科目:高中化学 来源: 题型:
Cu与F形成的化合物的晶胞结构如右图所示,若晶体密度为a g·cm-3,则Cu与F最近距离为________pm。(阿伏加德罗常数用NA表示,列出计算表达式,不用化简:图中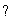 为Cu,
为Cu, 为F)
为F)

查看答案和解析>>
科目:高中化学 来源: 题型:
下面有关晶体的叙述中,不正确的是( )
A.金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子
B.氯化钠晶体中,每个Na+周围距离相等的Na+共有6个
C.氯化铯晶体中,每个Cs+周围紧邻8个Cl-
D.干冰晶体中,每个CO2分子周围紧邻12个CO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
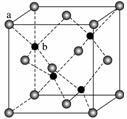
ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如图所示,其晶胞边长为540.0 pm,密度为______g·cm-3(列式并计算),a位置S2-与b位置Zn2+之间的距离为______pm(列式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
近年来,科学家合成一系列具有独特化学特性的氢铝化合物(AlH3)n。已知,最简单的氢铝化合物Al2H6的球棍模型如下图所示,它的熔点为150 ℃,燃烧热极高。下列说法肯定错误的是( )
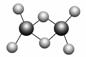
A.Al2H6在固态时所形成的晶体是分子晶体
B.Al2H6在空气中完全燃烧,产物为氧化铝和水
C.氢铝化合物可能成为未来的储氢材料和火箭燃料
D.氢铝化合物中可能存在组成为AlnH2n+2的物质(n为正整数)
查看答案和解析>>
科目:高中化学 来源: 题型:
下图为几种晶体或晶胞的示意图:

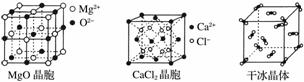
请回答下列问题:
(1)上述晶体中,粒子之间以共价键结合形成的晶体是________________。
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为________________________。
(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能________(填“大于”或“小于”)MgO晶体,原因是________________________。
(4)每个Cu晶胞中实际占有________个Cu原子,CaCl2晶体中Ca2+的配位数为________。
(5)冰的熔点远高于干冰,除H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
A+、B+、C-、D、E五种粒子(分子或离子)中,每个粒子均有10个电子,已知:
①A++C-===D+E↑;②B++C-===2D。
请回答:
(1)C-离子的电子式是________________。
(2)A+离子中的键角为______________。
(3)分别写出A+和D反应、B+和E反应的离子方程式____________、____________。
(4)除D、E外,请再写出两种含10个电子的分子的分子式____________。
(5)除A+、B+外,请再写出两种含10个电子的阳离子________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某100 mL混合酸中,HNO3物质的量浓度为0.4 mol·L-1,H2SO4物质的量浓度为0.2 mol·L-1。向其中加入2.56 g Cu粉,待充分反应后(反应前后溶液体积变化忽略不计),溶液中Cu2+物质的量浓度为( )
A.0.15 mol·L-1 B.0.3 mol·L-1
C.0.225 mol·L-1 D.无法计算
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com