
恒温恒容条件下,不是可逆反应2A(g)+3B(s) 2C(g)达到平衡标志的是( )
2C(g)达到平衡标志的是( )
①C的生成速率与C的分解速率相等;②单位时间生成amol A,同时消耗1.5amol B;③各组分的浓度不再变化;④混合气体的密度不再变化;⑤混合气体的总压强不再变化;⑥混合气体的物质的量不再变化;⑦混合气体的平均摩尔质量不再变化;⑧A、B、C的分子数目比为2:3:2。
A.②⑤⑧ B.⑤⑥⑧ C.①③④ D.②④⑦
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高一上期中化学试卷(解析版) 题型:选择题
下列各组物质中,分子数相同的是( )
A.5 L Cl2与5 L HCl B.36 g H2O与44.8 L CO2
C.25 ℃,1.01×105 Pa时,等体积的空气与H2 D.0.2 mol O2与标准状况下2.24 L水
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆中学高一上期中化学试卷(解析版) 题型:选择题
在无 色透明的酸性溶液中,能大量共存的离子组是( )
色透明的酸性溶液中,能大量共存的离子组是( )
A.Mg2+、Ag+、NO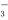 、Cl- B.Ba2+、K+、NO
、Cl- B.Ba2+、K+、NO 、Cl-
、Cl-
C. Cu2+、Na+、SO42-、Cl- D.Mg2+、Na+、OH-、SO42-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆中学高二上期中化学试卷(解析版) 题型:填空题
甲烷广泛存在于天然气、沼气、煤矿坑气之中,是优质的气体燃料,更是制造许多化工产品的重要原料。
Ⅰ.制取氢气
已知:CH4(g)+H2O(g) CO(g)+3H2(g) △H=+206.2kJ·mol-1
CO(g)+3H2(g) △H=+206.2kJ·mol-1
CH4(g)+CO2(g) 2CO(g)+2H2(g) △H=+247.4kJ·mol-1
2CO(g)+2H2(g) △H=+247.4kJ·mol-1
(1)请写出CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式___________________
(2)若将0.1mol CH4和0.1mol H2O(g)通入体积为10L的密闭容器里,在一定条件下发生反应:CH4(g)+H2O(g) CO(g)+3H2(g),CH4的平衡转化率与温度、压强的关系如图
CO(g)+3H2(g),CH4的平衡转化率与温度、压强的关系如图
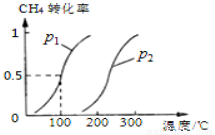
①已知1 00℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率_________;
00℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率_________;
②该反应的化学平衡常数___________________;
③图中的p1 p2(填“<”、“>”或“=”);
Ⅱ.制备甲醇
(3)在压强为0.1MPa条件下,将a mol CO与3amol H2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g)+2H2(g) CH3OH(g) △H<0。若容器容积不变,下列措施可增加甲醇产率的是________;
CH3OH(g) △H<0。若容器容积不变,下列措施可增加甲醇产率的是________;
A.升高温度
B.再充入1mol CO和3mol H2
C.将CH3OH(g)从体系中分离
D.充入He,使体系总压强增大
E.使用更高效的催化剂
Ⅲ.合成乙酸
(4)甲烷直接合成乙酸具有重要的理论意义和应用价值。光催化反应技术使用CH4和 (填化学式)直接合成乙酸,且符合“绿色化学”的要求(原子利用率100℅)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆中学高二上期中化学试卷(解析版) 题型:选择题
下列关于化学平衡常数的说法中,正确的是( )
A.在任何条件下,化学平衡常数都是一个定值
B.当改变反应物的浓度时,化学平衡常数会发生改变
C.化学平衡常数K与温度、反应物浓度、体系的压强都有关
D.化学平衡常数K可以推断一个可逆反应进行的程度
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆中学高二上期中化学试卷(解析版) 题型:选择题
对于A2+3B2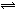 2C的反应来说,以下化学反应速率的表示中,反应速率最快的是( )
2C的反应来说,以下化学反应速率的表示中,反应速率最快的是( )
A.v(B2)=0.8mol/(L•s) B.v(A2)=0.4mol/(L•s)
C.v(C)=0.6mol/(L•s)  D.v(B2)=4.2mol/(L•min)
D.v(B2)=4.2mol/(L•min)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆一中高二上10月月考化学卷(解析版) 题型:填空题
碳及其化合物在能源、材料等方面具有广泛的用途。回答下列问题:
(1)碳酸和草酸均为二元弱酸,其电离分为两步进行,已知其电离常数的有关数据如下表:向Na2CO3溶液中滴加草酸溶液,开始时所发生反应的离子方程式为 。
H2CO3 | H2C2O4 | |
K1 | 4.2×10-7 | 5.4×10-2 |
K2 | 5.6×10-11 | 5.4×10-5 |
(2)常温时,C和CO的燃烧热△H分别为-394.0 kJ·mol-1、-283.0 kJ·mol-1,该条件下C转化为CO的热化学方程式为 。
(3)氢气和一氧化碳在一定条件下可合成甲醇,反应如下
2H2(g)+CO(g) CH3OH(g) △H=Q kJ·mol-1。
CH3OH(g) △H=Q kJ·mol-1。
①该反应在不同温度下的化学平衡常数(K)如下表:
温度(℃) | 250 | 300 | 350 |
K(L2·mol-1) | 2.041 | 0.270 | 0.012 |
由此可判断Q 0(填“>”、“=”或“<”)
②一定温度下,将6 mol H2和2mol CO充入到体积为2 L的密闭容器中,10 min时反应达到平衡状态,此时测得c(CO)=0.2 mol·L-1,该温度下的平衡常数K= 。0~10 min内,反应速率v(CH3OH)= 。
③在两个密闭容器中分别都充入20 mol H2和10 mol CO,测得一氧化碳的平衡转化率随温度(T)、压强(p)的变化如下图所示:
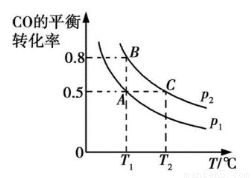
A、B两点压强大小关系:p1 p2(填“>”、“=”或“<”)。若A点对应容器的容积为20 L,则B点对应的容器的容积为 L。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆一中高二上10月月考化学卷(解析版) 题型:选择题
下列叙述中完全正确的一组是
①常温常压下,1mol甲基(-CH3)所含的电子数为10NA
②由Cu、Zn和稀硫酸组成的原电池工作时,若Cu极生成0.2gH2,则电路通过电子0.2NA
③在标准状况下,11.2L NO与11.2L O2混合后气体分子数为0.75NA
④常温常压下,16g O3所含的原子数为NA
⑤1mol Cl2发生反应时,转移的电子数一定是2NA
⑥标准状况下,22.4L水中含分子数为NA
A.①②③④ B.②④⑤⑥ C.②④ D.①②
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上期中化学试卷(解析版) 题型:选择题
参照反应Br+H2→HBr+H的能量对反应历程的示意图,下列叙述中正确的是( )
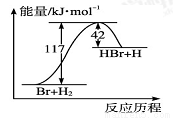
A.正反应为吸热反应
B.正反应为放热反应
C.加入催化剂,该化学反应的反应热增大
D.从图中可看出,该反应的反应热与反应途径有关
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com