
| A. | 用A表示反应的速率为0.1 mol•L-1•s-1 | |
| B. | 用B表示反应速率为0.4 mol•L-1•s-1 | |
| C. | 3s时生成C的物质的量为1.2mol | |
| D. | 3s时B的浓度为0.6mol•L-1 |
分析 根据题意,B物质起始的浓度为1.5mol/L,经3s后测得C的物质的量浓度为0.6mol•L-1,则
A(s)+3B(g)?2C(g)
开始(mol/L) 0.4 1.5 0
转化(mol/L) 0.3 0.9 0.6
3s时(mol/L) 0.1 0.6 0.6
以此计算转化率及反应速率,并结合平衡的移动及判定来解答.
解答 解:根据题意,B物质起始的浓度为1.5mol/L,经3s后测得C的物质的量浓度为0.6mol•L-1,则
A(s)+3B(g)?2C(g)
开始(mol/L) 1.5 0
转化(mol/L) 0.9 0.6
3s时(mol/L) 0.6 0.6
A.根据速率计算公式,计算物质A表示反应的速率=$\frac{0.3mol/L}{3s}$=0.1 mol•L-1•s-1,故A正确;
B.根据上面的分析,B转化的浓度为0.9mol/L,所以用B表示的反应速率为$\frac{0.9mol/L}{3s}$=0.3mol•L-1•s-1,故B错误;
C.3s时生成C的物质的量为0.6mol•L-1×2L=1.2mol,故C正确;
D.根据上面的分析可知,3s时B的浓度为0.6mol•L-1,故D正确,
故选B.
点评 本题考查化学平衡的计算,涉及化学平衡三段法计算、反应速率的计算等,综合性较强,题目难度中等,速率计算为解答的易错点.


科目:高中化学 来源: 题型:选择题
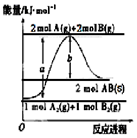
| A. | 该反应热△H=+(a-b)kJ•mol-1 | |
| B. | AB(g)═A(g)+B(g)△H=+b/2kJ•mol-1 | |
| C. | 断裂1 mol A-A键和1 mol B-B键,吸收a kJ能量 | |
| D. | 该反应在任何条件下都不可能自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100ρV/(36.5V+2240) | B. | 1000ρV/(36.5V+2240) | ||
| C. | ρ V/(36.5V+2240) | D. | (1000+36.5ρV)/( 36.5V+2240) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性溶液中:NH4+、Ba2+、AlO2-、Cl- | |
| B. | 滴入酚酞显红色的溶液中:Na+、K+、SiO32-、HCO3- | |
| C. | 滴入石蕊显红色的溶液中:K+、Ca2+、Fe2+、NO3- | |
| D. | 澄清透明溶液中:K+、MnO4-、H3O+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 L氟化氢气体分解成1 L氢气与1 L氟气吸收270 kJ热量 | |
| B. | 在相同条件下,1 mol氢气与1 mol氟气的能量总和大于2 mol氟化氢气体的能量 | |
| C. | 1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ | |
| D. | 1个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270 kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将称量NaOH固体时在烧杯中溶解后立即转移到容量瓶中 | |
| B. | 向容量瓶中加水定容时俯视 所配溶液浓度偏高 | |
| C. | 配制NaOH溶液不需用到量筒 | |
| D. | 定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2+、K+、C1-、NO3- | B. | Cu2+、K+、SO42-、NO3- | ||
| C. | Na+、K+、SO42-、AlO2- | D. | Ba2+、K+、SO42-、C1- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com