
【题目】下列热化学方程式及有关应用的叙述中,正确的是
A. 甲烷的燃烧热为890.3kJmol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+ 2O2(g) ═ CO2(g) + 2H2O(g) △H = -890.3kJmol-1
B. 已知强酸与强碱在稀溶液里反应的中和热为57.3kJmol-1,则![]() H2SO4(aq)+
H2SO4(aq)+![]() Ba(OH)2(aq)═
Ba(OH)2(aq)═![]() BaSO4(s)+H2O(l) △H < -57.3kJmol-1
BaSO4(s)+H2O(l) △H < -57.3kJmol-1
C. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) + 3H2(g)![]() 2NH3(g) △H = -38.6kJmol-1
2NH3(g) △H = -38.6kJmol-1
D. 已知25℃、101KPa条件下:4Al(s) + 3O2(g) ═ 2A12O3(s) △H = -2834.9kJmol-1,4Al(s) + 2O3(g) ═ 2A12O3(s) △H = -3119.1kJmol-1,则O3比O2稳定
【答案】B
【解析】
A. 甲烷的燃烧热为890.3kJmol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJmol-1,故A错误;
B. 已知强酸与强碱在稀溶液里反应的中和热为57.3kJmol-1,由于钡离子与硫酸根离子生成硫酸钡的反应为放热反应,则![]() H2SO4(aq)+
H2SO4(aq)+![]() Ba(OH)2(aq)═
Ba(OH)2(aq)═![]() BaSO4(s)+H2O(l) △H < -57.3kJmol-1,故B正确;
BaSO4(s)+H2O(l) △H < -57.3kJmol-1,故B正确;
C. 500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,由于该反应为可逆反应,则平衡时消耗氮气的物质的量小于0.5mol,即1mol氮气与氢气完全反应放出热量大于38.6kJ,则正确的热化学方程式为:N2(g) + 3H2(g)![]() 2NH3(g) △H <-38.6kJmol-1,故C错误;
2NH3(g) △H <-38.6kJmol-1,故C错误;
D. ①4Al(s)+3O2(g)=2A12O3,△H=-2834.9kJmol-1②4Al(s)+2O3(g)=2A12O3,△H=-3119.1gkJmol-1,根据盖斯定律①-②可得:302(g)=203(g)△H=-2834.9kJmol-1-(-3119.1kJmol-1)=+284.2kJmol-1,该反应为吸热反应,说明氧气的能量小于臭氧,则氧气比臭氧稳定,故D错误;
答案选B。


科目:高中化学 来源: 题型:
【题目】电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下。下列说法正确的是( )
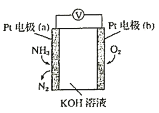
A.O2在电极b上发生氧化反应
B.溶液中OH-向电极b移动
C.反应消耗的NH3与O2的物质的量之比为4:3
D.正极的电极反应式为2NH3-6e-+6OH-=N2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均是短周期主族元素,其原子序数依次增大,A和B同周期,A和D同主族,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的阴离子与C的阳离子电子层结构相同,C的单质与B的单质在不同条件下反应,可生成C2B或C2B2,E是所在周期中原子半径最小的元素,请回答:
(1)D在元素周期表中的位置是___________。
(2)C2B2的电子式是________。
(3)B、C、E的离子半径由大到小的顺序为________(用离子符号回答);A、D、E元素最高价氧化物对应水化物的酸性由强到弱为_________(用化学式回答,下同),B的气态氢化物与H2S相比沸点高的是_____,原因是___________________________。
(4)写出D的氧化物与氢氟酸反应的化学方程式____________________________________。
(5)1mol C2B2与足量的水反应转移电子的物质的量是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:

下列有关叙述正确的是( )
A. 贝诺酯分子中有三种含氧官能团
B. 可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚
C. 乙酰水杨酸和对乙酰氨基酚均能与NaHCO3溶液反应
D. 贝诺酯与足量NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]() +CH3CHO+HBr
+CH3CHO+HBr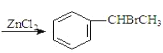 +H2O(卤烷基化反应);
+H2O(卤烷基化反应);
![]() +
+![]()
![]()
![]() +NaX
+NaX
用苯为原料合成化合物Ⅳ的线路如下:
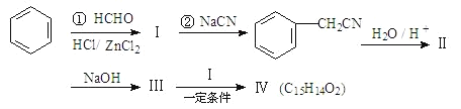
其中:Ⅱ是羧酸。请回答下列问题:
(1)②的反应类型是________。
(2)写出同时符合下列条件的化合物Ⅱ的同分异构体结构简式(写2种)_____、_____。
a.能与FeCl3溶液作用显紫色;
b.能发生银镜反应;
c.核磁共振氢谱除苯环峰外还有三组峰,峰面积之比为为 1:2:1。
(3)1mol化合物Ⅳ完全燃烧消耗O2_____mol,化合物Ⅳ的结构简式是__________。
(4)化合物Ⅱ与乙醇、浓硫酸共热,合成一种香精原料,试写出该反应的化学方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中,反应:aA(g) ![]() bB(g) 达平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,下列说法正确的是( )
bB(g) 达平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,下列说法正确的是( )
A. 平衡向逆反应方向移动了B. 物质A的转化率减少了
C. 物质B的质量分数增加了D. a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2O5是一种新型硝化剂,其性质和制备受到人们的关注。已知N2O5能与水发生反应,并放出大量的热。
Ⅰ.一定温度下,在恒容密闭容器中N2O5发生下列反应:2N2O5(g)![]() 4NO2(g)+O2(g)ΔH。
4NO2(g)+O2(g)ΔH。
(1)下表为反应在T1温度下的部分实验数据:
t/s | 0 | 500 | 1000 |
c(N2O5)/mol·L—1 | 5.00 | 3.52 | 2.48 |
则500s内NO2的生成速率为______________。
(2)反应达到平衡后,若再通入一定量N2O5,达到新平衡时,N2O5的转化率将______(填“增大”、“减小”、“不变”)。
(3)在温度T1和T2时,N2O5的浓度与反应时间的关系如图所示。据此判断:T1______T2(填“>”、“<”或“=”,下同),ΔH______0。
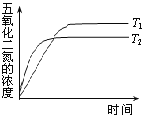
Ⅱ.下图所示装置,可用于制备N2O5气体。A是电源的____________(填“负极”或“正极”),电解池的阳极反应式为______________________________________________________。
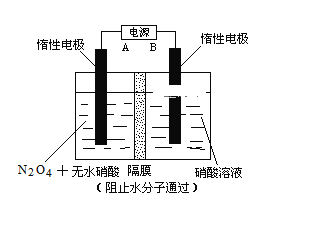
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是 ( )
A. FeO溶于稀硝酸:FeO+2H+ ![]() Fe2++H2O
Fe2++H2O
B. Al2(SO4)3溶液中加入过量Ba(OH)2溶液:Al3++4OH- ![]() AlO2-+2H2O
AlO2-+2H2O
C. 漂白粉溶液中通入少量CO2: 2ClO-+H2O+CO2![]() 2HClO+CO32-
2HClO+CO32-
D. 向NaOH溶液中滴加过量Ca(HCO3)2溶液:Ca2++HCO3-+OH-![]() CaCO3↓+H2O
CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空。
(1)有下列各组物质:
(A)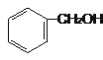 和
和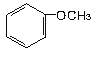 ;(B)CH2=CH-CH=CH2和CH3-CH2-C=CH;(C)
;(B)CH2=CH-CH=CH2和CH3-CH2-C=CH;(C) ;(D)
;(D)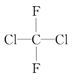 和
和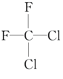 ;(E)甲烷和新戊烷
;(E)甲烷和新戊烷
其中____组两物质互为同系物;_______组两物质互为同分异构体;______组两物质互为同一物质;A组第一个物质的名称是:_________。
(2)写出1,3﹣丁二烯与Br2的CCl4溶液发生1,4﹣加成后的产物的结构简式:___________。
(3)写出由甲苯生成TNT(2,4,6﹣三硝基甲苯)的方程式:____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com