
【题目】下列有关实验装置进行的相应实验,能达到实验目的的是
A.利用图 方法验证装置的气密性
方法验证装置的气密性
B.实验室里利用图 装置制备氯气
装置制备氯气
C.利用图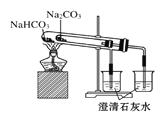 比较碳酸钠和碳酸氢钠的热稳定性
比较碳酸钠和碳酸氢钠的热稳定性
D.利用图 制备Fe(OH)2并能较长时间观察其颜色
制备Fe(OH)2并能较长时间观察其颜色
科目:高中化学 来源: 题型:
【题目】下列关于Na2CO3和NaHCO3的说法中,不正确的是
A. 焰色反应均为黄色
B. 溶解度:Na2CO3>NaHCO3
C. 可以用加热的方法除去Na2CO3固体中的NaHCO3杂质
D. 物质的量相同的两种固体分别与足量盐酸反应,Na2CO3产生的二氧化碳多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式的叙述正确的是( )
A.已知CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3kJ·mol-1,则甲烷的燃烧热为893.0kJ·mol-1
B.已知4P(红磷,s)=P4(白磷,s);ΔH>0,则白磷比红磷稳定
C.含20.0gNaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,反应的热化学方程式为:NaOH(aq)+![]() H2SO4(aq)=Na2SO4(aq)+H2O(l) ΔH=-57.4kJ·mol-1
H2SO4(aq)=Na2SO4(aq)+H2O(l) ΔH=-57.4kJ·mol-1
D.己知C(s)+O2(g)=CO2(g);ΔH1 C(s)+![]() O2(g)=CO(g);ΔH2,则ΔH1>ΔH2
O2(g)=CO(g);ΔH2,则ΔH1>ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用铜跟浓硫酸反应,探究SO2的部分性质,实验装置如图所示。
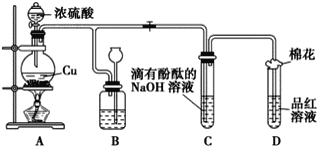
(1)装置A中发生的化学反应的化学方程式为________________________________
(2)装置B的作用是贮存多余的气体,B中广口瓶内应盛放的液体是________(填序号);
①水 ②饱和的NaHSO3溶液 ③NaOH溶液 ④酸性KMnO4
(3)装置C和D中产生的现象相同,但原因却不同。C中是由于SO2与溶液中的NaOH反应使碱性减弱,而D中则是由于SO2具有____________性
(4)装置D中试管口塞一团棉花,棉花中应浸有一种液体,其作用是____________
(5)若实验中用一定质量的铜片和25.0 mL 18.0 mol·L-1的浓硫酸在加热条件充分反应,最终铜片与硫酸均有剩余。假定反应前后溶液的体积不变,设剩余硫酸的浓度为d mol·L-1,现向反应后溶液中缓慢加入硝酸钾固体,充分搅拌直到剩余铜片恰好完全反应,反应消耗硝酸钾____________mol(用含d的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 向稀醋酸溶液中加入少量醋酸钠固体,醋酸的电离程度增大
B. 电镀时,通常把待镀金属制品作阴极,镀层金属作阳极
C. 常温下,2NO2(g)=2NO(g)+O2(g)不能自发进行,则该反应的△H>0
D. 工业通过反应“Na(l)+KCl(l) ![]() NaCl(l)+K(g)”冶炼钾,说明钠的金属性强于钾
NaCl(l)+K(g)”冶炼钾,说明钠的金属性强于钾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现以CO、O2、熔融盐Z(Na2CO3)组成的燃料电池,采用电解法处理CO同时制备N2O5,装置如图所示,其中Y为CO2。下列说法不合理的是
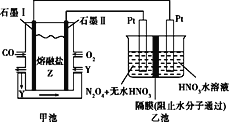
A.石墨Ⅰ是原电池的负极,发生氧化反应
B.甲池中的CO32-向石墨Ⅱ极移动
C.石墨Ⅰ的电极反应式:CO+CO32--2e-=2CO2
D.若甲池消耗标准状况下的氧气2.24L,则乙池中产生氢气0.2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在3个容积均为1.0L的恒容密闭容器中发生反应:PCl5(g)![]() PCl3(g)+Cl2(g)。下列说法正确的是
PCl3(g)+Cl2(g)。下列说法正确的是
容器 编号 | 物质的起始浓度(mol·L-1) | 物质的平衡浓度(mol·L-1) | ||
c(PCl5) | c(PCl3) | c(Cl2) | c(Cl2) | |
Ⅰ | 0.4 | 0 | 0 | 0.2 |
Ⅱ | 1.05 | 0.05 | 1.95 | |
Ⅲ | 0.8 | 0 | 0 | |
A.达平衡时,容器Ⅰ中![]() 比容器Ⅱ中的大
比容器Ⅱ中的大
B.达平衡时,容器Ⅰ与容器Ⅱ中的总压强之比为6∶31
C.达平衡时,容器Ⅲ中Cl2的体积分数大于![]()
D.达平衡时,容器Ⅲ中0.4mol·L-1<c(PCl5)<0.8mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸二氢钾在工农业和医学领域具有广泛的应用。以下是工业上制备磷酸二氢钾的三种方法。回答下列问题:
Ⅰ.直接法

(1)气体X为___(填化学式)。
(2)“转化”步骤发生反应的离子反应方程式___(已知:Ca3(PO4)2难溶于水)。
(3)滤液①中加入甲醇的作用是___。
(4)“操作Ⅰ”是___。
Ⅱ.酸碱中和法
(5)氢氧化钾溶液与高纯度磷酸在反应器中发生中和反应制备磷酸二氢钾。写出此反应的离子反应方程式___。由图1判断制备磷酸二氢钾(达80%)的最佳pH范围___。
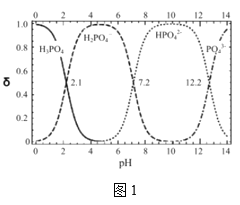
Ⅲ.电解法
电解法制取KH2PO4的原理如图2所示。一定件下,还可得到NaClO3。
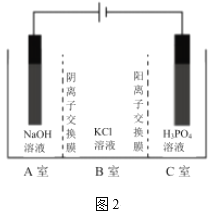
(6)在___室(填标号)可得到KH2PO4;写出产生ClO3-,的电极反应式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用下图所示装置研究化学反应X+2Y=2Z的能量变化情况。向试管中滴加试剂Y时,看到U形管中液面甲下降,液面乙上升。下列关于该反应的叙述中正确的是( )
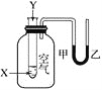
①该反应释放能量;②生成物的总能量比反应物的总能量高;③该反应过程可以看成是“贮存”于X、Y内部的能量转化为热量而释放出来。
A. ①②③B. ①③C. ①②D. ②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com