
A.ΔH1>ΔH2 B.ΔH1=ΔH2
C.ΔH1<ΔH2 D.无法比较
科目:高中化学 来源: 题型:
(1)混合物中氢氧化钠的物质的量;
(2)混合物中氢氧化钾的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
A.0.4 mol、0.5 mol、0.12 mol
B.0.66 mol、0.5 mol、0.24 mol
C.0.64 mol、0.5 mol、0.24 mol
D.0.64 mol、0.02 mol、0.24 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
盖尔达法分解蛋白质的过程可表示为:蛋白质![]() 硫酸铵
硫酸铵![]() 氨
氨
现对牛奶中的蛋白质进行下列实验。取30.0 mL牛奶用盖尔达法分解蛋白质,把氮完全转化成氨,用0.5 mol·L-1 H2SO4 50.0 mL吸收后,剩余的酸用1 mol·L-1 NaOH溶液中和,需38.0 mL。求:
(1)30.0 mL牛奶中共含有多少克氮?
(2)如果蛋白质中含氮16%(质量分数),则牛奶中含蛋白质的质量分数是多少?(已知牛奶的密度是1.03 g·mL-1)
查看答案和解析>>
科目:高中化学 来源:2012-2013学年云南省昆明市官渡区二中高二9月月考化学试卷(带解析) 题型:实验题
(共6分)实验室用50 mL 0.50 mol·L-1盐酸、50 mL 0.55 mol·L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据: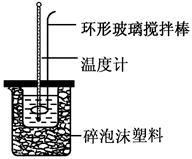
| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
查看答案和解析>>
科目:高中化学 来源:2014届云南省昆明市高二9月月考化学试卷(解析版) 题型:实验题
(共6分)实验室用50 mL 0.50 mol·L-1盐酸、50 mL 0.55 mol·L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:

|
实验次数 |
起始温度t1/℃ |
终止温度t2/℃ |
|
|
盐酸 |
NaOH溶液 |
||
|
1 |
20.2 |
20.3 |
23.7 |
|
2 |
20.3 |
20.5 |
23.8 |
|
3 |
21.5 |
21.6 |
24.9 |
完成下列问题:
(1)实验时不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是 。
(2)在操作正确的前提下,提高中和热测定准确性的关键是 。
(3)根据上表中所测数据进行计算,则该实验测得的中和热ΔH= [盐酸和NaOH溶液的密度按1 g·cm-3计算,反应后混合溶液的比热容(c)按4.18 J·(g·℃)-1计算]。如用0.5 mol/L的盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将 (填“偏大”、“偏小”、 “不变”)。
(4)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因是
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水
E.在量取盐酸时仰视计数
F.大烧杯的盖板中间小孔太大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com