
【题目】下列说法正确的是( )
A.摩尔是物质的数量单位
B.58.5 gNaCl溶解在1 L水中,得到溶液的物质的量浓度为1mol/L
C.标况下,1 mol CCl4 所占的体积约为22.4 L
D.12g12C含有的碳原子数约为6.02×1023个
科目:高中化学 来源: 题型:
【题目】工业上常用氨气为原料制备硝酸,其中有一步非常重要的反应为:4NH3+5O2 ![]() 4NO+6H2O该反应的氧化剂为 , 还原剂为 . 用单线桥法表示该氧化还原反应电子转移的方向和数目: . 若有标准状况下V L氨气完全反应,并转移n个电子,则阿伏伽德罗常数(NA)可表示为(写出含字母的表达式).
4NO+6H2O该反应的氧化剂为 , 还原剂为 . 用单线桥法表示该氧化还原反应电子转移的方向和数目: . 若有标准状况下V L氨气完全反应,并转移n个电子,则阿伏伽德罗常数(NA)可表示为(写出含字母的表达式).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中含有K+、Cl﹣、OH﹣、SO32﹣、SO42﹣ , 为检验溶液中所含的某些阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞溶液.检验其中OH﹣的实验方法省略,检验其他阴离子的过程如图所示. 
(1)图中试剂①~⑤溶质的化学式分别是 ① , ② , ③ , ④ , ⑤ .
(2)图中现象a、b、c表明检验出的离子分别是a、b、c .
(3)白色沉淀A加试剂②反应的离子方程式是 .
(4)无色溶液C加试剂③的主要目的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学内容填空
(1)现有下列A、B两组物质:
A组:CH3﹣CHCl﹣CH3、 ![]() 、HCOOH、CH3COOC2H5 .
、HCOOH、CH3COOC2H5 .
B组:CH3CH2CH2OH、银氨溶液、KOH溶液、Na2CO3溶液. 试回答:
①A组中能跟B组中所有物质都可发生反应.
②B组中可跟A组中三种物质反应
(2)在有机物① ![]() ﹣OH ②CH2=CH2③CH≡CH ④
﹣OH ②CH2=CH2③CH≡CH ④ ![]() ﹣CH2OH ⑤
﹣CH2OH ⑤ ![]() ﹣CH3 ⑥CH3COO﹣
﹣CH3 ⑥CH3COO﹣ ![]() ⑦CH3CH2CH2CH2Br
⑦CH3CH2CH2CH2Br
中属于芳香烃的是;能与溴水发生加成反应的是;能发生消去反应的是;能与NaOH溶液反应,但不能与Na2CO3溶液反应的是 . (填写上述物质的序号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】周期表前四周期的元素A、B、C、D、E,原子序数依次增大.A的核外电子总数与其周期数相同,B的价电子层中未成对电子有3个,C的最外层电子数为其内层电子数的3倍,D与C同族;E的最外层只有1个电子,但次外层有18个电子.回答下列问题;
(1)B、C、D中第一电离能最大的是(填元素符号),C的电子排布式为 .
(2)A和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为;分子中既含有极性共价键、又含有非极性共价键的化合物是(填化学式).
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是;酸根呈三角锥结构的酸是 . (填化学式)
(4)E和C形成的一种离子化合物的晶体结构如图(a),则E的离子符号为 . 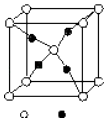
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,错误的是
A. 稀有气体元素原子的最外层电子数均为8个
B. 元素周期表中有7个主族、7个副族
C. 碳元素位于第2周期IVA族
D. 氢分子中的化学键是共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 ![]() 转变为
转变为 ![]() 的方法为( )
的方法为( )
A.与足量NaOH溶液共热后,再通入CO2
B.与足量NaOH溶液共热后,再加入稀硫酸
C.与稀硫酸共热后,加入足量NaOH溶液
D.与足量稀硫酸共热后,加入足量Na2CO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com