
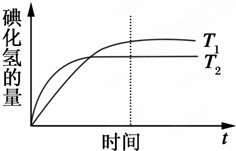
 在密闭容器中进行如下反应:H2(g)+I2(g)?2HI(g),在温度T1和T2时,产物的量与反应的时间的关系如图所示符合图示的正确判断是( )
在密闭容器中进行如下反应:H2(g)+I2(g)?2HI(g),在温度T1和T2时,产物的量与反应的时间的关系如图所示符合图示的正确判断是( )| A、T1>T2,△H>0 |
| B、T1<T2,△H<0 |
| C、T1<T2,△H>0 |
| D、T1>T2,△H<0 |
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、②①③ |
| C、③②① | D、①③② |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 分馏又称为分级蒸馏或精馏.适用于互溶而且沸点相差很小的多组分混合液的分离.控制好温度,便可将各种物质分离.有关分馏操作,下列说法正确的是( )
分馏又称为分级蒸馏或精馏.适用于互溶而且沸点相差很小的多组分混合液的分离.控制好温度,便可将各种物质分离.有关分馏操作,下列说法正确的是( )| 1 |
| 3 |
| 1 |
| 4 |
| A、①③④ | B、②③④ |
| C、③④⑤ | D、②③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、天然橡胶易溶于水 |
| B、羊毛是合成高分子材料 |
| C、聚乙烯塑料是天然高分子材料 |
| D、酚醛塑料(俗称电木)不可以进行热修补 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、①③ | C、②③ | D、③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com