
| A、1.0mol/L |
| B、2.5mol/L |
| C、1.5mol/L |
| D、1.8mol/L |
| ||
| 4.48L |
| 22.4L/mol |


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
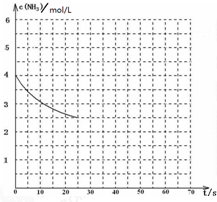 氨是最重要的化工产品之一.
氨是最重要的化工产品之一.| 1 |
| 2 |
| 1 |
| 2 |
| 弱电解质 | H2CO3 | NH3?H2O |
| 电离平衡常数 | Ka1=4.30×10-7 Ka2=5.61×10-11 | Kb=1.77×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
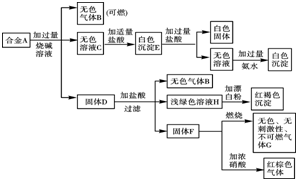 现有四种单质组成的合金A,为分析其成分,用此合金进行一系列实验,其过程及发生反应的现象如下图所示.
现有四种单质组成的合金A,为分析其成分,用此合金进行一系列实验,其过程及发生反应的现象如下图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③ | B、①②③ |
| C、①③④ | D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1L 1.0mol?L-1的NaC1O溶液中含有C1O-的数目为NA |
| B、标准状况下,22.4L盐酸含有NA个HC1分子 |
| C、常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA |
| D、1molNa被完成氧化生成Na2O2,失去个2NA电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KHCO3、NH4HCO3 |
| B、NH4HCO3、KHCO3 |
| C、KHCO3、KHCO3 |
| D、NH4HCO3、NH4HCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、aNA/25 |
| B、aNA/(25×18) |
| C、aNA/(25×20) |
| D、aNA/(1000×22.4) |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、H2O(g)═H2(g)+
| ||
B、H2O(g)═H2(g)+
| ||
| C、2H2(g)+O2(g)═2H2O(g)△H=+485kJ?mol-1 | ||
| D、2H2(g)+O2(g)═2H2O(g)△H=-485kJ?mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com