
| A. | 向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3↓+3H+ | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O | |
| D. | 用Pt电极电解饱和氯化镁溶液:2Cl-+2H2$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ |
分析 A.水解生成胶体,而不是沉淀;
B.发生氧化还原反应生成碘化亚铁、碘和水;
C.反应生成氯化钠、水、二氧化碳;
D.生成氢氧化镁、氢气、氯气.
解答 解:A.向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体的离子反应为Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3H+,故A错误;
B.Fe(OH)3溶于氢碘酸的离子反应为2Fe(OH)3+2I-+6H+═2Fe2++I2+6H2O,故B错误;
C.用小苏打治疗胃酸过多的离子反应为HCO3-+H+═CO2↑+H2O,故C正确;
D.用Pt电极电解饱和氯化镁溶液的离子反应为Mg2++2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Mg(OH)2↓+H2↑+Cl2↑,故D错误;
故选C.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重水解、氧化还原反应及电解反应的离子反应考查,综合性较强,题目难度不大,注意离子反应中保留化学式的物质.


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:多选题
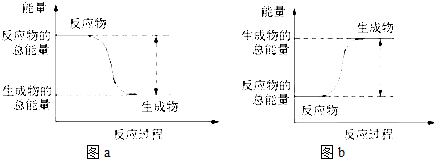
| A. | 图a表示的是吸热反应的能量变化 | |
| B. | 图b中反应物比生成物稳定 | |
| C. | 图b可以表示氯化铵固体与氢氧化钡晶体反应的能量变化 | |
| D. | 图a不需要加热就一定能发生,图b一定需要加热才能发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,雷电作用能进行氮的固定,写出反应方程式N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO.
,雷电作用能进行氮的固定,写出反应方程式N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z、W是金属元素 | |
| B. | 原子半径:r(R)<r(W)<r(Z) | |
| C. | Y与Z形成的化合物只有一种 | |
| D. | X、Z、R的最高价氧化物对应的水化物之间都能相互发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1的Na2CO3溶液中粒子浓度关系:c(Na+)═2c(CO32-)+2c(HCO3-)+2c(H2CO3) | |
| B. | 常温下,氢氧化钠溶液中滴入醋酸使溶液的pH=7,则混合溶液中醋酸已过量 | |
| C. | 0.2mol•L-1的HCl和0.1 mol•L-1的NH3•H2O等体积混合后溶液中的离子浓度关系:c(Cl-)>c (NH4+)>c(H+)>c (OH-) | |
| D. | 0.1mol•L-1的NaHS溶液中离子浓度关系:c(S2-)+c(OH-)═c(H+)+c(H2S) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡金属元素与非金属元素化合时都能形成离子键 | |
| B. | 非金属原子间不可能形成离子键 | |
| C. | 钠原子与氯原子通过得失电子,以离子键结合成氯化钠后体系能量降低 | |
| D. | 含有共价键的化合物一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素的相对原子质量的递增 | |
| B. | 元素的原子半径呈周期性变化 | |
| C. | 元素原子的最外层电子排布呈周期性变化 | |
| D. | 元素的金属性和非金属性呈周期性变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com