
”¾ĢāÄæ”æ¼øÖÖ¶ĢÖÜĘŚŌŖĖŲµÄŌ×Ó°ė¾¶¼°Ö÷ŅŖ»ÆŗĻ¼ŪČēĻĀ±ķ£ŗ
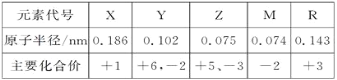
ŅŃÖŖXŹĒ¶ĢÖÜĘŚÖŠ×ī»īĘĆµÄ½šŹō£¬ĒŅÓėRĶ¬ÖÜĘŚ”£ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ(””””)
A.Ąė×Ó°ė¾¶“󊔣ŗR3£«£¼X£«£¼M2£
B.YÓėM×é³ÉµÄ»ÆŗĻĪļŹĒŠĪ³É¹ā»ÆѧŃĢĪķµÄŌŅņÖ®Ņ»
C.½«YM2ĶØČėBa(NO3)2ČÜŅŗÖŠÓŠ“óĮæ°×É«³Įµķ²śÉś
D.MµÄĒā»ÆĪļµÄČŪ”¢·ŠµćøßÓŚZµÄĒā»ÆĪļµÄČŪ”¢·Šµć
”¾“š°ø”æB
”¾½āĪö”æ
XŹĒ¶ĢÖÜĘŚÖŠ×ī»īĘĆµÄ½šŹō£¬ŌņXŹĒNa£»RÓėXĶ¬ÖÜĘŚ£¬ĒŅÖ÷ŅŖ»ÆŗĻ¼ŪĪŖ+3£¬ŌņRĪŖAl£»YŗĶMÖ÷ŅŖ»ÆŗĻ¼Ū¾łÓŠ-2¼Ū£¬ĒŅYÓŠ+6¼Ū£¬ŌņYĪŖS£¬MĪŖO£»ZµÄŌ×Ó°ė¾¶±ČY(S)Š”ĒŅÖ÷ŅŖ»ÆŗĻ¼ŪĪŖ+5”¢-3£¬ŌņZĪŖN£¬×ŪÉĻĖłŹö£¬X”¢Y”¢Z”¢M”¢R·Ö±šĪŖ£ŗNa”¢S”¢N”¢O”¢Al£¬¾Ż“Ė½ā“š”£
A£®RĪŖAl£¬XĪŖNa£¬MĪŖO£¬R3£«”¢X£«”¢M2£¾łŗ¬2øöµē×Ó²ć£¬ŗĖµēŗÉŹż£ŗR3£«£¾X£«£¾M2££¬ŗĖĶāµē×ÓÅŲ¼ĻąĶ¬µÄĄė×Ó£¬ŗĖµēŗÉŹżŌ½“ó£¬Ąė×Ó°ė¾¶Ō½Š”£¬¹ŹĄė×Ó°ė¾¶£ŗR3£«£¼X£«£¼M2££¬AÕżČ·£»
B£®YĪŖS£¬MĪŖO£¬µŖŃõ»ÆĪļŹĒŠĪ³É¹ā»ÆѧŃĢĪķµÄŌŅņÖ®Ņ»£¬²»ŹĒĮņŃõ»ÆĪļ£¬B“ķĪó£»
C£®YM2¼“SO2£¬SO2ÓėĖ®·“Ӧɜ³ÉŃĒĮņĖį£¬NO3-ŌŚĖįŠŌĢõ¼žĻĀÓŠĒæŃõ»ÆŠŌ£¬½«SO2Ńõ»Æ³ÉSO42-£¬SO42-ŗĶBa2+·“Ӧɜ³ÉBaSO4³Įµķ£¬CÕżČ·£»
D£®MĪŖO£¬Ęä¼ņµ„Ēā»ÆĪļĪŖH2O£¬³£ĪĀ³ŹŅŗĢ¬£¬ZĪŖN£¬Ęä¼ņµ„Ēā»ÆĪļĪŖNH3£¬³£ĪĀ³ŹĘųĢ¬£¬¹ŹM(O)µÄĒā»ÆĪļµÄČŪ”¢·ŠµćøßÓŚZ(N)µÄĒā»ÆĪļµÄČŪ”¢·Šµć£¬DÕżČ·”£
“š°øŃ”B”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŖĮĖ±Č½ĻĀ±ĖŲµ„ÖŹµÄŃõ»ÆŠŌĒæČõ£¬æÉŌŚŹµŃéŹŅĻČÖĘČ”Cl2(ĄūÓĆMnO2ÓėÅØŃĪĖį·“Ó¦æÉÖĘČ”Cl2)£¬²¢½«Cl2ŅĄ“ĪĶØČėNaBrČÜŅŗŗĶKI-µķ·ŪČÜŅŗÖŠ”£ČēĶ¼ĖłŹ¾ŅĒĘ÷¼°Ņ©Ę·£¬ŹŌ»Ų“š£ŗ
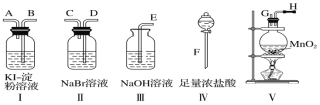
(1)ČōĖłÖĘČ”ĘųĢåµÄĮ÷Ļņ“Ó×óĻņÓŅŹ±£¬ÉĻŹöŅĒĘ÷½ÓæŚµÄĮ¬½ÓĖ³ŠņĪŖ____½Ó_____”¢ ____½Ó____”¢________½Ó____”¢_____½Ó____(Ģī×ÖÄø)”£
(2)ŹµŃéæŖŹ¼ŗó×°ÖĆ¢õÖŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ________”£
(3)×°ÖĆ¢ņÖŠ·¢ÉśµÄĻÖĻóŹĒ_______£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_____”£
(4)×°ÖĆ¢ńÖŠ²śÉśµÄĻÖĻó£ŗČÜŅŗĻȱ䥶Ņ»¶ĪŹ±¼äŗóĄ¶É«ĶŹČ„£¬Éś³ÉĮ½ÖÖĒæĖį£¬ĒėŠ“³öĄ¶É«ĶŹČ„µÄ»Æѧ·½³ĢŹ½£ŗ_____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĮ×»ÆĒā![]() ŹĒŅ»ÖÖÓŠ“óĖāĘųĪ¶µÄ”¢ĪŽÉ«¾ē¶¾µÄĒ滹ŌŠŌĘųĢ壬Ņ×ŌŚæÕĘųÖŠ×ŌČ¼£¬Ņ»°ćŌŚĻ”ŹĶדĢ¬ĻĀŹ¹ÓĆÄܽµµĶ·ēĻÕ”£Ä³æĘŃŠŠ”×éÄāÓĆĖ®½ā·ØÖʱø²¢ĄäÄżŹÕ¼Æ²æ·ÖøÉŌļµÄ
ŹĒŅ»ÖÖÓŠ“óĖāĘųĪ¶µÄ”¢ĪŽÉ«¾ē¶¾µÄĒ滹ŌŠŌĘųĢ壬Ņ×ŌŚæÕĘųÖŠ×ŌČ¼£¬Ņ»°ćŌŚĻ”ŹĶדĢ¬ĻĀŹ¹ÓĆÄܽµµĶ·ēĻÕ”£Ä³æĘŃŠŠ”×éÄāÓĆĖ®½ā·ØÖʱø²¢ĄäÄżŹÕ¼Æ²æ·ÖøÉŌļµÄ![]() £¬ŌŁĄūÓĆĪ“Ņŗ»ÆµÄÓąĘų¼ĢŠųĢ½¾æĘäČČ·Ö½āĒéæö”£ŹµŃé×°ÖĆĶ¼¼°±ąŗÅČēĻĀ
£¬ŌŁĄūÓĆĪ“Ņŗ»ÆµÄÓąĘų¼ĢŠųĢ½¾æĘäČČ·Ö½āĒéæö”£ŹµŃé×°ÖĆĶ¼¼°±ąŗÅČēĻĀ![]() µ¼¹ÜŗĶ²æ·Ö¼Š³Ö×°ÖĆŹ”ĀŌ
µ¼¹ÜŗĶ²æ·Ö¼Š³Ö×°ÖĆŹ”ĀŌ![]() £¬Ęä֊װÖĆDŹĒ¹ÄÅŻĘ÷£¬ÓĆÓŚ¼ą²ā
£¬Ęä֊װÖĆDŹĒ¹ÄÅŻĘ÷£¬ÓĆÓŚ¼ą²ā![]() µÄĮ÷ĖŁ”£
µÄĮ÷ĖŁ”£
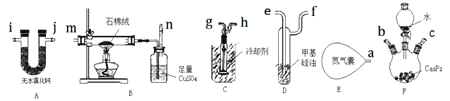
(1)Š“³ö![]() Ė®½ā·ØÖʱø
Ė®½ā·ØÖʱø![]() µÄ»Æѧ·“Ó¦·½³ĢŹ½________”£ÓÉÓŚ
µÄ»Æѧ·“Ó¦·½³ĢŹ½________”£ÓÉÓŚ![]() Ė®½ā·“Ó¦Ģ«¾ēĮŅ£¬ĪŖĮĖ¼õ»ŗ·“Ó¦ĖŁĀŹŹµŃéŹŅæÉÓĆ________“śĢęĖ®”£
Ė®½ā·“Ó¦Ģ«¾ēĮŅ£¬ĪŖĮĖ¼õ»ŗ·“Ó¦ĖŁĀŹŹµŃéŹŅæÉÓĆ________“śĢęĖ®”£
(2)ŹµŃé×°ÖĆ½ÓæŚµÄÕżČ·Į¬½ÓĖ³ŠņĪŖ![]() ________
________![]() ӣ
ӣ
(3)![]() ÖŠŹ¢×°ŹÆĆŽČŽµÄŅĒĘ÷Ćū³ĘŹĒ________£»×°ÖĆE֊װӊ×ćĮæµÄ
ÖŠŹ¢×°ŹÆĆŽČŽµÄŅĒĘ÷Ćū³ĘŹĒ________£»×°ÖĆE֊װӊ×ćĮæµÄ![]() £¬ŹµŃéÖŠŠč³ÖŠųĶØČėŗóŠų×°ÖĆ£¬Ęä×÷ÓĆÖ÷ŅŖÓŠ________
£¬ŹµŃéÖŠŠč³ÖŠųĶØČėŗóŠų×°ÖĆ£¬Ęä×÷ÓĆÖ÷ŅŖÓŠ________![]() “šĮ½µć¼“æÉ
“šĮ½µć¼“æÉ![]() ”£
ӣ
(4)![]() ÖŠ·“Ó¦Ņ»¶ĪŹ±¼äŗ󣬳öĻÖ°×É«ĄÆד¹ĢĢ壬¾¼ģŃéĪŖ°×Į×
ÖŠ·“Ó¦Ņ»¶ĪŹ±¼äŗ󣬳öĻÖ°×É«ĄÆד¹ĢĢ壬¾¼ģŃéĪŖ°×Į×![]() ”£Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½________”£
”£Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½________”£
(5)ŌŚ![]() ČÜŅŗĪüŹÕĪ“·“Ó¦µÄ
ČÜŅŗĪüŹÕĪ“·“Ó¦µÄ![]() ĘųĢå¹ż³ĢÖŠ£¬²śÉś
ĘųĢå¹ż³ĢÖŠ£¬²śÉś![]() ŗĶĮ½ÖÖ³£¼ūµÄ×īøß¼Ūŗ¬ŃõĖį£¬·“Ó¦»Æѧ·½³ĢŹ½ĪŖ________£»ŅŃÖŖ
ŗĶĮ½ÖÖ³£¼ūµÄ×īøß¼Ūŗ¬ŃõĖį£¬·“Ó¦»Æѧ·½³ĢŹ½ĪŖ________£»ŅŃÖŖ![]() ×ćĮæŹ±£¬
×ćĮæŹ±£¬![]() æɼĢŠų±»»¹ŌÉś³ÉCuµ„ÖŹ”£øĆŠ”×éĪŖĮĖ²ā¶Ø“Ė“ĪÖʱø
æɼĢŠų±»»¹ŌÉś³ÉCuµ„ÖŹ”£øĆŠ”×éĪŖĮĖ²ā¶Ø“Ė“ĪÖʱø![]() µÄĢå»ż·ÖŹż£¬ŹÕ¼Æµ½A×°ÖĆ³öæŚµÄĘųĢåĢå»żĪŖ
µÄĢå»ż·ÖŹż£¬ŹÕ¼Æµ½A×°ÖĆ³öæŚµÄĘųĢåĢå»żĪŖ![]() ŅŃÕŪĖćĪŖ±ź×¼×“æö
ŅŃÕŪĖćĪŖ±ź×¼×“æö![]() £¬øÕŗƱ»
£¬øÕŗƱ»![]() µÄ
µÄ![]() ČÜŅŗĶźČ«ĪüŹÕ£¬¾¹żĀĖ”¢Ļ“µÓ”¢øÉŌļŗó£¬µĆµ½
ČÜŅŗĶźČ«ĪüŹÕ£¬¾¹żĀĖ”¢Ļ“µÓ”¢øÉŌļŗó£¬µĆµ½![]() µ„ÖŹ£¬Ōņ
µ„ÖŹ£¬Ōņ![]() µÄĢå»ż·ÖŹżĪŖ________”£
µÄĢå»ż·ÖŹżĪŖ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
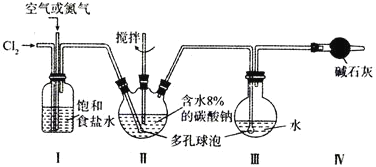
”¾ĢāÄæ”æijŹµŃéŹŅÓĆĻĀĶ¼ĖłŹ¾×°ÖĆÖʱøøßÅØ¶ČµÄ“ĪĀČĖį£¬ĻČŌŚ¢ņÖŠÉś³É![]() £¬ŌŁŌŚ¢óÖŠµĆµ½HClOČÜŅŗ”£
£¬ŌŁŌŚ¢óÖŠµĆµ½HClOČÜŅŗ”£
ŅŃÖŖ£ŗ![]() µÄ·ŠµćĪŖ
µÄ·ŠµćĪŖ![]() £¬
£¬![]() ŅŌÉĻ·Ö½āĪŖ
ŅŌÉĻ·Ö½āĪŖ![]() ŗĶ
ŗĶ![]() £»
£»![]() ¼«Ņ×ČÜÓŚĖ®²¢ÓėĖ®·“Ӧɜ³ÉHClO”£
¼«Ņ×ČÜÓŚĖ®²¢ÓėĖ®·“Ӧɜ³ÉHClO”£
(1)·“Ó¦ÖŠĶØČėæÕĘų»ņµŖĘųµÄ×÷ÓĆŹĒ________________£¬ŹµŃéÖŠæŲÖĘĀČĘųÓėæÕĘų»ņµŖĘųµÄĢå»ż±ČµÄ·½·ØŹĒ_________”£
(2)×°ÖĆ¢ņ”¢¢óÖŠŹ¹Óƶąæ×ĒņÅŻµÄ×÷ÓĆŹĒ_________£»×°ÖĆ¢ņÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_________”£
(3)·“Ó¦Ź±£¬¢ņÖŠŅŖ¼Ó×°ĄäȓװÖĆ£¬ĘäŌŅņŹĒ__________”£
(4)ŅŃÖŖ“ĪĀČĖįæɱ»![]() »¹Ō³É
»¹Ō³É![]() £¬æÉĄūÓĆ“ĖŌĄķ²ā¶Ø¢óÖŠĖłµĆ“ĪĀČĖįČÜŅŗµÄĪļÖŹµÄĮæÅØ¶Č”£
£¬æÉĄūÓĆ“ĖŌĄķ²ā¶Ø¢óÖŠĖłµĆ“ĪĀČĖįČÜŅŗµÄĪļÖŹµÄĮæÅØ¶Č”£
![]() “Ė·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ__________________________”£
“Ė·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ__________________________”£
![]() ĮæČ”
ĮæČ”![]() “ĪĀČĖįČÜŅŗÓŚÉÕ±ÖŠ£¬¼ÓČė×ćĮæµÄ
“ĪĀČĖįČÜŅŗÓŚÉÕ±ÖŠ£¬¼ÓČė×ćĮæµÄ![]() ČÜŅŗ£¬»ģŗĻ¾łŌČŗóŌŁ¼ÓČė×ćĮæµÄ
ČÜŅŗ£¬»ģŗĻ¾łŌČŗóŌŁ¼ÓČė×ćĮæµÄ![]() ČÜŅŗ£¬·“Ó¦ĶźČ«ŗó¹żĀĖ£¬Ļ“µÓ£¬øÉŌļ£¬ÓƵē×ÓĢģĘ½³ĘĮ棬µĆµ½¹ĢĢå
ČÜŅŗ£¬·“Ó¦ĶźČ«ŗó¹żĀĖ£¬Ļ“µÓ£¬øÉŌļ£¬ÓƵē×ÓĢģĘ½³ĘĮ棬µĆµ½¹ĢĢå![]() £¬ŌņĖłÖĘČ”“ĪĀČĖįµÄÅضČĪŖ______
£¬ŌņĖłÖĘČ”“ĪĀČĖįµÄÅضČĪŖ______![]() ”£
ӣ
(5)ČōÖʵĆÉĻŹö“ĪĀČĖįČÜŅŗ![]() £¬×Ŗ»Æ¹ż³ĢÖŠĀȵÄĖšŗÄĪŖ
£¬×Ŗ»Æ¹ż³ĢÖŠĀȵÄĖšŗÄĪŖ![]() £¬ŌņÖĮÉŁŠčŅŖ±źæöĻĀ
£¬ŌņÖĮÉŁŠčŅŖ±źæöĻĀ![]() __________L”£
__________Lӣ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ( )
A.22gN2OŗĶ22gCO2Ėłŗ¬ÓŠµÄÖŹ×ÓŹż¾łĪŖ11NA
B.18gH2OŗĶ18gD2OµÄÖŠ×ÓŹż¶¼ĪŖ10NA
C.78gNa2O2ÖŠĖłŗ¬Ąė×ӵďżÄæĪŖ3NA
D.±ź×¼×“æöĻĀ£¬2.24LD2ŗĶH2µÄ»ģŗĻĘųĢåĖłŗ¬ÖŹ×ÓŹżĪŖ0.2NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æCuClŹĒÉś²śÓ”Ė¢ŃÕĮĻĢŖŻ¼Ą¶µÄÖŲŅŖŌĮĻ£¬¹¤ŅµÉĻæÉÓĆŅ»ÖÖµĶĘ·Ī»Ķæó(Ö÷ŅŖ³É·ÖCuS”¢Cu2S”¢CuO”¢Fe2O3”¢FeO¼°ĘäĖū·ĒĖįČÜŠŌŌÓÖŹ)ŗĶČķĆĢæó(Ö÷ŅŖ³É·ÖĪŖMnO2ŗĶĘäĖū·ĒĖįČÜŠŌŌÓÖŹ)Ą“½ųŠŠÉś²ś£¬¹ż³ĢČēĻĀ£ŗ

»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©²½Öč¢ńÖŠ·“Ó¦½Ļ¶ą£¬ĻĀĮŠ·“Ó¦ŹĒĘäÖŠÖ®Ņ»£ŗCu2S+2MnO2+4H2SO4=2CuSO4+2MnSO4+4H2O+S£¬øĆ·“Ó¦µÄŃõ»Æ²śĪļĪŖ____________________(Ģī»ÆѧŹ½)”£
£Ø2£©ĪŖČ·¶ØĀĖŅŗ1ÖŠŹĒ·ńŗ¬ÓŠFe2+£¬Ź×ĻČÓĆÓŠ»śŻĶČ”¼Į³żČ„ČÜŅŗÖŠMnSO4£¬ŌŁČ”ĻĀ²ćĖ®ČÜŅŗ½ųŠŠ¼ģ²ā£¬ĖłÓĆŹŌ¼ĮĪŖ_____________________”£
£Ø3£©²½Öč¢ņ¼ÓČė°±Ė®æŲÖĘČÜŅŗµÄpHĪŖ5×óÓŅ£¬ÄæµÄŹĒ______________________”£
£Ø4£©ĪŖÄ£Äā²½Öč¢óµÄÉś²ś¹ż³Ģ£¬Ä³Ķ¬Ń§Éč¼ĘČēĻĀŹµŃ飬ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ_____________”£

A.aĶØČėCO2£¬Č»ŗóbĶØČėNH3£»cÖŠ·Å¼īŹÆ»Ņ
B.bĶØČėNH3£¬Č»ŗóaĶØČėCO2£»cÖŠ·Å¼īŹÆ»Ņ
C.aĶØČėNH3£¬Č»ŗóbĶØČėCO2£»cÖŠ·ÅÕŗĻ”ĮņĖįµÄĶŃ֬Ǝ
D.bĶØČėCO2£¬Č»ŗóaĶØČėNH3£»cÖŠ·ÅÕŗĻ”ĮņĖį|µÄĶŃ֬Ǝ
£Ø5£©²½Öč¢ōµÄĀĖŅŗÖŠÖ÷ŅŖ³É·ÖXŹĒ²½Öč¢ņŗĶ²½Öč¢ó¶¼ÓŠµÄ²śĪļ£¬æÉŅŌ»ŲŹÕ×÷ĪŖ·ŹĮĻŹ¹ÓĆ£¬øĆ·ŹĮĻ_______(Ģī”°æÉŅŌ”±»ņ”°²»æÉŅŌ”±)Óė²ŻÄ¾»Ņ(ÓŠŠ§³É·ÖK2CO3)¹²ÓĆ£¬¼ņŹöŌŅņ£ŗ__________”£
£Ø6£©ŅŃÖŖCuClĪŖÄŃČÜÓŚĖ®µÄ°×É«³Įµķ£¬Š“³ö²½Öč¢õ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ_____________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijŗģÉ«¹ĢĢå·ŪĩѳʷæÉÄÜŗ¬ÓŠ![]() ŗĶ
ŗĶ![]() ÖŠµÄŅ»ÖÖ»ņĮ½ÖÖ£¬Ä³»ÆѧŠĖȤŠ”×é¶ŌĘä×é³É½ųŠŠĢ½¾æ£®×ŹĮĻÖ§³Ö£ŗ
ÖŠµÄŅ»ÖÖ»ņĮ½ÖÖ£¬Ä³»ÆѧŠĖȤŠ”×é¶ŌĘä×é³É½ųŠŠĢ½¾æ£®×ŹĮĻÖ§³Ö£ŗ![]() ŌŚĖįŠŌČÜŅŗÖŠ»į·¢Éś·“Ó¦£ŗ
ŌŚĖįŠŌČÜŅŗÖŠ»į·¢Éś·“Ó¦£ŗ![]()
·½°øŅ»£ŗ
(1)ѧɜ¼×ȔɣĮæѳʷӌÉÕ±ÖŠ£¬¼ÓČė¹żĮæÅØĻõĖį£¬²śÉśŅ»ÖÖŗģ×ŲÉ«µÄĘųĢ壮ÓÉ“ĖæÉµĆ³öѳʷ֊Ņ»¶Øŗ¬ÓŠ____£¬Š“³ö²śÉśÉĻŹöĘųĢåµÄ»Æѧ·½³ĢŹ½___”£
(2)½ųŅ»²½Ģ½¾æѳʷ֊ĮķŅ»Öֳɷ֣®ŹµŃé²Ł×÷²½ÖčĪŖ£ŗȔɣĮæÉĻŹöČÜŅŗ£¬___”£
·½°ø¶ž£ŗ
(3)ѧɜŅŅȔɣĮæѳʷӌÉÕ±ÖŠ£¬¼ÓČė¹żĮæĻ”ĮņĖį£¬²¢×÷³öČēĻĀ¼ŁÉčŗĶÅŠ¶Ļ£¬½įĀŪÕżČ·µÄŹĒ______”£
A.Čō¹ĢĢåČ«²æČܽā£¬ĖµĆ÷ѳʷŅ»¶Øŗ¬ÓŠ![]() £¬Ņ»¶Ø²»ŗ¬ÓŠ
£¬Ņ»¶Ø²»ŗ¬ÓŠ![]()
B.Čō¹ĢĢå²æ·ÖČܽā£¬ĖµĆ÷ѳʷŅ»¶Øŗ¬ÓŠ![]() £¬Ņ»¶Ø²»ŗ¬ÓŠ
£¬Ņ»¶Ø²»ŗ¬ÓŠ![]()
C.Čō¹ĢĢåČ«²æČܽā£¬ŌŁµĪ¼ÓKSCNČÜŅŗ£¬ČÜŅŗ²»±äŗģÉ«£¬ĖµĆ÷ѳʷŅ»¶Øŗ¬ÓŠ![]() ŗĶ
ŗĶ![]()
·½°øČż£ŗѧɜ±ūĄūÓĆČēĶ¼ĖłŹ¾×°ÖĆ½ųŠŠŹµŃ飬³ĘĮæ·“Ó¦Ē°ŗó×°ÖĆC֊ѳʷµÄÖŹĮ棬ŅŌČ·¶ØѳʷµÄ×é³É£®»Ų“šĻĀĮŠĪŹĢā£ŗ
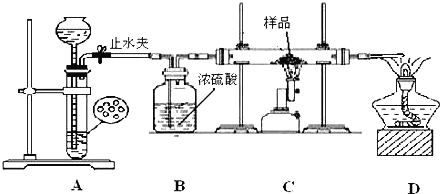
(4)×°ÖĆAŹĒĒāĘųµÄ·¢Éś×°ÖĆ£¬æÉŅŌŹ¹ÓƵÄŅ©Ę·ŹĒ______”£
A.ĒāŃõ»ÆÄĘČÜŅŗŗĶĀĮʬ B.Ļ”ĻõĖįŗĶĢśĘ¬ C.Ļ”ĮņĖįŗĶŠæʬ D.ÅØĮņĖįŗĶĆ¾Ę¬
(5)ĻĀĮŠŹµŃé²½ÖčµÄĻČŗóĖ³ŠņŹĒ______(ĢīŠņŗÅ)”£
¢Ł“ņæŖÖ¹Ė®¼Š£» ¢Ś¹Ų±ÕÖ¹Ė®¼Š£» ¢ŪµćČ¼C“¦µÄ¾Ę¾«ÅēµĘ£»¢ÜĻØĆšC“¦µÄ¾Ę¾«ÅēµĘ ¢ŻŹÕ¼ÆĒāĘų²¢Ńé“æ
(6)¼ŁÉčѳʷȫ²æ²Ī¼Ó·“Ó¦£¬ČōŹµŃéĒ°ŃłĘ·µÄÖŹĮæĪŖ1.6æĖ£¬ŹµŃéŗó³ĘµĆ×°ÖĆCÖŠ¹ĢĢåµÄÖŹĮæĪŖ1.3æĖ£®ŌņѳʷµÄ×é³ÉŹĒ______”£(æÉÄÜÓƵ½µÄĻą¶ŌŌ×ÓÖŹĮæ£ŗFe£ŗ56Cu£ŗ64C£ŗ12O£ŗ16 )
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ(1)Š“³öŅŌŅŅČ²ĪŖŌĮĻÖʱø![]() £Ø¾ŪĀČŅŅĻ©£©µÄ¹ż³ĢÖŠĖł·¢ÉśµÄ·“Ó¦ĄąŠĶ£ŗ____________”¢_____________”£
£Ø¾ŪĀČŅŅĻ©£©µÄ¹ż³ĢÖŠĖł·¢ÉśµÄ·“Ó¦ĄąŠĶ£ŗ____________”¢_____________”£![]() £Ø¾ŪŅŅĻ©£©²ÄĮĻÄæĒ°±»¹«ČĻĪŖ°²Č«²ÄĮĻ£¬Ņ²æÉÓĆÓŚÖĘ×÷±£ĻŹÄ¤ŗĶŅ»“ĪŠŌ²ĶŗŠ”£±ę±š
£Ø¾ŪŅŅĻ©£©²ÄĮĻÄæĒ°±»¹«ČĻĪŖ°²Č«²ÄĮĻ£¬Ņ²æÉÓĆÓŚÖĘ×÷±£ĻŹÄ¤ŗĶŅ»“ĪŠŌ²ĶŗŠ”£±ę±š![]() ŗĶ
ŗĶ![]() ÓŠČżÖÖ·½·Ø£¬Ņ»ŹĒĪÅĘųĪ¶·Ø£ŗ¾ßÓŠ“Ģ¼¤ŠŌĘųĪ¶µÄŹĒ___________________£»¶žŹĒ²āĆÜ¶Č·Ø£ŗĆܶȓóµÄÓ¦ŹĒ___________________£»ČżŹĒČ¼ÉÕ·Ø£ŗ
ÓŠČżÖÖ·½·Ø£¬Ņ»ŹĒĪÅĘųĪ¶·Ø£ŗ¾ßÓŠ“Ģ¼¤ŠŌĘųĪ¶µÄŹĒ___________________£»¶žŹĒ²āĆÜ¶Č·Ø£ŗĆܶȓóµÄÓ¦ŹĒ___________________£»ČżŹĒČ¼ÉÕ·Ø£ŗ![]() µÄµ„ĢåŗĶ
µÄµ„ĢåŗĶ![]() µÄµ„ĢåŌŚ×ćĮææÕĘųÖŠČ¼ÉÕµÄŹµŃéĻÖĻóµÄĆ÷ĻŌĒų±šŹĒ__________”£
µÄµ„ĢåŌŚ×ćĮææÕĘųÖŠČ¼ÉÕµÄŹµŃéĻÖĻóµÄĆ÷ĻŌĒų±šŹĒ__________”£
(2)![]() £Ø
£Ø![]() £©ŹĒŅ»ÖÖ×čøōŠŌøß”¢ČĶŠŌĒ攢»ÆѧĪČ¶ØŠŌŗƵĥķĻė°ü×°²ÄĮĻ£¬¹ć·ŗÓĆÓŚČāÖĘĘ·”¢¶¹ÖĘĘ·µČµÄ°ü×°”£Š“³öŗĻ³É
£©ŹĒŅ»ÖÖ×čøōŠŌøß”¢ČĶŠŌĒ攢»ÆѧĪČ¶ØŠŌŗƵĥķĻė°ü×°²ÄĮĻ£¬¹ć·ŗÓĆÓŚČāÖĘĘ·”¢¶¹ÖĘĘ·µČµÄ°ü×°”£Š“³öŗĻ³É![]() µÄµ„ĢåµÄĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½_________”£
µÄµ„ĢåµÄĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½_________”£
(3) ”°°×É«ĪŪČ¾”±ŹĒÖøø÷ÖÖĖÜĮĻÖĘĘ·¶Ō»·¾³µÄĪŪČ¾”£·ŁÉÕĖÜĮĻ»įÉś³ÉÓŠ¶¾ĪļÖŹ¶žfÓ¢£¬¶žfÓ¢ŹĒŗ¬ÓŠČēĶ¼ĖłŹ¾ÄøĢåµÄĻµĮŠ»ÆŗĻĪļ£¬ĻĀĮŠ¹ŲÓŚČēĶ¼ĖłŹ¾ĪļÖŹµÄĖµ·Ø²»ÕżČ·µÄŹĒ___________________£ØĢīŠņŗÅ£©”£

a£®øĆĪļÖŹŌŚŃõĘųÖŠĶźČ«Č¼ÉյIJśĪļŹĒ![]() ŗĶ
ŗĶ![]()
b£®øĆĪļÖŹŹōÓŚĢž
c£®øĆĪļÖŹµÄŅ»Ā±“śĪļÖ»ÓŠ2ÖÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČżŃõ»Æ¶žÄų![]() ŹĒŅ»ÖÖ»ŅŗŚÉ«ĪŽĘųĪ¶ÓŠ¹āŌóµÄæéדĪļ£¬Ņ×Ėé³ÉĻø·ŪÄ©£¬³£ÓĆÓŚÖĘŌģøßÄܵē³Ų”£¹¤ŅµÉĻŅŌ½šŹōÄų·ĻĮĻ
ŹĒŅ»ÖÖ»ŅŗŚÉ«ĪŽĘųĪ¶ÓŠ¹āŌóµÄæéדĪļ£¬Ņ×Ėé³ÉĻø·ŪÄ©£¬³£ÓĆÓŚÖĘŌģøßÄܵē³Ų”£¹¤ŅµÉĻŅŌ½šŹōÄų·ĻĮĻ![]() ŗ¬ÓŠÉŁĮæµÄĢś”¢ĀĮµČŌÓÖŹ
ŗ¬ÓŠÉŁĮæµÄĢś”¢ĀĮµČŌÓÖŹ![]() £¬¼Ģ¶ųÉś²ś
£¬¼Ģ¶ųÉś²ś![]() µÄ¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ
µÄ¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ
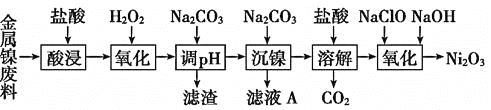
ĻĀ±ķĮŠ³öĮĖĻą¹Ų½šŹōĄė×ÓÉś³ÉĒāŃõ»ÆĪļ³ĮµķµÄ![]() æŖŹ¼³ĮµķµÄpH°“½šŹōĄė×ÓÅضČĪŖ
æŖŹ¼³ĮµķµÄpH°“½šŹōĄė×ÓÅضČĪŖ![]() ¼ĘĖć
¼ĘĖć![]() ”£
ӣ
ĒāŃõ»ÆĪļ |
|
|
|
|
æŖŹ¼³ĮµķµÄpH |
|
|
|
|
³ĮµķĶźČ«µÄpH |
|
|
|
|
(1)ĪŖĮĖĢįøß½šŹōÄų·ĻĮĻ½ž³öµÄĖŁĀŹ£¬ŌŚ”°Ėį½ž”±Ź±æɲÉČ”µÄ“ėŹ©ÓŠ______
A. ½µµĶĪĀ¶Č ![]() ½Į°č
½Į°č ![]() ¼õÉŁŃĪĖįµÄÅضČ
¼õÉŁŃĪĖįµÄÅØ¶Č ![]() ½«·ĻĮĻŃŠ³É·ŪÄ©
½«·ĻĮĻŃŠ³É·ŪÄ©
(2)Ėį½žŗóµÄĖįŠŌČÜŅŗÖŠ¼ÓČė![]() µÄÄæµÄ£ŗ__________”£³ĮÄųĒ°Šč¼Ó
µÄÄæµÄ£ŗ__________”£³ĮÄųĒ°Šč¼Ó![]() æŲÖĘČÜŅŗpH·¶Ī§ĪŖ______£¬ĖłµĆµ½ĀĖŌüµÄÖ÷ŅŖ³É·ÖŹĒ_______”£
æŲÖĘČÜŅŗpH·¶Ī§ĪŖ______£¬ĖłµĆµ½ĀĖŌüµÄÖ÷ŅŖ³É·ÖŹĒ_______”£
(3)“ÓĀĖŅŗAÖŠæÉ»ŲŹÕĄūÓƵÄÖ÷ŅŖĪļÖŹŹĒ![]() ŗĶ________”£
ŗĶ________”£
(4)”°Ńõ»Æ”±Éś³É![]() µÄĄė×Ó·½³ĢŹ½ĪŖ__________________________”£
µÄĄė×Ó·½³ĢŹ½ĪŖ__________________________”£
(5)¹¤ŅµÉĻÓĆÄųĪŖŃō¼«£¬µē½ā![]() ČÜŅŗÓėŅ»¶ØĮæ
ČÜŅŗÓėŅ»¶ØĮæ![]() ×é³ÉµÄ»ģŗĻČÜŅŗ£¬æɵƵ½øß“æ¶Č”¢ĒņŠĪµÄ³¬ĻøÄų·Ū”£µ±ĘäĖūĢõ¼žŅ»¶ØŹ±£¬
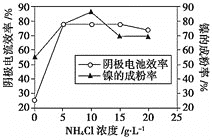
×é³ÉµÄ»ģŗĻČÜŅŗ£¬æɵƵ½øß“æ¶Č”¢ĒņŠĪµÄ³¬ĻøÄų·Ū”£µ±ĘäĖūĢõ¼žŅ»¶ØŹ±£¬![]() µÄÅØ¶Č¶ŌŅõ¼«µēĮ÷Š§ĀŹ¼°ÄųµÄ³É·ŪĀŹµÄÓ°ĻģČēĶ¼ĖłŹ¾£¬Ōņ
µÄÅØ¶Č¶ŌŅõ¼«µēĮ÷Š§ĀŹ¼°ÄųµÄ³É·ŪĀŹµÄÓ°ĻģČēĶ¼ĖłŹ¾£¬Ōņ![]() µÄÅضČ×īŗĆæŲÖĘĪŖ_________”£
µÄÅضČ×īŗĆæŲÖĘĪŖ_________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com