
【题目】下列关于物质结构与性质的说法正确的是
A.标况下,22.4 L C2H2中所含的π键数和18 g冰中所含的氢键数均为2NA
B.由于氢键的作用NH3、H2O、HF的沸点反常,且高低顺序为HF>H2O>NH3
C.VSEPR模型就是分子的空间构型
D.HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱
【答案】A
【解析】
A.乙炔的结构简式为H- C![]() C- H,所以1mol乙炔中含2mol
C- H,所以1mol乙炔中含2mol![]() 键;冰中水分子的O原子以类似于金刚石中C原子的四面体空间网状结构排列,每2个O原子间都有一个H原子,更靠近H原子的O原子与它形成共价键,另一个与它形成氢键,即每个H原子都形成一个氢键,18g冰的物质的量为1mol,所以1mol冰中存在2mol氢键,即标况下,22.4 L C2H2中所含的π键数和18 g冰中所含的氢键数均为2NA,故A正确;
键;冰中水分子的O原子以类似于金刚石中C原子的四面体空间网状结构排列,每2个O原子间都有一个H原子,更靠近H原子的O原子与它形成共价键,另一个与它形成氢键,即每个H原子都形成一个氢键,18g冰的物质的量为1mol,所以1mol冰中存在2mol氢键,即标况下,22.4 L C2H2中所含的π键数和18 g冰中所含的氢键数均为2NA,故A正确;
B.氢键的作用力大于分子间作用力,由于氢键的作用NH3、H2O、HF的沸点反常,且常温下H2O为液态,所以沸点由高到低的顺序为H2O>HF>NH3,故B错误;
C. VSEPR模型可用来预测分子的立体构型,但不一定是分子的空间构型,还要考虑孤电子对的影响,故C错误;
D. F、Cl、Br、I属于同主族元素,同主族从上到下非金属性减弱,其氢化物的热稳定性减弱,还原性增强,故D错误;
故答案:A。


科目:高中化学 来源: 题型:
【题目】立方烷(C8H8)外观为有光泽的晶体。其八个碳原子对称地排列在立方体的八个角上。以下相关说法错误的是
A. 立方烷在空气中可燃,燃烧有黑烟产生
B. 立方烷一氧代物1种、二氯代物有3种、三氯代物也有3种
C. 立方烷是苯(C6H6)的同系物、也是苯乙烯(C6H5-CH=CH2)的同分异构体
D. 八硝基立方烷完全分解可能只产生二氧化碳和氮气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.0×10-16。下列关于难溶物之间转化的说法中错误的是( )
A.AgCl不溶于水,不能转化为AgI
B.两种难溶物的Ksp相差越大,难溶物就越容易转化为更难溶的物质
C.AgI比AgCl更难溶于水,所以AgCl可以转化为AgI
D.常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中铋元素的数据如图,下列说法正确的是
![]()
A.Bi元素的质量数为209B.Bi元素在周期表中的位置位于第六周期IIIA族
C.Bi原子有3个未成对电子D.Bi原子最外层有5个能量相同的电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度时,将nmolL-1氨水滴入10mL1.0molL-1盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,下列有关说法正确的是( )

A.a点Kw=1.0×10-14
B.水的电离程度:b>c>a>d
C.b点:c(NH4+)>c(Cl-)>c(H+)>c(OH-)
D.25℃时NH4Cl水解常数为(n-1)×10-7molL-1(用n表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是生产生活中的常见有机物的分子式、结构式、结构简式或名称有关说法正确的是
①![]() ②
②![]() ③
③![]() ④
④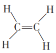 ⑤CH3CH2OH⑥C6H12O6⑦CH3COOH⑧硬脂酸甘油酯⑨蛋白质⑩聚乙烯
⑤CH3CH2OH⑥C6H12O6⑦CH3COOH⑧硬脂酸甘油酯⑨蛋白质⑩聚乙烯
A.能跟溴的四氯化碳溶液发生加成反应并使之褪色的有①②④⑩
B.含碳量最高、有毒、常温下为液体且点燃时有浓烟的是①
C.属于高分子材料的是⑧⑨⑩
D.投入钠能产生H2的是⑤⑦⑧⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2CO(g)+O2(g)=2CO2(g) △H=-566 kJ·mol-1
2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g) △H=-452 kJ·mol-1
根据以上热化学方程式判断,下列说法正确的是
A. 1molCO 完全燃烧,放出热量为283 J
B. Na2O2(s)+CO2(s)=Na2CO3(s)+ ![]() O2(g) △H=-226 kJ·mol-l
O2(g) △H=-226 kJ·mol-l
C. CO(g) 与Na2O2(s)反应放出509kJ 热量时,电子转移数为1.204×1024
D. CO 的燃烧热为566 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构与H2O2类似,熔点为193K,沸点为411K,遇水很容易水解,产生的气体能使品红褪色,S2Cl2可由干燥氯气通入熔融的硫中制得。下列有关说法正确的是
A. S2Cl2的电子式为![]()
B. 固态时S2Cl2属于原子晶体
C. S2Cl2与NaOH的化学方程式可能为:S2Cl2+6NaOH=2NaCl+Na2SO3+Na2S+3H2O
D. S2Cl2是含有极性键和非极性键的离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于10 mL 0.1 mol·L-1的NH3·H2O溶液,下列说法正确的是( )
A.25 ℃时,若溶液的pH=11,则Kb(NH3·H2O)=1×10-6mol·L-1
B.向溶液中加入少量CH3COONa固体,溶液中的![]() 值变小
值变小
C.向溶液中加入10 mL 0.1 mol·L-1HCl,所得溶液中离子浓度大小顺序为c(NH4+)>c(Cl-)>c(H+)>c(OH-)
D.向溶液中加入5 mL 0.1 mol·L-1HCl,所得溶液中离子的浓度一定符合:c(NH4+)+c(H+)=c(Cl-)+c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com