
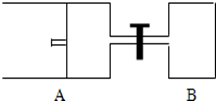
·ÖĪö £Ø1£©AÖŠæŖŹ¼ĪļÖŹµÄĮæĪŖ2mol£¬Ģå»żĪŖaL£¬Ę½ŗāŹ±Ģå»żĪŖ1.2aL£¬½įŗĻĪļÖŹµÄĮæÓėĢå»ż³ÉÕż±Č¼°²īĮæ·Ø¼ĘĖć£»
£Ø2£©AÖŠŗćŃ¹£¬BÖŠĪļÖŹµÄĮæŌö“ó”¢Ģå»ż²»±äŹ±£¬Ń¹ĒæŌö“ó£¬Ę½ŗāÄęĻņŅĘ¶Æ£»
£Ø3£©AÖŠŗćŃ¹£¬BÖŠĪļÖŹµÄĮæŌö“ó”¢Ģå»ż²»±äŹ±£¬Ń¹ĒæŌö“ó£»
£Ø4£©ĻņAÖŠ³äČė1molXŗĶ1molY“ļµ½Ę½ŗāŹ±£¬VA=1.2aL£»µ±“ņæŖKŹ±£¬ABÖŠĘųĢå¹²ĪŖ3molXŗĶ3molY£¬ĪļÖŹµÄĮæÓėĢå»ż³ÉÕż±Č£¬æÉÖŖĘ½ŗāŹ±×ÜĢå»żĪŖ3.6L£»
£Ø5£©øĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬ÉżøßĪĀ¶Č£¬Ę½ŗāÄęĻņŅĘ¶Æ£¬ĘųĢåµÄ×ÜĪļÖŹµÄĮæ¼õŠ”£¬Ōņ×ÜĢå»ż¼õŠ”£®
½ā“š ½ā£ŗ£Ø1£©µČŃ¹”¢µČĪĀĢõ¼žĻĀ£¬ĘųĢåµÄĢå»żÖ®±ČµČÓŚĘųĢåµÄĪļÖŹµÄĮæÖ®±Č£¬2molĘųĢåŹ±£¬Ģå»żĪŖaL£¬“ļµ½Ę½ŗāŹ±£¬VA=1.2a L£¬ĖłŅŌĘ½ŗāŗó»ģŗĻĘųĢåµÄĪļÖŹµÄĮæŹĒ2.4mol£¬
Éč²Ī¼Ó·“Ó¦µÄAĪļÖŹĪŖm mol£¬
X£Øg£©+Y£Øg£©?2Z£Øg£©+W£Øg£© ĪļÖŹµÄĮæŌö¶ą
1mol 1mol
nmol £Ø2.4-2£©mol
n=0.4
ĖłŅŌXĪļÖŹµÄ×Ŗ»ÆĀŹĪŖ$\frac{0.4mol}{1mol}$”Į100%=40%£¬
¹Ź“š°øĪŖ£ŗ40%£»
£Ø2£©B×°ÖĆŹĒŌŚµČČŻĢõ¼žĻĀ£¬·“Ó¦ĻņÕż·“Ó¦·½ĻņŅĘ¶ÆŹ±£¬»ģŗĻĘųĢåµÄĪļÖŹµÄĮæŌö“󣬵¼ÖĀČŻĘ÷ÄŚĘųĢåŃ¹ĒæŌö“ó£¬Ōö“óŃ¹ĒæÄÜŅÖÖĘXµÄ×Ŗ»ÆĀŹ£¬ĖłŅŌXµÄ×Ŗ»ÆĀŹ¼õŠ”£¬ĖłŅŌBČŻĘ÷ÖŠXµÄ×Ŗ»ÆĀŹ±ČAŠ”£»
¹Ź“š°øĪŖ£ŗ£¾£»
£Ø3£©BÖŠĪļÖŹµÄĮæĪŖAÖŠĪļÖŹµÄĮæµÄ2±¶£¬AÖŠŗćŃ¹£¬BÖŠĪļÖŹµÄĮæŌö“ó”¢Ģå»ż²»±äŹ±£¬Ń¹ĒæŌö“ó£¬Ę½ŗāŹ±µÄŃ¹Ēæ£ŗP£ØB£©£¾2P£ØA£©£¬
¹Ź“š°øĪŖ£ŗ£¾£»
£Ø4£©µ±“ņæŖKŹ±£¬Õūøö×°ÖĆŹĒŌŚµČĪĀ”¢µČŃ¹Ģõ¼žĻĀ·“Ó¦£¬Ź¹Õūøö×°ÖĆÖŠĘųĢåµÄŃ¹ĒæÓėA×°ÖĆÖŠµÄ³õŹ¼Ń¹ĒæĻąĶ¬Ź±£»ĻņAÖŠ³äČė1molXŗĶ1molY“ļµ½Ę½ŗāŹ±£¬VA=1.2aL£»µ±“ņæŖKŹ±£¬ABÖŠĘųĢå¹²ĪŖ3molXŗĶ3molY£¬ÓÉÓŚÕūøö×°ÖĆŹĒŌŚµČĪĀ”¢µČŃ¹Ģõ¼žĻĀµÄ·“Ó¦£¬“ļµ½Ę½ŗāדĢ¬Ź±£¬»ģŗĻĘųĢåµÄĢå»żŹĒ3.6aL£¬ĘäÖŠBŹĒaL£¬ĖłŅŌAĢå»żĪŖ2.6aL£¬
¹Ź“š°øĪŖ£ŗ2.6a£»
£Ø5£©øĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬ÉżøßĪĀ¶Č£¬Ę½ŗāÄęĻņŅĘ¶Æ£¬ĘųĢåµÄ×ÜĪļÖŹµÄĮæ¼õŠ”£¬Ōņ×ÜĢå»ż¼õŠ”£¬BµÄĢå»ż²»±ä£¬ŌņAµÄĢå»ż±äŠ”£¬¹Ź“š°øĪŖ£ŗ±äŠ”£®
µćĘĄ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗāµÄ¼ĘĖć£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕĪļÖŹµÄĮæÓėĢå»ż³ÉÕż±Č”¢Ę½ŗāŅĘ¶ÆµÄÓ°ĻģĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓė¼ĘĖćÄÜĮ¦µÄ漲飬עŅā²īĮæ·Ø¼ĘĖćµÄÓ¦ÓĆ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £Ø1£©·“Ó¦Fe£Øs£©+CO2£Øg£©?FeO£Øs£©+CO£Øg£©”÷H1£¬Ę½ŗā³£ŹżĪŖK1£»·“Ó¦Fe£Øs£©+H2O£Øg£©?FeO£Øs£©+H2£Øg£©”÷H2£¬Ę½ŗā³£ŹżĪŖK2£®ŌŚ²»Ķ¬ĪĀ¶ČŹ±K1”¢K2µÄÖµČē±ķ£ŗ
£Ø1£©·“Ó¦Fe£Øs£©+CO2£Øg£©?FeO£Øs£©+CO£Øg£©”÷H1£¬Ę½ŗā³£ŹżĪŖK1£»·“Ó¦Fe£Øs£©+H2O£Øg£©?FeO£Øs£©+H2£Øg£©”÷H2£¬Ę½ŗā³£ŹżĪŖK2£®ŌŚ²»Ķ¬ĪĀ¶ČŹ±K1”¢K2µÄÖµČē±ķ£ŗ| 700”ę | 900”ę | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł=¢Ś£¾¢Ū£¾¢Ü | B£® | ¢Ł=¢Ś=¢Ū=¢Ü | C£® | ¢Ł=¢Ś=¢Ü£¾¢Ū | D£® | ¢Ł£¾¢Ū£¾¢Ś£¾¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ČŻĘ÷ | ¼× | ŅŅ |
| ·“Ó¦ĪļĶ¶ČėĮæ | 2mol CO2”¢6mol H2 | a mol CO2”¢b mol H2 c mol CH3OH£Øg£©”¢c mol H2O£Øg£© |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | »ż¼«ĶĘ¹ćĢ«ŃōÄÜ”¢·ēÄÜ”¢µŲČČÄܼ°Ė®Äܵȵď¹ÓĆ£¬¼õÉŁ»ÆŹÆČ¼ĮĻµÄŹ¹ÓĆ | |
| B£® | ¼ÓĒæ³ĒŹŠÉś»īĪŪĖ®ĶѵŖ³żĮד¦Ąķ£¬¶ōÖĘĖ®Ģåø»ÓŖŃų»Æ | |
| C£® | ½«·Ļ¾Éµē³ŲÉīĀń£¬·ĄÖ¹ĘäÖŠµÄÖŲ½šŹōĄė×ÓĪŪČ¾»·¾³ | |
| D£® | “óĮ¦ŹµŹ©æóĪļČ¼ĮĻ”°ĶŃĮņ”¢ĶŃĻõ¼¼Źõ”±£¬¼õÉŁĮņµÄŃõ»ÆĪļŗĶµŖµÄŃõ»ÆĪļĪŪČ¾ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś | B£® | ¢Ś¢Ū | C£® | ¢Ł¢Ū | D£® | ¢Ś¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¦Ń1£¾¦Ń2£¾¦Ń3£¾¦Ń4 | B£® | ¦Ń1£¾¦Ń2£¾¦Ń4£¾¦Ń3 | C£® | ¦Ń2£¾¦Ń1£¾¦Ń3£¾¦Ń4 | D£® | ¦Ń2£¾¦Ń1£¾¦Ń4£¾¦Ń3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com