
【题目】近20年来,对以氢气作为未来的动力燃料氢能源的研究获得了迅速发展,像电一样,氢是一种需要依靠其他能源如石油、煤、原子能等的能量来制取的所谓“二级能源”,而存在于自然界的可以提供现成形式能量的能源称为一级能源,如煤、石油、太阳能和原子能。
(1)氢气燃烧时耗氧量小,发热量大。已知,热化学方程式:
C(g)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
H2(g)+1/2O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
试通过计算说明等质量的氢气和碳燃烧时产生热量的比是________。
(2)氢能源有可能实现能源贮存,也有可能实现经济、高效的输送。研究表明在过渡金属型氢化物(又称间充氢化物)中,氢原子填充在金属的晶格间隙之间,其组成不固定,通常是非化学计量的,如LaH2.76、TiH1.73、CeH2.69、ZrH1.98、PrH2.85、TaH0.78。已知标准状况下,1体积的钯粉大约可吸附896体积的氢气(钯粉的密度为10.64g·cm-3,相对原子质量为106.4),试写出钯(Pd)的氢化物的化学式________________。
【答案】4.36∶1 PdH0.8
【解析】
(1)根据热化学方程式的意义求出1克物质燃烧放出的热量,然后求出比值;
(2)设1体积为1cm3,求出钯粉的质量和物质的量;再根据1体积的钯粉大约可吸附标准状况下896体积的氢气,求出氢气的物质的量,根据两种原子的物质的量之比,写出其化学式。
(1)由C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1可知,1g碳完全燃烧放出热量为![]() ;由H2(g)+
;由H2(g)+![]() O2(g)=H2O(l) △H=-285.8kJ·mol-1可知,1g氢气完全燃烧放出热量为
O2(g)=H2O(l) △H=-285.8kJ·mol-1可知,1g氢气完全燃烧放出热量为![]() ;等质量的氢气和碳燃烧时产生热量的比是
;等质量的氢气和碳燃烧时产生热量的比是 =4.36:1,
=4.36:1,
故答案为:4.36:1;
(2)设1体积为1cm3,则1cm3的钯粉的质量m=ρV=10.64g/cm3×1cm3=10.64g,钯的物质的量n(Pd)=![]() =
=![]() =0.1mol,由1体积钯粉约可吸附标准状况下896体积氢气,可知被吸附氢气的体积为896cm3=0.896L,氢气的物质的量n(H2)=
=0.1mol,由1体积钯粉约可吸附标准状况下896体积氢气,可知被吸附氢气的体积为896cm3=0.896L,氢气的物质的量n(H2)=![]() =
=![]() =0.04mol,所以钯与氢气反应的物质的量之比为
=0.04mol,所以钯与氢气反应的物质的量之比为![]() ,则产物中Pd与H数目之比为
,则产物中Pd与H数目之比为![]() =
=![]() ,所以钯的氢化物化学式为PdH0.8,
,所以钯的氢化物化学式为PdH0.8,
故答案为:PdH0.8


 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.根据类推思想,氯化铝溶液蒸干后灼烧,最后得到氧化铝,则硫酸铝也一样
B.高温高压下的超临界水,溶液中的氢离子和氢氧根离子浓度较大,有时显酸性,有时显碱性
C.如图可表示水分解过程中的能量变化
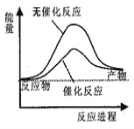
D.等体积、等浓度的醋酸钠溶液和次氯酸钠溶液中,所含离子总数前者小于后者
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知苯甲酸的酸性比碳酸强,苯酚的酸性比碳酸弱。则可以将
 转变为
转变为![]() 的方法是( )
的方法是( )
①与足量的NaOH溶液共热,再通入CO2②与稀硫酸共热后,加入足量的NaOH溶液③加热溶液,通入足量的CO2④与稀H2SO4共热后,加入足量的NaHCO3
A. ①②B. ①④C. ②③D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备1,2二溴乙烷的反应原理如下:CH3CH2OH![]() CH2=CH2↑+H2O,CH2=CH2+Br2→BrCH2CH2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:
CH2=CH2↑+H2O,CH2=CH2+Br2→BrCH2CH2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:

有关数据列表如下:
乙醇 | 1,2二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在装置c中应加入________(选填序号),其目的是吸收反应中可能生成的酸性气体。
①水 ②浓硫酸 ③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)判断d管中制备二溴乙烷反应已结束的最简单方法是______________________。
(3)将二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的________(填“上”或“下”)层。
(4)若产物中有少量未反应的Br2,最好用________(填正确选项前的序号)洗涤除去。
①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(5)反应过程中需用冷水冷却(装置e),其主要目的是______________________; 但不用冰水进行过度冷却,原因_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在1×105Pa,298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是
A. H2O(g)=H2(g)+![]() O2(g) △H=+484kJ/mol
O2(g) △H=+484kJ/mol
B. 2H2(g)+O2(g)=2H2O(l) △H=-484kJ/mol
C. H2(g)+![]() O2(g)=H2O(l) △H=+242kJ/mol
O2(g)=H2O(l) △H=+242kJ/mol
D. H2O(g)=H2(g)+![]() O2(g) △H=+242kJ/mol
O2(g) △H=+242kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是生活生产中常见的物质,表中列出了它们的(主要)成分
编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
名称 | 酒 精 | 醋酸 | 火碱 | 食盐 | 铜线 | 氨气 | 苏打 | 小苏打 |
主要成分 | CH3CH2OH | CH3COOH | NaOH | NaCl | Cu | NH3 | Na2CO3 | NaHCO3 |
根据情景回答问题
(1)请你对表中①~的主要成分进行分类:属于电解质的是____________(填编号)
(2)写出⑧的主要成分溶于水的电离方程式_______________________________
(3)写出NaHCO3受热分解的化学方程式_______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有效去除大气中的NOx,保护臭氧层,是环境保护的重要课题。
(1)在没有NOx催化时,O3的分解可分为以下两步反应进行;
①O3=O+O2 (慢) ②O+O3=2O2 (快)
第一步的速率方程为v1=k1c(O3),第二步的速率方程为v2=k2c(O3)·c(O)。其中O为活性氧原子,它在第一步慢反应中生成,然后又很快的在第二步反应中消耗,因此,我们可以认为活性氧原子变化的速率为零。请用k1、k2组成的代数式表示c(O)=____________。
(2)NO做催化剂可以加速臭氧反应,其反应过程如图所示:
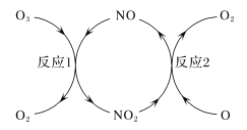
已知:O3(g)+O(g)=2O2(g) ΔH=-143 kJ/mol
反应1:O3(g)+NO(g)=NO2(g)+O2(g) ΔH1=-200.2 kJ/mol。
反应2:热化学方程式为____________________________。
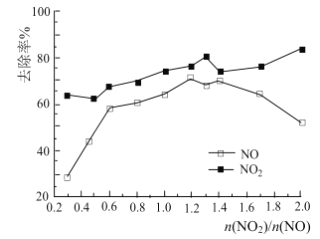
(3)一定条件下,将一定浓度NOx(NO2和NO的混合气体)通入Ca(OH)2悬浊液中,改变![]() ,NOx的去除率如图所示。
,NOx的去除率如图所示。
已知:NO与Ca(OH)2不反应;
NOx的去除率=1-![]() ×100%
×100%
①![]() 在0.3-0.5之间,NO吸收时发生的主要反应的离子方程式为:___________。
在0.3-0.5之间,NO吸收时发生的主要反应的离子方程式为:___________。
②当![]() 大于1.4时,NO2去除率升高,但NO去除率却降低。其可能的原因是__________。
大于1.4时,NO2去除率升高,但NO去除率却降低。其可能的原因是__________。
(4)若将CO和NO按不同比例投入一密闭容器中发生反应:2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-759.8 kJ/mol,反应达到平衡时,N2的体积分数随![]() 的变化曲线如图。
的变化曲线如图。
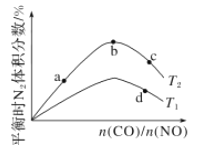
①b点时,平衡体系中C、N原子个数之比接近________。
②a、b、c三点CO的转化率从小到大的顺序为________;b、c、d三点的平衡常数从大到小的顺序为__________(以上两空均用a、b、c、d表示)。
③若![]() =0.8,反应达平衡时,N2的体积分数为20%,则NO的转化率为_____。
=0.8,反应达平衡时,N2的体积分数为20%,则NO的转化率为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知白磷和P4O6的分子结构如图所示,又知化学键的键能是形成(或断开)1 mol化学键时释放(或吸收)的能量,现查知P—P键能为198 kJ·mol-1、P—O键能为360 kJ·mol-1、O===O键能为498 kJ·mol-1。若生成1 mol P4O6,则反应P4(白磷)+3O2=P4O6中的能量变化为( )
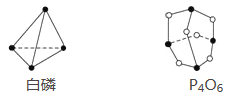
A. 吸收1 638 kJ能量 B. 放出1 638 kJ能量
C. 吸收126 kJ能量 D. 放出126 kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有以下物质相互转化
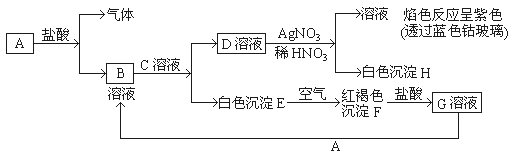
试回答:(1)写出B的化学式_________,D的化学式 ______。
(2)写出由E转变成F的化学方程式 ______________。
(3)写出G转化成B的离子方程式 ___________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com