
某合成气的主要成分是一氧化碳和氢气,可用于合成甲醚等清洁燃料。由天然气获得该合成气过程中可能发生的反应有:
①CH4(g)+H2O(g)CO(g)+3H2(g) ΔH1=+206.1 kJ·mol-1
②CH4(g)+CO2(g)2CO(g)+2H2(g) ΔH2=+247.3 kJ·mol-1
③CO(g)+H2O(g)CO2(g)+H2(g) ΔH3
请回答下列问题:
(1)在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示。
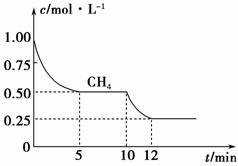
图1
反应进行的前5 min内,v(H2)=________;10 min时,改变的外界条件可能是______________________________________________________________。
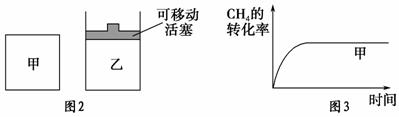
(2)如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。已知甲容器中CH4的转化率随时间的变化如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图像。
(3)反应③中ΔH3=________。800 ℃时,反应③的平衡常数K=1,测得该温度下密闭容器中某时刻各物质的物质的量见下表:
| CO | H2O | CO2 | H2 |
| 0.5 mol | 8.5 mol | 2.0 mol | 2.0 mol |
此时反应③中正、逆反应速率的关系式是________(填代号)。
a.v正>v逆 B.v正<v逆
c.v正=v逆 D.无法判断
(4)用该合成气制取甲醚的化学方程式为______________________________。
该反应的原子利用率为________(设反应完全进行,用质量百分比表示)。
解析 (1)可根据图像先计算CH4的反应速率,再计算H2的生成速率。10 min时,改变的条件不可能是增大容器的体积(否则改变条件的瞬间CH4浓度应突然减小),由于c(CH4)减小,平衡右移,故改变的条件可能是升高温度(或充入水蒸气)。(2)甲容器反应开始后压强增大,乙容器压强不变、体积增大,可看成是由甲减压得到乙,故乙容器的反应速率慢,平衡右移,CH4的转化率大。(3)根据盖斯定律,反应①减去反应②即可得到反应③,进而通过计算求得ΔH3。根据浓度商: =0.94<K=1,可知反应向正反应方向进行,即
=0.94<K=1,可知反应向正反应方向进行,即
v正>v逆。(4)根据质量守恒定律可知,反应的化学方程式为2CO+4H2===CH3OCH3+H2O,可以求出甲醚质量占反应物总质量的71.9%。
答案 (1)0.3 mol·L-1·min-1 升高温度(或充入水蒸气)
(2)

(3)-41.2 kJ·mol-1 a
(4)2CO+4H2===CH3OCH3+H2O 71.9%


科目:高中化学 来源: 题型:
下列实验基本操作正确的是( )
A.稀释浓硫酸时,将水沿器壁缓慢注入浓硫酸中
B.过滤时,漏斗里液体的液面要高于滤纸的边缘
C.胶头滴管的管口直接伸入试管里滴加液体,以免外溅
D.实验室取用液体药品做实验时,如没有说明用量,一般取1~2 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
CO和NO都是汽车尾气中的有害物质,它们之间能缓慢地发生如下反应:2NO(g)+2CO(g)N2(g)+2CO2(g) ΔH<0,现利用此反应,拟设计一种环保装置,用来消除汽车尾气对大气的污染,下列设计方案可以提高尾气处理效果的是 ( )。
①选用适当的催化剂 ②提高装置温度 ③降低装置的压强 ④装置中放入碱石灰
A.①③ B.②④
C.①④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙三个容器中最初存在的物质及数量如图所示,三个容器最初的容积相等,温度相同,反应中甲、丙的容积不变,乙中的压强不变,在一定温度下反应达到平衡。下列说法正确的是 ( )。
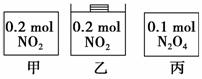
A.平衡时各容器内c(NO2)的大小顺序为乙>甲>丙
B.平衡时N2O4的百分含量:乙>甲=丙
C.平衡时甲中NO2与丙中N2O4的转化率不可能相同
D.平衡时混合物的平均相对分子质量:甲>乙>丙
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解400 mL一定浓度的硫酸铜溶液(不考虑电解过程中溶液体积的变化),通电一段时间后,如果向所得的溶液中加入0.05 mol Cu2(OH)2CO3后,使溶液恰好恢复到电解前的浓度和体积(不考虑CO2的溶解),电解过程中转移的电子物质的量为( )
A.0.2 mol
B. 0.3mol
C. 0.4 mol
D. 0.6 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
如下图所示是根据图甲的电解池进行电解时某个量(纵坐标x)随时间变化的函数图像(各电解池都用石墨作电极,不考虑电解过程中溶液浓度变化对电极反应的影响),这个量x是表示( )
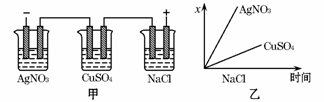 A.各电解池析出气体的体积
A.各电解池析出气体的体积
B.各电解池阳极质量的增加量
C.各电解池阴极质量的增加量
D.各电极上放电的离子总数
查看答案和解析>>
科目:高中化学 来源: 题型:
Harbermann等设计出利用Desulfovibrio desulfurcan菌种生成的硫化物作为介体的微生物燃料电池,电池内部有质子通过,该系统不经任何维护可连续运行5年。该电池的负极反应式为S2-+4H2O-8e-===SO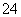 +8H+。有关该电池的下列说法中正确的是 ( )。
+8H+。有关该电池的下列说法中正确的是 ( )。
A.若有1.12 L氧气参与反应,则有0.2 mol电子发生转移
B.质子由正极移向负极
C.该电池的总反应为S2-+2O2===SO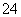
D.正极的电极反应式为2O2+8e-+4H2O===8OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
为增强金属制品的抗蚀性能,需要对金属进行表面处理。如图为铝的阳极氧化法表面处理技术原理示意图,可使铝制品表面生成一层致密的氧化膜。则下列说法不正确的是( )

A.阳极反应为2Al+3H2O-6e-===Al2O3+6H+
B.阴极反应为2H++2e-===H2↑
C.电解一段时间后溶液的pH升高
D.表面生成的致密的氧化膜不溶于稀硫酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com