现有0.03mol/L的BaCl2溶液200ml,加入0.02mol/L的CuSO4溶液400mL反应后,溶液中离子浓度大小判别正确的是( )
A.c(Cu2+)>c(Cl-)>c(SO42-)>c(Ba2+)
B.c(Cl-)>c(Cu2+)>c(SO42-)>c(Ba2+)
C.c(Cu2+)>c(Cl-)>c(SO42-)=c(Ba2+)
D.c(Cl-)>c(Cu2+)>c(SO42-)=c(Ba2+)
【答案】
分析:0.03mol/L的BaCl
2溶液200ml,加入0.02mol/L的CuSO
4溶液400mL反应后,反应生成硫酸钡和氯化铜,还剩余硫酸铜,以此来解答.
解答:解:0.03mol/L的BaCl
2溶液200ml,加入0.02mol/L的CuSO
4溶液400mL反应后,反应生成硫酸钡和氯化铜,还剩余硫酸铜,
c(Cl
-)=
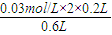
=0.02mol/L,c(Cu
2+)=
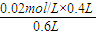
=0.013mol/L,
因硫酸钡不溶于水,发生反应时剩余硫酸根离子,
则离子浓度关系为c(Cl
-)>c(Cu
2+)>c(SO
42-)>c(Ba
2+),
故选B.
点评:本题考查离子浓度大小的比较,注意发生的复分解反应生成硫酸钡是解答的关键,注意混合后溶液体积的变化,题目难度不大.

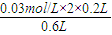 =0.02mol/L,c(Cu2+)=
=0.02mol/L,c(Cu2+)=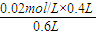 =0.013mol/L,
=0.013mol/L,

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案