
下列两组热化学方程式中,有关ΔH的比较正确的是 ( )
①CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH1
CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH2
②NaOH(aq)+ H2SO4(浓)===
H2SO4(浓)=== Na2SO4(aq
Na2SO4(aq )+H2O(l) ΔH3
)+H2O(l) ΔH3
NaOH(aq)+CH3COOH(aq)===CH3COONa(aq)+H2O(l) ΔH4
A.ΔH1>ΔH2;ΔH3>ΔH4 B.ΔH1>ΔH2;ΔH3<ΔH4
C.ΔH1=ΔH2;ΔH3<ΔH4 D.ΔH1<ΔH2;ΔH3>ΔH4
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
.0.01 mol氯化铬(CrCl3·6H2O)在水溶液中用过量AgNO3处理,产生0.02 mol AgCl沉淀,此氯化铬在溶液中的存在形式最可能为
A.[Cr(H2O)6] Cl3 B.[Cr(H2O)5Cl]Cl2·H2O
C.[Cr(H2O)4Cl2]Cl·2H2O D.[Cr(H2O)3Cl3]·3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
依据事实,写出下列反应的热化学方程式。
(1)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成Si O2和液态H2O。已知室温下2 g SiH4自燃放出热量89.2 kJ。SiH4自燃的热化学方程式为_________________
O2和液态H2O。已知室温下2 g SiH4自燃放出热量89.2 kJ。SiH4自燃的热化学方程式为_________________
________________________________________________________________________。
(2)在25 ℃、101 kPa下,一定质量的无水乙醇完全燃烧时放出热量Q kJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100 g CaCO3沉淀,则乙醇燃烧的热化学方程式为________________________________________________________________________
_________________________ _______________________________________________。
_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:P4(g)+6Cl2(g)===4PCl3(g),
ΔH=a k J·mol-1,
J·mol-1,
P4(g)+10Cl2(g)===4PCl5(g) ΔH=b kJ·mol-1,
P4具有正四面体结构,PCl5中P—Cl键的键能为c kJ·mol-1,PCl3中P—Cl键的键能为1.2c kJ·mol-1。
下列叙述正确的是 ( )
A.P—P键的键能大于P—Cl键的键能
B.可求Cl2(g)+PCl3(g)===PCl5(s)的反应热ΔH
C.Cl—Cl键的键能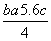 kJ·mol-1
kJ·mol-1
D.P—P键的键能为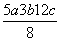 kJ·mol-1
kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
根据碘与氢气反应的热化学方程式
(ⅰ)I2(g)+H2(g)2HI(g) ΔH=-9.48 kJ·mol-1
(ⅱ)I2(s)+H2(g)2HI(g) ΔH=26.48 kJ·mol-1
下列判断正确的是 ( )
A.1 mol I2(s)中通入2 g H2(g),反应吸热26.48 kJ
B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ
C.反应(ⅱ)的反应物总能量比反应(ⅰ)的反应物总能量低
D.反应(ⅰ)放出的热量多,所以产物的能量低,比反应(ⅱ)的产物更稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
在量热计(如图)中将100 mL 0.50 mol·L-1的CH3COOH溶液与
100 mL 0.55 mol·L-1 NaOH溶液混合,温度从298.0 K升高到
300.7 K。已知量热计的热容常数(量热计各部件每升高1 K所需要的热量)是150.5 J·K-1,溶液密度均为1 g·mL-1,生成溶液的比热容c=4.184 J·g-1·K(已知CH3COOH电离要吸热)。
(1)CH3COOH的中和热ΔH=_____________________________。
(2)CH3COOH中和热的文献值为-56.1 kJ·mol-1,你认为造成(1)中 测得的实验值有偏差的可能原因是____________________________________________
________________________________________________________________________。
(3)实验中NaOH溶液过量的目的是_________________________________________。
(4)你认为CH3COOH的中和热与盐酸的中和热绝对值相比,__________的较大,其原因是________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列四个数据是在不同条件下测出的合成氨反应的速率,其中最快是( )
A.V(H2)==0.1 mol/(L·min) B.V(N2)==0.1mol/(L·min)
C.V(NH3)==0.15mol/(L·min) D. V(N2)==0.002mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
2-丁烯的结构简式正确的是 ( )
A.CH2=CHCH2CH3 B.CH3CH=CHCH3 C.CH2=CHCH=CH2 D.CH2=C=CHCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
石油化工的废气中有H2S。写出从废气中回收单质硫的两种方法(除空气外,不使用其他原料),以化学方程式表示。_____________________、______________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com