
| |||||||||||||||
科目:高中化学 来源: 题型:058
以MgCl2·6H2O为原料制备无水氯化镁。已知:MgCl2·6H2O晶体在空气中加热时,释出部分结晶水,同时生成Mg(OH)Cl或MgO;在干燥HCl气流中加热能制得无水MgCl2。
可选用药品:MgCl2·6H2O晶体、NaCl(固)、KClO3(固)、MnO2、浓H2SO4、浓HCl、稀NaOH溶液。
仪器:如下图所示(装置可重复使用)。回答下列问题:
(1)组装氯化氢气体发生器,应选用的仪器(用编号A、B……填入)是________,有关的化学方程式是________;
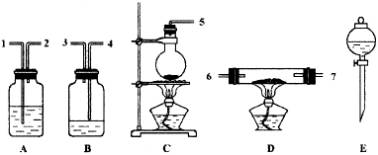
(2)按HCl气流方向,其余装置的连接顺序(用数学1、2……填入)是:
( )→( )( )→( )( )→( )( );
(3)各装置中应放的药品:A________B________C________D________E________;
(4)B装置的作用是________,B中能观察到的现象是________。
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
可选用药品:MgCl2·6H2O晶体、NaCl(固)、KClO3(固)、MnO2、浓H2SO4、浓HCl、稀NaOH溶液。
仪器:如下图所示(装置可重复使用)。回答下列问题:
(1)组装氯化氢气体发生器,应选用的仪器(用编号A、B……填入)是________,有关的化学方程式是________;
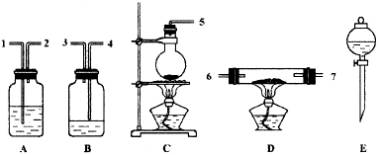
(2)按HCl气流方向,其余装置的连接顺序(用数学1、2……填入)是:
( )→( )( )→( )( )→( )( );
(3)各装置中应放的药品:A________B________C________D________E________;
(4)B装置的作用是________,B中能观察到的现象是________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山西省康杰中学高二第一次月考化学试卷(带解析) 题型:填空题
(14分)高炉炼铁中发生的基本反应之一如下:
FeO(固)+CO(气)  Fe(固)+CO2(气) △H﹤0。已知1100℃时,K=0.263。化学平衡常数只与温度有关,不随浓度和压强的变化而变化。
Fe(固)+CO2(气) △H﹤0。已知1100℃时,K=0.263。化学平衡常数只与温度有关,不随浓度和压强的变化而变化。
(1)其平衡常数可表示为K=_______ ,若温度升高,化学平衡移动后达到新的平衡,平衡常数K值_____(本小题空格填写:增大、减小或不变)
(2)1100℃时,测得高炉中c(CO2)="0.025" mol·L-1,c(CO)=0.1mol·L-1,在这种情况下该反应是否处于化学平衡状态_______ (选填“是”或“否”),此时化学反应速率是 υ正___υ逆(选填大于、小于或等于)其原因是___________。
(3)若平衡时,保持容器容积不变,使容器内压强增大,则平衡_______
A. 一定向正反应方向移动 B. 一定向逆反应方向移动
C. 一定不移动 D. 不一定移动
(4)欲提高CO的平衡转化率,可采取的措施( )
A. 减少Fe B. 增加FeO
C. 移出部分CO2 D. 提高反应的温度
E. 减小容器的体积 F. 加入合适的催化剂
查看答案和解析>>
科目:高中化学 来源:2014届山西省高二第一次月考化学试卷(解析版) 题型:填空题
(14分 )高炉炼铁中发生的基本反应之一如下:
FeO(固)+CO(气)  Fe(固)+CO2(气) △H﹤0。已知1100℃时,K=0.263。化学平衡常数只与温度有关,不随浓度和压强的变化而变化。
Fe(固)+CO2(气) △H﹤0。已知1100℃时,K=0.263。化学平衡常数只与温度有关,不随浓度和压强的变化而变化。
(1) 其平衡常数可表示为K=_______ ,若温度升高,化学平衡移动后达到新的平衡,平衡常数K值_____(本小题空格填写:增大、减小或不变)
(2)1100℃时,测得高炉中c(CO2)=0.025 mol·L-1,c(CO)=0.1mol·L-1,在这种情况下该反应是否处于化学平衡状态_______ (选填“是”或“否”),此时化学反应速率是 υ正___υ逆(选填大于、小于或等于)其原因是___________。
(3)若平衡时,保持容器容积不变,使容器内压强增大,则平衡_______
A. 一定向正反应方向移动 B. 一定向逆反应方向移动
C. 一定不移动 D. 不一定移动
(4)欲提高CO的平衡转化率,可采取的措施( )
A. 减少Fe B. 增加FeO
C. 移出部分CO2 D. 提高反应的温度
E. 减小容器的体积 F. 加入合适的催化剂
查看答案和解析>>
科目:高中化学 来源:同步题 题型:推断题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com