
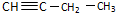 ,而不是
,而不是 的事实是( )
的事实是( )| A. | 燃烧有浓烟 | |
| B. | 能使酸性高锰酸钾溶液褪色 | |
| C. | 所在原子不在同一平面上 | |
| D. | 与足量溴水反应,生成物中只有2个碳原子上有溴原子 |
分析 A.有机物含碳量较高,燃烧会产生浓烟,而二者含碳量相同;
B.二者都是不饱和烃,都能够使高锰酸钾溶液褪色;
C.根据1-丁炔和1,3-丁二烯平面结构进行分析;
D.根据炔烃和二烯烃中含有不饱和碳原子个数分析.
解答 解:A.丁炔和丁二烯含碳量相同,燃烧都有浓烟,不能据此确定结构,故A错误;
B.两者都为不饱和烃,均能使KMnO4溶液褪色,也不能确定,故B错误;
C.1,3-丁二烯的所有原子都在同一平面上,但1-丁炔分子中3,4碳原子上的氢原子不在同一平面上,故C正确;
D.与足量溴水反应,生成物中只有2个碳原子上有溴原子,说明是炔烃,因为溴加成后Br原子只能连在炔烃的两个不饱和碳原子上,而1,3丁二烯会出现在四个碳原子上,故D正确.
故选CD.
点评 本题考查了有机物的结构和性质,为高频考点,题目难度不大,根据炔烃和二烯烃的结构决定化学性质、反应产物分析,试题旨在培养学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力.


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:填空题
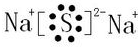 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | R的原子半径在五种原子中最大 | |
| B. | Y的氢化物的稳定性比W的强 | |
| C. | X与Y形成的化合物只有一种 | |
| D. | R的最高价氧化物的水化物的酸性比W的弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
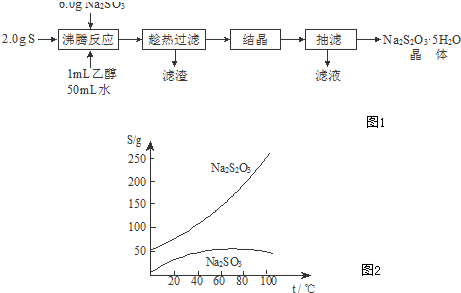
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
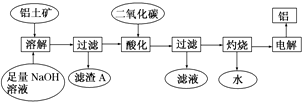
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
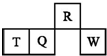 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A. | 最简单气态氢化物的热稳定性:R>Q | |
| B. | 最高价氧化物对应水化物的酸性:Q<W | |
| C. | 原子半径:T>Q>R | |
| D. | T的最高价氧化物对应的水化物不能和强碱反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 单质铜与稀硝酸反应:Cu+2 H++2NO3-═Cu2++2 NO↑+H2O | |
| B. | NaOH溶液与足量的Ca(HCO3)2溶液反应:2HCO3-+2OH-+Ca2+═CaCO3↓+2H2O | |
| C. | 等物质的量的FeBr2和Cl2在溶液中的反应:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| D. | 氨水吸收少量的二氧化硫:2NH3•H2O+SO2═2NH4++SO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com