
| ѡ�� | ʵ�� | ���� | ���� |
| A | ��KI��Һ�м���CCl4������ | Һ��ֲ㣬�²���Ϻ�ɫ | ��������CCl4��������ˮ |
| B | ��ij��Һ�еμ�BaCl2��Һ������ϡ�����ữ | ��Һ�в�����ɫ��������ϡ����ܽ� | ԭ��Һ��һ������SO42- |
| C | ��ϡ�����ữ��H2O2��Һ����Fe��NO3��2��Һ�� | ��Һ���ɫ | �����ԣ�H2O2��Fe3+ǿ |
| D | ���з�̪��Na2CO3��Һ�м�������BaCl2���� | ��Һ��ɫ��dz | ֤��Na2CO3��Һ�д���ˮ��ƽ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
���� A��KI��Һ��CCl4�ֲ㣻
B����ɫ��������ΪAgCl�����ᱵ�������ᱵ��
C��������������������ӿ������������ӣ���������������������ӣ�
D����������BaCl2���壬����̼�ᱵ������ˮ��ƽ�������ƶ���
��� �⣺A��KI��Һ��CCl4�ֲ㣬�²�Ϊ��ɫ���л��㣬�����۾�����������A����
B����ɫ��������ΪAgCl�����ᱵ�������ᱵ���������������ܽ⣬ԭ��Һ���ܺ�SO42-����B����
C��������������������ӿ������������ӣ���������������������ӣ������ж������ԣ����۲���������C����
D����������BaCl2���壬����̼�ᱵ������ˮ��ƽ�������ƶ�����Һ��ɫ��dz����D��ȷ��
��ѡD��
���� ���⿼�黯ѧʵ�鷽�������ۣ�Ϊ��Ƶ���㣬���ջ��������ᴿ�����Ӽ��顢������ԭ��Ӧ������ˮ��Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע��ʵ��������Է�������Ŀ�ѶȲ���


 ������ҵ��ͬ����ϰ��ϵ�д�
������ҵ��ͬ����ϰ��ϵ�д� С��ſ�ʱ��ҵϵ�д�
С��ſ�ʱ��ҵϵ�д� һ������ϵ�д�
һ������ϵ�д� �Ƹ�С״Ԫ���ֳ������ϵ�д�
�Ƹ�С״Ԫ���ֳ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ϊ11.2 L | B�� | Ħ��������32g/mol | ||
| C�� | ����Ϊ64g | D�� | Լ����6.02��1023����ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
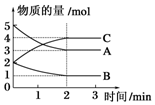 ��2L�̶��ݻ����ܱ������У��ڲ�ͬ��Ӧʱ������ʵ����ʵ����ı仯�����ͼ��ʾ��
��2L�̶��ݻ����ܱ������У��ڲ�ͬ��Ӧʱ������ʵ����ʵ����ı仯�����ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ͼ��������ϩ�������Ʊ���ȩͬʱ�ܻ�õ��ܵ�һ��װ�ã������ܷ�ӦΪ2CH2=CH2+O2��2CH3CHO������˵��������ǣ�������
��ͼ��������ϩ�������Ʊ���ȩͬʱ�ܻ�õ��ܵ�һ��װ�ã������ܷ�ӦΪ2CH2=CH2+O2��2CH3CHO������˵��������ǣ�������| A�� | �õ�ؿɽ���ѧ��ת��Ϊ���� | |
| B�� | ÿ��0.1 molol O2��Ӧ������Һ��Ǩ��0.4 mol e- | |
| C�� | ������ӦʽΪCH2=CH2-2e-+H2O=CH3CHO+2H+ | |
| D�� | ��������Һ��pH���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£�11.2 L���������ķ�����ΪNA | |
| B�� | 1.8 g ��NH4+�к��еĵ�����Ϊ1.1NA | |
| C�� | 22g������̼���״����11.2LH2������ͬ��ԭ���� | |
| D�� | 2.3 g��������O2��ȫ��Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ0.1mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| �ɷ� | Cl- | ����HCl | Fe2+ | Fe3+ |
| ����g•/L-1 | 130-160 | 50-70 | 60-80 | 0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
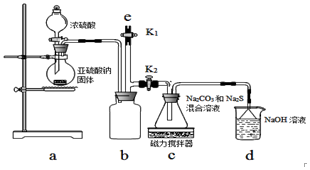 �軯����һ����Ҫ�Ļ�������ԭ�ϣ�й©ʱ�ᵼ�»�����Ⱦ������ͨ������˫��ˮ�������������Һ��������
�軯����һ����Ҫ�Ļ�������ԭ�ϣ�й©ʱ�ᵼ�»�����Ⱦ������ͨ������˫��ˮ�������������Һ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 18.4 mol/L��Ũ�������������ˮ���������Һ�����ʵ���Ũ�ȴ���9.2 mol/L | |
| B�� | �����£�1LpH=13��NaOH��Һ�У���ˮ�����OH-������ĿΪ0.1NA | |
| C�� | 50 mL 14.0 mol•L-1Ũ����������ͭ��Ӧ��ת�Ƶĵ�����Ϊ0.35 NA | |
| D�� | ͬ��ͬѹͬ����µ���������12C18O��14N2���еĵ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol Na������O2��Ӧ������Na2O��Na2O2�Ļ�����ת��NA������ | |
| B�� | ��״���£�5.6 Lһ��������5.6 L������Ϻ�ķ�������Ϊ0.5NA | |
| C�� | ��״���£�11.2 L HF����0.5 NA��HF���� | |
| D�� | 500mL 12mol��L-1������������ MnO2���ȳ�ַ�Ӧ������Cl2 ������Ŀ1.5 NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com