


①向甲中通入干燥的Cl2之前,需先通人一段时间CO2,目的是_________________。
②实验过程中,应控制__________,以减少PCl5的生成。
③蒸馏烧瓶乙中得到的粗产品含有POCl3、PCl5等。加入黄磷加热除去 PCl5后,通过___________(填实验操作名称),即可得到PCl3纯品。
(2)已知:
a. H3PO3+H2O+I2 H3PO4+2HI
H3PO4+2HI
b. (NH4)3BO3溶液可与HI和H3PO4反应生成H3BO3
c. Na2S2O3溶液可定量测定碘:I2+2Na2S2O3=Na2S4O6+2NaI
①测定产品中PCl3质量分数的实验如下,请补充相应的实验步骤:
步骤1:迅速移取mg产品,水解完全后在500 mL容量瓶中定容;
步骤2:从容量瓶中移取25.00 mL溶液置于碘量瓶中;
步骤3:准确加入c1 mol/L碘溶液V1mL(过量),再________________;
步骤4:_____________;滴至终点时消耗c2 mol/L Na2S2O3溶液V2mL;
②根据上述数据,该产品中PCl3的质量分数为____________(用含字母的代数式表示)。
 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:阅读理解
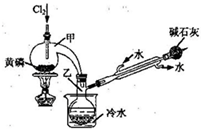 (2011?南京二模)PCl3可用于半导体生产的外延、扩散工序.有关物质的部分性质如下:
(2011?南京二模)PCl3可用于半导体生产的外延、扩散工序.有关物质的部分性质如下:| 熔点/℃ | 沸点/℃℃℃ | 密度/g?cm-3 | 其他 | |||||||||
| 黄磷 | 44.1 | 280.5 | 1.82 | 2P(过量)+3Cl2
| ||||||||
| PCl3 | -112 | 75.5 | 1.574 | 遇水生成H3PO3和HCl,遇O2生成POCl3 | ||||||||
| POCl3 | 2 | 105 3 | 1.675 | 遇水生成H3PO4和HCl,能溶于PCl3 |
2.75(c1v1-
| ||
| m |
2.75(c1v1-
| ||
| m |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 熔点/℃ | 沸点/℃ | 密度/g?mL | 其他 | |||||||||
| 黄磷 | 44.1 | 280.5 | 1.82 | 2P(过量)+3Cl2
2P+5Cl2(过量)
| ||||||||
| PCl3 | -112 | 75.5 | 1.574 | 遇水生成H3PO3和HCl,遇O2生成POCl3 | ||||||||
| POCl3 | 2 | 105.3 | 1.675 | 遇水生成H3PO4和HCl,能溶于 PCl3 |
| ||
| ||
(c1V1-
| ||
| m |
(c1V1-
| ||
| m |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖南省株洲市高三第四次月考化学试卷(解析版) 题型:实验题
PCl3可用于半导体生产的外延、扩散工序。有关物质的部分性质如下:
|
|
熔点/℃ |
沸点/℃ |
密度/g·mL-1 |
其他 |
|
黄磷 |
44.1 |
280.5 |
1.82 |
2P(过量)+3Cl2 |
|
PCl3 |
-112 |
75.5 |
1.574 |
遇水生成H3PO3和HCl,遇O2生成POCl3 |
|
POCl3 |
2 |
105.3 |
1.675 |
遇水生成H3PO4和HCl,能溶于PCl3 |
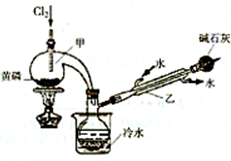
如图是实验室制备PCl3的装置(部分仪器已省略)。
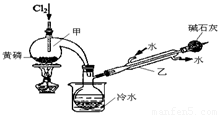
(1)向甲中通入干燥的Cl2之前,需先通入一段时间CO2,目的是 。
(2)实验过程中,应控制 ,以减少PCl5的生成。
(3)粗产品品中常含有POCl3、PCl5等。加入黄磷加热除去PCl5后,通过 (填实验操作名称),即可得到PCl3的纯品。
(4)已知:a.H3PO3+H2O+I2
 H3PO4+2HI;b.(NH4)3BO3溶液可与HI和H3PO4反应生成H3BO3(弱酸);c.Na2S2O3溶液可定量测定碘:I2+2Na2S2O3→Na2S4O6+2NaI
H3PO4+2HI;b.(NH4)3BO3溶液可与HI和H3PO4反应生成H3BO3(弱酸);c.Na2S2O3溶液可定量测定碘:I2+2Na2S2O3→Na2S4O6+2NaI
①测定产品中PCl3质量分数的实验如下,请补充相应的实验步骤:
步骤1:迅速移取m g产品,水解完全后在500mL容量瓶中定容。
步骤2:从容量瓶中移取25.00mL溶液置于锥形瓶中。
步骤3:准确加入c1 mol/L碘溶液V1 mL(过量),再 。
步骤4:用标准Na2S2O3溶液回滴过量的碘,将近终点时加入3 mL淀粉溶液,继续滴至终点(蓝色溶液褪色);滴至终点时消耗c2 mol/L Na2S2O3溶液V2 mL。
②根据上述数据,该产品中PCl3的质量分数为 (用含字母的代数式表示)。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖南省株洲市高三第四次月考化学试卷(解析版) 题型:实验题
PCl3可用于半导体生产的外延、扩散工序。有关物质的部分性质如下:
|
|
熔点/℃ |
沸点/℃ |
密度/g·mL-1 |
其他 |
|
黄磷 |
44.1 |
280.5 |
1.82 |
2P(过量)+3Cl2 |
|
PCl3 |
-112 |
75.5 |
1.574 |
遇水生成H3PO3和HCl,遇O2生成POCl3 |
|
POCl3 |
2 |
105.3 |
1.675 |
遇水生成H3PO4和HCl,能溶于PCl3 |
如图是实验室制备PCl3的装置(部分仪器已省略)。
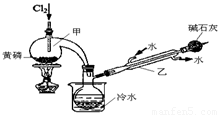
(1)向甲中通入干燥的Cl2之前,需先通入一段时间CO2,目的是 。
(2)实验过程中,应控制 ,以减少PCl5的生成。
(3)粗产品品中常含有POCl3、PCl5等。加入黄磷加热除去PCl5后,通过 (填实验操作名称),即可得到PCl3的纯品。
(4)已知:a.H3PO3+H2O+I2
 H3PO4+2HI;b.(NH4)3BO3溶液可与HI和H3PO4反应生成H3BO3(弱酸);c.Na2S2O3溶液可定量测定碘:I2+2Na2S2O3→Na2S4O6+2NaI
H3PO4+2HI;b.(NH4)3BO3溶液可与HI和H3PO4反应生成H3BO3(弱酸);c.Na2S2O3溶液可定量测定碘:I2+2Na2S2O3→Na2S4O6+2NaI
①测定产品中PCl3质量分数的实验如下,请补充相应的实验步骤:
步骤1:迅速移取m g产品,水解完全后在500mL容量瓶中定容。
步骤2:从容量瓶中移取25.00mL溶液置于锥形瓶中。
步骤3:准确加入c1 mol/L碘溶液V1 mL(过量),再 。
步骤4:用标准Na2S2O3溶液回滴过量的碘,将近终点时加入3 mL淀粉溶液,继续滴至终点(蓝色溶液褪色);滴至终点时消耗c2 mol/L Na2S2O3溶液V2 mL。
②根据上述数据,该产品中PCl3的质量分数为 (用含字母的代数式表示)。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖南省株洲市高三第四次月考化学试卷(解析版) 题型:实验题
PCl3可用于半导体生产的外延、扩散工序。有关物质的部分性质如下:
|
|
熔点/℃ |
沸点/℃ |
密度/g·mL-1 |
其他 |
|
黄磷 |
44.1 |
280.5 |
1.82 |
2P(过量)+3Cl2 |
|
PCl3 |
-112 |
75.5 |
1.574 |
遇水生成H3PO3和HCl,遇O2生成POCl3 |
|
POCl3 |
2 |
105.3 |
1.675 |
遇水生成H3PO4和HCl,能溶于PCl3 |
如图是实验室制备PCl3的装置(部分仪器已省略)。

(1)向甲中通入干燥的Cl2之前,需先通入一段时间CO2,目的是 。
(2)实验过程中,应控制 ,以减少PCl5的生成。
(3)粗产品品中常含有POCl3、PCl5等。加入黄磷加热除去PCl5后,通过 (填实验操作名称),即可得到PCl3的纯品。
(4)已知:a.H3PO3+H2O+I2
 H3PO4+2HI;b.(NH4)3BO3溶液可与HI和H3PO4反应生成H3BO3(弱酸);c.Na2S2O3溶液可定量测定碘:I2+2Na2S2O3→Na2S4O6+2NaI
H3PO4+2HI;b.(NH4)3BO3溶液可与HI和H3PO4反应生成H3BO3(弱酸);c.Na2S2O3溶液可定量测定碘:I2+2Na2S2O3→Na2S4O6+2NaI
①测定产品中PCl3质量分数的实验如下,请补充相应的实验步骤:
步骤1:迅速移取m g产品,水解完全后在500mL容量瓶中定容。
步骤2:从容量瓶中移取25.00mL溶液置于锥形瓶中。
步骤3:准确加入c1 mol/L碘溶液V1 mL(过量),再 。
步骤4:用标准Na2S2O3溶液回滴过量的碘,将近终点时加入3 mL淀粉溶液,继续滴至终点(蓝色溶液褪色);滴至终点时消耗c2 mol/L Na2S2O3溶液V2 mL。
②根据上述数据,该产品中PCl3的质量分数为 (用含字母的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com