
| A. | 原子序数为34 | |
| B. | 最高价氧化物的水化物的分子式为:H2SeO4 | |
| C. | Se的非金属性比Br强 | |
| D. | 气态氢化物的稳定性比硫化氢气体弱 |
分析 A.Se与硫元素同族,与氪同周期;
B.Se元素最高正价为+6价,和S属于同一主族,根据S元素确定其最高价氧化物的水化物化学式;
C.同一周期元素,元素的非金属性随着原子序数增大而增强;
D.元素的非金属性越强,其气态氢化物的还原性越弱.
解答 解:A.Se与硫元素同族,与氪同周期,则原子序数为36-2=34,故A正确;
B.Se元素最高正价为+6价,和S属于同一主族,根据S元素确定其最高价氧化物的水化物化学式为H2SeO4,故B正确;
C.同一周期元素,元素的非金属性随着原子序数增大而增强,Br和Se属于同一周期元素,且原子序数Br>Se,所以Br的非金属性比Se强,故C错误;
D.元素的非金属性越强,其气态氢化物的还原性越弱,非金属性S>Se,所以气态氢化物的稳定性比硫化氢气体弱,故D正确;
故选C.
点评 本题考查元素周期表和元素周期律,明确元素的位置和性质的关系及同主族性质变化规律即可解答,难度不大.


 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
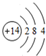 ,丙的电子式为
,丙的电子式为 ;E在周期表中的位置为第三周期VA族;
;E在周期表中的位置为第三周期VA族;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大.第二周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层P轨道的电子为半充满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请回答下列问题:
A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大.第二周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层P轨道的电子为半充满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最高价氧化物对应水化物碱性强弱:A>C | |
| B. | D、E是铝土矿的主要成分 | |
| C. | B、E的最高价氧化物具有相似的物理性质和化学性质 | |
| D. | B、C、D、E的氧化物都是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a-c=m-n | B. | a-b=n-m | C. | c-d=m+n | D. | b-d=m+n |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | W的离子半径>Y的离子半径 | |
| B. | Z的氢化物稳定性<W的氢化物稳定性 | |
| C. | Y的氧化物既能与盐酸,又能与NaOH溶液反应 | |
| D. | X2W2、Y2W3两种化合物含有的化学键类型完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol苯分子中所含的C=C键数为3NA | |
| B. | 60gSiO2中含有Si-O键的个数为2NA | |
| C. | 0.1molCnH2n+2中含有的碳碳单键数为0.1nNA | |
| D. | 18 g冰中含氢键的个数为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com