
| A. | ①⑥ | B. | ①②③④⑥ | C. | ①②③⑥ | D. | ①②③④ |
分析 玻璃中含有二氧化硅,只要能和二氧化硅反应的药品不能盛放在带有玻璃塞的试剂瓶中,据此分析解答.
解答 解:①NaOH与二氧化硅反应生成粘性的硅酸钠,导致玻璃塞和试剂瓶粘结在一起而打不开,所以氢氧化钠溶液需放在带橡胶塞的玻璃试剂瓶中;
②Na2SiO3溶液由于弱酸阴离子水解导致溶液显示碱性,可以和玻璃的成分二氧化硅之间反应,所以盛放Na2SiO3等溶液的试剂瓶应用橡皮塞;
③Na2S水解显碱性,与二氧化硅反应,所以Na2S需放在带橡胶塞的玻璃试剂瓶中;
④Na2CO3水解显碱性,与二氧化硅反应硅酸钠和水,所以Na2CO3需放在带橡胶塞的玻璃试剂瓶中;
⑤NH4Cl溶液弱碱阳离子水解导致溶液显示酸性,酸性溶液与玻璃成分不反应,可以存放在玻璃塞的试剂瓶中;
⑥石灰水与二氧化硅反应硅酸钙和水,所以石灰水需放在带橡胶塞的玻璃试剂瓶中;
⑦浓H2SO4溶液显示酸性,酸性溶液与玻璃成分不反应,可以存放在玻璃塞的试剂瓶中.
故选B.
点评 本题主要考查的是试剂的存放以及盐类水解原理的应用,属于中等难度的题目,注意总结.


科目:高中化学 来源: 题型:解答题
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热才发生的化学反应,反应物的总能量可能高于生成物的总能量 | |
| B. | 已知:H2(g)+F2(g)═2HF(g)△H=-270 kJ•mol-1,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ | |
| C. | 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)═2NH3(g)△H=-38.6 kJ•mol-1 | |
| D. | 已知:C(s,金刚石)═C(s,石墨)△H=-1.5 kJ•mol-1,说明金刚石更稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可 | |
| B. | 可用蘸有浓盐酸的棉棒检验输送氨气的管道是否漏气 | |
| C. | 碘是人体必需的微量元素,所以要多吃富含高碘酸的食物 | |
| D. | 提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓溶液再冷却结晶、过滤、干燥的方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某学生在如图所示装置中用苯和液溴制取溴苯,请根据下列实验步骤完成有关问题:
某学生在如图所示装置中用苯和液溴制取溴苯,请根据下列实验步骤完成有关问题: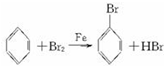 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 空气中PM2.5(2.5微米以下的颗粒物)的存在能够形成丁达尔效应 | |
| B. | 煤燃烧时加入少量的生石灰可以减少废气中的二氧化硫排放 | |
| C. | 将造纸废水通过高压水井压到地下,节约生产成本 | |
| D. | 绿色化学的核心是应用呼吸原理对环境污染进行治理 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Na2SiO3溶液中通入过量SO2:SiO32-+SO2+H2O═H2SiO3↓+SO32- | |
| B. | 碳酸氢镁溶液中加入过量石灰水:Mg2++2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+MgCO3↓ | |
| C. | 往FeCl3溶液中通入H2S气体:2Fe3++H2S═2Fe2++S↓+2H+ | |
| D. | 大苏打溶液中加入稀硫酸:S2O32-+2SO42-+6H+═4 SO2↑+3H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com