
【题目】“花卉保鲜剂”是一种可以延长花期的试剂。如表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
成分 | 质量(g) | 摩尔质量(gmol1) |
蔗糖 | 25.00 | 342 |
硫酸钾 | 0.87 | 174 |
阿司匹林 | 0.17 | 180 |
高锰酸钾 | 0.316 | 158 |
硝酸银 | 0.0075 | 170 |
(1)下列“花卉保鲜剂”的成分中,属于非电解质的是______,可做杀菌剂的是____
A. 高锰酸钾B. 硫酸钾C. 蔗糖D. 硝酸银E. 水
(2) 配制1L上述“鲜花保鲜剂”需要高锰酸钾______mol。
(3)在溶液配制过程中,下列操作会使配制结果无影响的是______。
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚配制完一定物质的量浓度的氯化钠溶液未洗涤
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(4)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为______mol/L。
(5)如果用高铁酸钾(K2FeO4)代替高锰酸钾效果会更好,湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O.碱性条件下,氧化剂与还原剂的物质的量的比为3:2发生反应,写出并配平湿法制备高铁酸钾的离子反应方程式___________________________________________________________
【答案】C A 0.004 BD 0.024 4OH-+3ClO-+2Fe(OH)3=3Cl-+2FeO42-+5H2O
【解析】
(1)A. 高锰酸钾,电解质,可杀菌消毒;
B. 硫酸钾,电解质,不用于杀菌消毒;
C. 蔗糖,非电解质,不用于杀菌消毒;
D. 硝酸银,电解质,不用于杀菌消毒;
E. 水,电解质,不能杀菌消毒。
(2) 在500mL上述“鲜花保鲜剂”中,高锰酸钾用量为0.316g,物质的量为![]() ,由此可求出配制1L此溶液需要高锰酸钾的物质的量。
,由此可求出配制1L此溶液需要高锰酸钾的物质的量。
(3)A.定容时俯视容量瓶刻度线,溶液体积偏小;
B.容量瓶在使用前未干燥,里面有少量蒸馏水,不影响溶质的物质的量和溶液的体积;
C.容量瓶在使用前刚配制完一定物质的量浓度的氯化钠溶液未洗涤,溶质的物质的量增大;
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理,不影响溶液的体积。
(4)“鲜花保鲜剂”中K+来自硫酸钾和高锰酸钾,由此可求出物质的量浓度。
(5)K2FeO4是生成物,则Fe(OH)3为反应物,由价态变化,确定其为还原剂;ClO-为氧化剂,其产物为Cl-,再由氧化剂与还原剂的物质的量的比为3:2,可得出湿法制备高铁酸钾的离子反应方程式。
(1)A. 高锰酸钾,电解质,可杀菌消毒;
B. 硫酸钾,电解质,不用于杀菌消毒;
C. 蔗糖,非电解质,不用于杀菌消毒;
D. 硝酸银,电解质,不用于杀菌消毒;
E. 水,电解质,不能杀菌消毒。
由经上分析可知,属于非电解质的是C,可做杀菌剂的是A。答案为:C;A;
(2) 在500mL上述“鲜花保鲜剂”中,高锰酸钾用量为0.316g,物质的量为![]() ,由此可求出配制1L此溶液需要高锰酸钾的物质的量0.002mol×2=0.004mol。答案为:0.004;
,由此可求出配制1L此溶液需要高锰酸钾的物质的量0.002mol×2=0.004mol。答案为:0.004;
(3)A.定容时俯视容量瓶刻度线,溶液体积偏小,使配制结果偏高;
B.容量瓶在使用前未干燥,里面有少量蒸馏水,不影响溶质的物质的量和溶液的体积,不影响配制结果;
C.容量瓶在使用前刚配制完一定物质的量浓度的氯化钠溶液未洗涤,溶质的物质的量增大,使配制结果偏高;
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理,不影响溶液的体积,不影响配制结果。故BD符合题意。答案为:BD;
(4)“鲜花保鲜剂”中K+来自硫酸钾和高锰酸钾,由此可求出物质的量浓度 。答案为:0.024;
。答案为:0.024;
(5)K2FeO4是生成物,则Fe(OH)3为反应物,由价态变化,确定其为还原剂;ClO-为氧化剂,其产物为Cl-,再由氧化剂与还原剂的物质的量的比为3:2,利用电子守恒、电荷守恒及质量守恒,可得出湿法制备高铁酸钾的离子反应方程式4OH-+3ClO-+2Fe(OH)3=3Cl-+2FeO42-+5H2O。答案为:4OH-+3ClO-+2Fe(OH)3=3Cl-+2FeO42-+5H2O。


 互动英语系列答案
互动英语系列答案科目:高中化学 来源: 题型:
【题目】根据所学知识,回答下列问题:
(1)高铁酸钠(Na2FeO4)可作为高效、多功能水处理剂,其摩尔质量是__________。高铁酸钠可与水反应生成Fe(OH)3胶体、氢氧化钠和氧气,写出相应的离子方程式:_____________。
(2)戴维通过电解法首先制得了金属钠,随后几十年内,工业上采用铁粉和氢氧化钠高温熔融的方法制得钠蒸气,同时获得Fe3O4和氢气。写出该反应的化学方程式_____________,该反应中属于电解质但不属于氧化物的物质是________________(填化学式),若制得22.4L(折算为标准状况下)钠蒸气,转移电子的数目为________________。
(3)漂白粉常用于饮水、污水、排泄物及被污染的环境消毒,其主要成分是氯化钙和次氯酸钙[Ca(ClO)2],有效成分为次氯酸钙。为测得某漂白粉的有效成分含量,称取A g漂白粉样品溶解,往所得溶液中通入CO2至不再产生沉淀为止,反应的化学方程式为Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,若反应生成次氯酸(HClO)的物质的量为Kmol,则该漂白粉中有效成分的质量分数为___________%(用含A、K的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化镓(![]() )材料具有低的热产生率和高的击穿电场,是制造大功率和高频微波电子器件的理想半导体材料。
)材料具有低的热产生率和高的击穿电场,是制造大功率和高频微波电子器件的理想半导体材料。
已知:①Ga和Al同主族且相邻,化学性质与铝相似;②在室温下,氮化镓不溶于水,硬度高,熔点高,能与热的碱溶液缓慢反应。
(1)配平氮化镓制备的化学方程式:□Ga(l)+□NH3(g)□GaN(s)+□H2(g)+QkJ(Q>0)_____________
(2)上述反应的平衡常数表达式K=_____________;在恒温恒容密闭容器中制备氮化镓,下列有关说法正确的是_____________
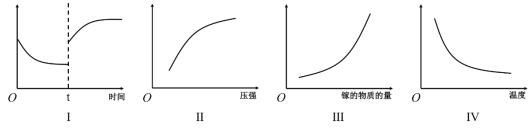
A.Ⅰ图像中如果纵坐标为正反应速率,则t时刻改变的条件可能是加压
B.Ⅱ图像中纵坐标可以为镓的转化率
C.Ⅲ图像中纵坐标可以为化学反应速率
D.Ⅳ图像中纵坐标可以为平衡常数
(3)Ga最外层电子的核外电子排布式___________________,N核外能量最高的电子亚层上电子云空间伸展方向有_____________种;
(4)氮化镓的晶体类型_____________,氮化铝和氮化镓晶体类型相同,且结构相似,比较两者熔点的高低并解释原因_____________________________________________________________;
(5)写出氮化镓溶于热的NaOH溶液的离子方程式____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铂基催化剂表面的氧化还原反应(ORR)是燃料电池最重要的阴极反应。厦门大学李剑锋课题组模拟研究了在酸性条件下铂单晶表面的反应路径如图所示,其中吸附在铂基催化剂表面上的物种用*标注。下列说法正确的是( )
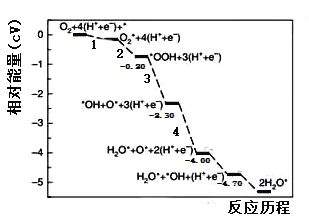
A.②为氧氧双键的断裂过程
B.过程③断裂非极性键,过程⑤形成非极性键
C.该历程的总反应式为O2+4H++4e-=2H2O
D.若在碱性条件下,铂单晶表面的ORR过程及产物均不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用铂丝按如图进行氨的催化氧化实验,下列说法正确的是( )
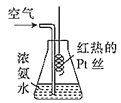
A.通入空气的目的是让氨挥发出来,从而使氧气和氨充分混合
B.瓶口出现少量红棕色气体,说明氨催化氧化的产物是NO2
C.瓶内有白烟出现是由于生成了白色晶体NH4NO3
D.铂丝保持红热说明该反应的ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在固定容积的密闭容器中,可逆反应:mA(s)+nB(g) ![]() pC(g)+qD(g),当m、n、p、q为任意正整数时,下列状态:①体系的压强不再发生变化,②体系的密度不再发生变化,③各组分的物质的量浓度不再改变,④各组分的质量分数不再改变,⑤反应速率vB∶vC∶vD=n∶p∶q,其中,能说明反应已达到平衡的是 ( )
pC(g)+qD(g),当m、n、p、q为任意正整数时,下列状态:①体系的压强不再发生变化,②体系的密度不再发生变化,③各组分的物质的量浓度不再改变,④各组分的质量分数不再改变,⑤反应速率vB∶vC∶vD=n∶p∶q,其中,能说明反应已达到平衡的是 ( )
A. 只有③④B. 只有②③④C. 只有①②③④D. ①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.1mol·L-1的NaOH溶液分别滴定20mL、浓度均为0.1mol·L-1的HCl溶液和HCOOH溶液,溶液中由水电离出的氢离子浓度的对数[1gc(H+)水]随加入NaOH溶液体积的变化如图所示(忽略溶液体积变化),下列说法正确的是( )
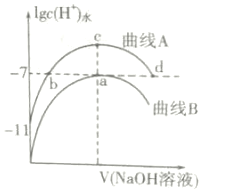
A.该温度下HCOOH的电离常数为Ka=1×10-5
B.a、c两点对应溶液同时升高相同温度,![]() 增大
增大
C.在c点溶液中有:c(HCOO-)+c(HCOOH)=0.1mol·L-1
D.在a、b、c、d四点中对应的溶液呈中性的为a、b、d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应mA(固)+nB(气)![]() pC(气)+qD(气),反应过程中其它条件不变时C的百分含量C%与温度(T)和压强(P)的关系如图所示,下列叙述中正确的是
pC(气)+qD(气),反应过程中其它条件不变时C的百分含量C%与温度(T)和压强(P)的关系如图所示,下列叙述中正确的是
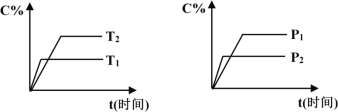
A. 达到平衡后,使用催化剂,C%将增大
B. 达到平衡后,若升高温度、化学平衡向逆反应方向移动
C. 方程式中n>p+q
D. 达到平衡后,增加A的量有利于化学平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH= +49.0kJ/mol
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(g) ΔH= -192.9kJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH= -192.9kJ/mol
由上述方程式可知:CH3OH的燃烧热____(填“大于”“等于”或“小于”)192.9kJ/mol。已知水的气化热为44kJ/mol。则表示氢气燃烧热的热化学方程式为___。
(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH= -159.5kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH= +116.5kJ/mol
③H2O(l)=H2O(g) ΔH= +44.0kJ/mol
写出CO2与NH3合成尿素和液态水的热化学反应方程式___。
(3)已知:①Fe(s)+![]() O2(g)=FeO(s) ΔH1= -272.0kJ/mol
O2(g)=FeO(s) ΔH1= -272.0kJ/mol
②2Al(s)+![]() O2(g)=Al2O3(s) ΔH2= -1675.7kJ/mol
O2(g)=Al2O3(s) ΔH2= -1675.7kJ/mol
Al和FeO发生铝热反应的热化学方程式是___。铝热反应的反应类型___,某同学认为,铝热反应可用于工业炼铁,你的判断是____(填“能”或“不能”),你的理由____。
(4)再生装置中产生的CO2和H2在一定条件下反应生成甲醇等产物,工业上利用该反应合成甲醇。已知:25℃、101KPa下:
①H2(g)+![]() O2(g)=H2O(g) ΔH1= -242kJ/mol
O2(g)=H2O(g) ΔH1= -242kJ/mol
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(g) ΔH2= -676kJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH2= -676kJ/mol
写出CO2和H2生成气态甲醇等产物的热化学方程式____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com