
| I1/kJ•mol-1 | I2/kJ•mol-1 | I3/kJ•mol-1 | I4/kJ•mol-1 | I5/kJ•mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
分析 (1)①Ti为22号元素,原子核外有22个电子,失去3个电子形成Ti3+,基态Ti3+的核外电子排布式为1s22s22p63s23p63d1;
②计算B原子价层电子对确定杂化方式;
(2)①电子层结构相同的离子,其离子半径随着核电荷数的增大而减小;
②M元素的第三电离能剧增,则该元素原子最外层有2个电子,由于存在第五电离能,故其核外电子数大于4,故M为Mg.
解答 解:(1)①Ti为22号元素,原子核外有22个电子,失去3个电子形成Ti3+,基态Ti3+的核外电子排布式为1s22s22p63s23p63d1,基态Ti3+中含有的电子数为19,电子占据的最高能级是3d,该能级具有的原子轨道数为5,故答案为:19;3d;5;
②BH4-中B原子价层电子数=4+$\frac{3+1-1×4}{2}$=4,且不含孤电子对,B原子采取sp3杂化,故答案为:sp3杂化;
(2)①Li+和H-的电子层结构相同,锂元素的核电荷数大于氢元素,所以离子半径Li+<H-,故答案为:<;
②M元素的第三电离能剧增,则该元素原子最外层有2个电子,由于存在第五电离能,故其核外电子数大于4,故M为Mg,则该氢化物化学式为MgH2,故答案为:MgH2.
点评 本题是对物质结构的考查,涉及核外电子排布、杂化方式、微粒半径比较、电离能,难度不大,注意理解电离能与原子结构、化合价关系.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
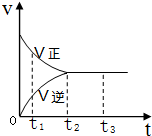 在一密闭容器中放入1mol X,进行可逆反应2X(g)?3Y(g),反应过程中的反应速率(v)与时间(t)的变化关系如图所示,下列叙述正确的是( )
在一密闭容器中放入1mol X,进行可逆反应2X(g)?3Y(g),反应过程中的反应速率(v)与时间(t)的变化关系如图所示,下列叙述正确的是( )| A. | t1时,只有正反应在进行 | |
| B. | t2~t3时间段,反应停止 | |
| C. | t2时,容器内有1.5mol Y | |
| D. | t2~t3时间段,X,Y的物质的量均没有发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2与C2H4 | B. | CO与C2H4 | C. | H2与C4H6 | D. | CO 与C3H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 键能 | 键能 | 键能 | 键能 | ||||
| H-H | 436 | Cl-Cl | 243 | H-Cl | 432 | H-O | 464 |
| S=S | 255 | H-S | 339 | H-F | 565 | C-O | 347 |
| C-Cl | 330 | C-I | 218 | C-F | 427 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 固体氯化钠溶于水 | B. | 氯化氢溶于水 | ||
| C. | 冰经加热变成水蒸气 | D. | 氯化铵受热分解生成氯化氢和氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
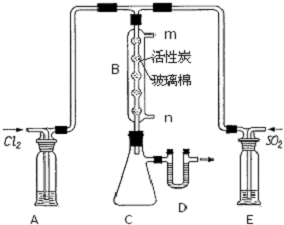 磺酰氯(SO2Cl2)是一种有机氯化物,也是锂电池正极活性物质.已知磺酰氯是一种无色液体,熔点-54.1℃,沸点69.1℃,遇水发生剧烈水解,且产生白雾.
磺酰氯(SO2Cl2)是一种有机氯化物,也是锂电池正极活性物质.已知磺酰氯是一种无色液体,熔点-54.1℃,沸点69.1℃,遇水发生剧烈水解,且产生白雾.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com