
分析 根据是否发生化学反应判断化学键是否被破坏,根据物质中存在的化学键判断破坏的化学键类型,分子晶体中存在分子间作用力和共价键,离子晶体中存在离子键,可能有共价键,据此分析.
解答 解:①碘的升华属于物理变化,只是状态发生变化,没有化学键的破坏;
②氧气溶于水,属于物理变化,没有化学键的破坏;
③氯化钠溶于水,在水分子的作用下,氯化钠中的离子键被破坏,所以破坏的是离子键;
④烧碱熔化中存在离子键,融化烧碱时,阴阳离子间的化学键被破坏,所以破坏的是离子键;
⑤氯化氢溶于水,在水分子的作用下,氯化氢中的共价键被破坏,所以破坏的是共价键;
⑥氯化铵受热分解,氯化铵是离子化合物,存在的化学键有离子键、共价键,受热分解时,阴阳离子间的化学键、及铵根离子中的共价键被破坏,所以所以破坏的是离子键、共价键;
故答案为:①②;③④;⑤;⑥.
点评 本题考查了离子键、共价键的区别,侧重考查学生对概念的辨别能力,离子化合物中可能含有共价键,如:KOH,共价化合物中一定不含离子键,配位键属于共价键,但氢键不属于化学键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 2 mol SO2与1 mol O2能完全反应生成2 mol SO3,升高温度可以加快此反应的化学反应速率 | |
| B. | 2 mol SO2与1 mol O2不能完全反应生成2 mol SO3,升高温度可以加快此反应的化学反应速率 | |
| C. | 2 mol SO2与1 mol O2能完全反应生成2 mol SO3,升高温度减慢此反应的化学反应速率 | |
| D. | 2 mol SO2与1 mol O2不能完全反应生成2 mol SO3,升高温度减慢此反应的化学反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 白磷与氧气可发生如下反应:P4+5O2═P4O10.已知断裂下列1mol化学键需要吸收的能量分别为:P-P a kJ、P-O b kJ、P=O c kJ、O=O d kJ.根据下图所示的分子结构和有关数据估算1mol P4发生该反应放出的热量是( )
白磷与氧气可发生如下反应:P4+5O2═P4O10.已知断裂下列1mol化学键需要吸收的能量分别为:P-P a kJ、P-O b kJ、P=O c kJ、O=O d kJ.根据下图所示的分子结构和有关数据估算1mol P4发生该反应放出的热量是( )| A. | (6a+5d-4c-12b) kJ | B. | (4c+12b-6a-5d) kJ | C. | (4c+12b-4a-5d) kJ | D. | (5a+5d-4c-12b) kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
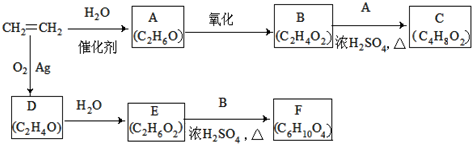
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{53}^{131}$I的化学性质与${\;}_{53}^{127}$I相同 | |
| B. | ${\;}_{53}^{131}$I的原子序数为53 | |
| C. | ${\;}_{53}^{131}$I的原子核外电子数为78 | |
| D. | ${\;}_{53}^{131}$I的原子核内中子数多于质子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
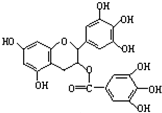 绿茶中含有物质EGCG具有抗癌作用,能使癌细胞自杀性死亡其结构见图.下列有关EGCG的说法中正确的是( )
绿茶中含有物质EGCG具有抗癌作用,能使癌细胞自杀性死亡其结构见图.下列有关EGCG的说法中正确的是( )| A. | EGCG易被氧化 | |
| B. | EGCG的分子中有1个手性碳原子 | |
| C. | 1mol EGCG与浓溴水发生取代反应时最多消耗6molBr2 | |
| D. | 1mol EGCG与氢氧化钠溶液反应最多消耗10molNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 每生成2mol SO2的同时,消耗2molSO3 | |
| B. | 混合气体的总质量不再变化 | |
| C. | 每生成2mol SO3的同时,消耗1molSO2 | |
| D. | 混合气体的压强不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com