
【题目】在一密闭容器中有HCHO、H2、O2 混合气体共20g和足量的Na2O2,用电火花引燃,使其完全反应,Na2O2增重8g,则原混合气体中O2的质量分数是()
A. 40% B. 33% C. 60% D. 36%
科目:高中化学 来源: 题型:
【题目】常温时,Ksp[Mg(OH)2]=1.1×10﹣11 , Ksp(AgCl)=1.8×10﹣10 , Ksp(Ag2CrO4)=1.9×10﹣12Ksp(CH3COOAg)=2.3×10﹣3 , 下列叙述不正确的是( )
A.浓度均为0.2 molL﹣1的AgNO3溶液和CH3COONa溶液等体积混合一定产生CH3COOAg沉淀
B.将0.001 molL﹣1的AgNO3溶液滴入0.001 molL﹣1的KCl和0.001 molL﹣1的K2CrO4的混合溶液中,先产生Ag2CrO4沉淀
C.c(Mg2+)为0.11 molL﹣1的溶液中要产生Mg(OH)2沉淀,溶液的pH要控制在9以上
D.在其他条件不变的情况下,向饱和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一定物质的量浓度的NaOH溶液100mL,然后向其通入一定量的CO2气体,得到溶液A,向A中逐滴缓慢加入0.1 molL-1的HCl溶液,产生的CO2气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示,通过计算回答:
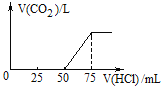
(1)A溶液中的溶质为_________(化学式),其物质的量之比是_______。
(2)通入CO2气体体积__________________(标准状况)。
(3)NaOH溶液的物质的量浓度______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意解答
(1)已知ClO2是易溶于水难溶于有机溶剂的气体,常用于自来水消毒.实验室制备ClO2是用亚氯酸钠固体与氯气反应:2NaClO2+Cl2═2ClO2+2NaCl,装置如图所示: 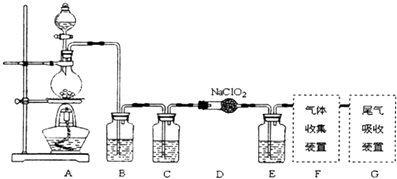
(i)烧瓶内可发生的反应的化学方程式: .
(ii)B,C,E装置中的试剂依次为
a、NaOH溶液 b、浓硫酸 c、饱和食盐水 d、CCl4 e、饱和石灰水
(iii)以下装置既能吸收尾气又能防止倒吸的是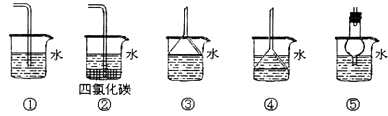
(2)用ClO2处理后的自来水中,ClO2的浓度应在0.10~0.80mgL﹣1之间.用碘量法检测水中ClO2浓度的实验步骤如下:取100mL的水样加稀硫酸调节pH至1~3,加入一定量的碘化钾溶液,振荡,再加入少量指示剂后,用1.0×10﹣4molL﹣1的Na2S2O3溶液滴定(己知:2S2O32﹣+I2═S4O62﹣+2I﹣). (i)加入的指示剂是 , 达到滴定终点时的现象是
(ii)碘化钾反应的离子方程式是
(iii)已知滴定终点时,消耗Na2S2O3溶液16.30mL,则水样中ClO2的浓度是mgL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20.00mL 0.1000molL﹣1 (NH4)2SO4溶液中逐滴加入0.2000molL﹣1 NaOH时,溶液的pH与所加NaOH溶液体积的关系如图所示(不考虑挥发).下列说法正确的是( ) 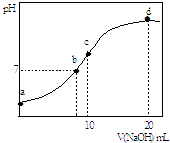
A.点a所示溶液中:c(SO42﹣)>c(NH4+)>c(H+)>c(OH﹣)
B.点b所示溶液中:c(NH4+)=c(Na+)>c(H+)=c(OH﹣)
C.点d所示溶液中:c(SO42﹣)>c(NH3H2O )>c(OH﹣)>c(NH4+)
D.点c所示溶液中:c(SO42﹣)+c(H+)=c(NH3H2O )+c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是人体不可缺少的微量元素,摄入含铁的化合物可补充铁.“速力菲”是市场上一种常见的补铁药物,如图1是它的说明书: 
该药品中Fe2+会缓慢氧化,国家规定该药物中Fe2+的氧化率超过10%即不能再服用.
(1)为了检验某药店出售的“速力菲”是否被氧化,实验室可选用的最常用且最灵敏的检验试剂为(填试剂的名称).
(2)实验室采用H2SO4酸化的KMnO4溶液对“速力菲”中的Fe2+进行滴定(假设药品中其他成分不与KMnO4反应);该反应的离子方程式为: .
(3)称量上述含铁元素质量分数为20.00%的“速力菲”19.00g,将其全部溶于稀硫酸中,配制成1000.00mL溶液.取出20.00mL,用0.01300mol/L的KMnO4溶液滴定,消耗KMnO4溶液体积如图2所示.
①实验前,首先要精确配制0.01300mol/L KMnO4溶液250mL,配制时需要的玻璃仪器除玻璃棒、烧杯、胶头滴管外,还需 .
②某同学的滴定方式(夹持部分略去)如图,最合理的是 . 
③由图可知消耗KMnO4溶液体积为mL;
④滴定终点观察到的现象为;
⑤以标准KMnO4溶液滴定样品溶液的浓度,判断以下操作所引起实验结果偏小的是 .
A.滴定过程中,锥形瓶振荡太剧烈,有少量液滴溅出
B.未用标准KMnO4溶液润洗滴定管
C.滴定接近终点时,用少量蒸馏水冲洗锥形瓶内壁
D.滴定前仰视,滴定后俯视(标准液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与滴定实验有关的说法中正确的是( )
A.容量瓶和滴定管都需要用试剂润洗
B.用NaOH滴定盐酸时,若滴定结束时俯视刻度,会导致测定结果偏高
C.用滴定管准确量取20.0 mL盐酸
D.用KMnO4滴定亚硫酸钠溶液的实验中不需要另外加入指示剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com