
科目:高中化学 来源: 题型:
| 元素 | 结构或性质信息 |
| T | 原子的L层上s电子数等于p电子数. |
| X | 元素的原子半径是第三周期主族元素中最大的. |
| Y | 空气中含其单质,原子的最外层未成对电子数是该元素所在周期中最多的. |
| Z | 单质常温、常压下是气体.原子的M层上有1个未成对的p电子. |

查看答案和解析>>
科目:高中化学 来源:湖北省天门中学2008-2009学年高二下学期5月月考化学试题(A卷) 题型:013
|
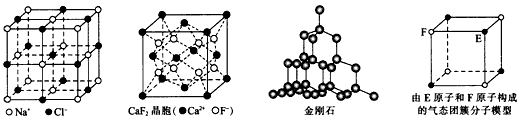
有关晶体的结构如下图所示,下列说法中不正确的是
| |
| [ ] | |
A. |
在NaCl晶体中,距Na+最近的Cl-形成正八面体 |
B. |
在CaF2晶体中,每个晶胞平均占有4个Ca2+ |
C. |
在金刚石晶体中,碳原子与碳碳键个数的比为1∶2 |
D. |
该气态团簇分子的分子式为EF或FE |
查看答案和解析>>
科目:高中化学 来源:江苏省清江中学2008-2009学年第二学期高二化学第2次月考试卷 题型:021
|
有关晶体的结构如下图所示,下列说法中不正确的是
| |
A. |
在NaCl晶体中,距Na+最近的Cl-形成正八面体 |
B. |
在CaF2晶体中,每个晶胞平均占有4个Ca2+ |
C. |
在金刚石晶体中,碳原子与碳碳键个数的比为1∶2 |
D. |
该气态团簇分子的分子式为EF或FE |
查看答案和解析>>
科目:高中化学 来源:黑龙江省齐齐哈尔市2009届高三第一次模拟考试、化学试卷 题型:013
|
钡在氧气中燃烧时得到一种钡的氧化物晶体,结构如下图所示,有关说法不正确的是
| |
| [ ] | |
A. |
该晶体属于离子晶体 |
B. |
晶体的化学式为Ba2O2 |
C. |
该晶体晶胞结构与NaCl相似 |
D. |
与每个Ba2+距离相等且最近的Ba2+共有12个 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com