
| A. | 在饱和AgCl、AgBr的混合溶液中c(Cl-)/c(Br-)=360 | |
| B. | 向AgCl悬浊液中滴加浓NaBr溶液会产生淡黄色沉淀 | |
| C. | AgCl在水中溶解度及Ksp均比在NaCl溶液中的大 | |
| D. | 向含有AgCl的饱和溶液中加入少量水后,c(Cl-)不变 |
分析 A.根据AgCl,AgBr的Ksp计算;
B.溶度积大的沉淀容易转化为溶度积小的沉淀;
C.溶解度与Ksp均只与温度有关;
D.加入少量水后仍然为氯化银饱和溶液,则氯离子的浓度不变.
解答 解:A.已知常温下Ksp(AgCl)=1.8×10-10,Ksp(AgBr)=5×10-13,在饱和AgCl,AgBr的混合溶液中:$\frac{c(C{l}^{-})}{c(B{r}^{-})}$=$\frac{{K}_{sp}(AgCl)}{{K}_{sp}(AgBr)}$=$\frac{1.8×1{0}^{-10}}{5×1{0}^{-13}}$=360,故A正确;
B.已知Ksp(AgCl)>Ksp(AgBr),溶度积大的沉淀容易转化为溶度积小的沉淀,所以向AgCl悬浊液中滴加NaBr溶液会产生淡黄色AgBr沉淀,故B正确;
C.溶解度与Ksp均只与温度有关,AgCl在水中溶解度及Ksp均与在NaCl溶液中的相同,故C错误;
D.向含有AgCl的饱和溶液中加入少量水后,得到的仍然为AgCl饱和溶液,则c(Cl-)不变,故D正确;
故选C.
点评 本题考查难溶电解质的溶解平衡及沉淀转化的本质,题目难度中等,明确难溶物溶解平衡及其影响为解答关键,注意溶度积常数的利用和理解,试题侧重考查学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C4H10的属于烷烃的同分异构体有3种 | |
| B. | 分子组成是C5H10属于烯烃的同分异构体有6种 | |
| C. | 分子组成是C4H8O属于醛类的同分异构体有3种 | |
| D. | 结构为 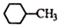 的物质的一溴代物有5种 的物质的一溴代物有5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸在水中电离:CH3COOH?H++CH3COO- | |
| B. | 乙烷和溴蒸气的混合物光照后发生反应:CH3CH3+Br2$\stackrel{光}{→}$CH3CH2Br+HBr | |
| C. | 苯在浓硫酸并加热条件下与浓硝酸发生反应: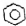 +HNO3$→_{50~60℃}^{浓硫酸}$ +HNO3$→_{50~60℃}^{浓硫酸}$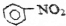 +H2O +H2O | |
| D. | 乙酸、乙醇和浓硫酸的混合物在加热条件下发生酯化反应:CH3COOH+CH3CH2OH$→_{△}^{催化剂}$CH3COOCH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
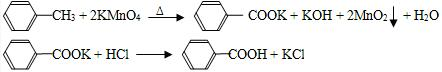
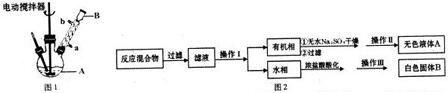
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
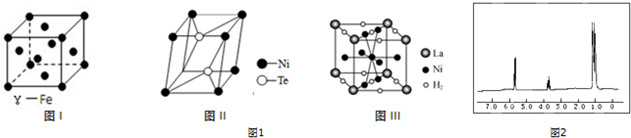
.

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
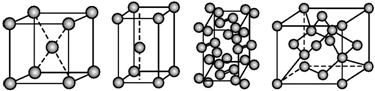
| A. | 碘、锌、钠、金刚石 | B. | 金刚石、锌、碘、钠 | C. | 钠、锌、碘、金刚石 | D. | 锌、钠、碘、金刚石 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com