
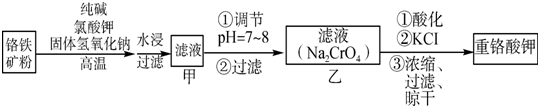
分析 铬铁矿(主要成份为FeO•Cr2O3、SiO2、Al2O3)加纯碱、NaOH和KClO3在高温下反应,生成Na2CrO4和Fe2O3,Al2O3、SiO2和纯碱反应生成NaAlO2和Na2SiO3,Fe2O3与纯碱反应生成NaFeO2,NaFeO2能强烈水解生成Fe(OH)3沉淀,过滤,滤渣为FeOH)3,调节pH7~8使NaAlO2和Na2SiO3转化为沉淀,酸化CrO42-转化为Cr2O72-,加KCl浓缩结晶过滤得到K2Cr2O7,
(1)根据过滤操作分析;
(2)高温下SiO2与纯碱反应生成硅酸钠和二氧化碳;高温下氧化铝与纯碱反应生成偏铝酸钠和二氧化碳;
(3)根据流程分析,水浸生成的沉淀是Fe(OH)3,调节pH7~8使NaAlO2和Na2SiO3转化为沉淀;
(4)利用溶解度不同Na2Cr2O7与KCl反应生成K2Cr2O7和NaCl;
(5)①碘遇淀粉变蓝色,到达终点时,碘完全反应,蓝色褪去;
②由Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O、I2+2S2O32-=2I-+S4O62- 可知,存在Cr2O72-~6S2O32-,以此计算,再求出质量和重铬酸钾的纯度.
解答 解:(1)过滤操作用到的玻璃仪器有:玻璃棒、烧杯、漏斗;故答案为:漏斗;
(2)SiO2与纯碱反应生成硅酸钠和二氧化碳,则化学方程式为SiO2+Na2CO3$\frac{\underline{\;高温\;}}{\;}$2Na2SiO2+CO2↑,
Al2O3与SiO2一样与Na2CO3反应,则Al2O3是作为酸性氧化物参与反应,生成偏铝酸钠,则反应的方程式为:Na2CO3+Al2O3$\frac{\underline{\;高温\;}}{\;}$2NaAlO2+CO2↑;
故答案为:SiO2+Na2CO3$\frac{\underline{\;高温\;}}{\;}$2Na2SiO2+CO2↑;Na2CO3+Al2O3$\frac{\underline{\;高温\;}}{\;}$2NaAlO2+CO2↑;
(3)根据流程分析可知水浸生成的沉淀是Fe(OH)3,调节pH=7~8是使Na2SiO3、NaAlO2发生水解反应而生成Al(OH)3和H2SiO3沉淀而除去杂质;
故答案为:Fe(OH)3;使NaAlO2和Na2SiO3发生水解而生成Al(OH)3和H2SiO3沉淀而除去;
(4)利用溶解度不同Na2Cr2O7与KCl反应生成K2Cr2O7和NaCl,反应的方程式为:Na2Cr2O7+2KCl=K2Cr2O7+2NaCl;
故答案为:Na2Cr2O7+2KCl=K2Cr2O7+2NaCl;
(5)①该滴定的原理是用碘化钾还原重铬酸钾,生成的I2使淀粉变蓝色,然后用Na2S2O3滴定生成的I2,因此终点现象是当滴入最后一滴Na2S2O3溶液,溶液蓝色褪去,而且半分钟内不恢复即达终点;
故答案为:当滴入最后一滴Na2S2O3溶液,溶液蓝色褪去,而且半分钟内不恢复即达终点;
②由Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O、I2+2S2O32-=2I-+S4O62- 可知,
存在Cr2O72-~6S2O32-,
1 6
n 0.1200×40×10-3mol
则250ml含重铬酸钾的物质的量为n=$\frac{0.1200×40×10{\;}^{-3}mol}{6}$×10,
则所得产品中重铬酸钾纯度为$\frac{0.1200×40×10{\;}^{-3}×10×294}{6×2.5000}$×100%=94.1%,
故答案为:94.1%.
点评 本题考查混合物的分离、提纯,明确流程中操作的目的是解答的关键,注意利用反应方程式中各物质之间的关系计算,(5)为解答的难点,题目难度中等,侧重于考查学生对基础知识的综合应用能力.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| 操作及现象 | 结 论 | |
| A | 用蒸馏水润湿的pH试纸测溶液的pH | 一定会使测定结果偏低 |
| B | 向硅酸钠溶液中,滴入硫酸 | 可以验证S的氧化性强于Si |
| C | 将SO2通入溴水中,溴水褪色 | SO2具有漂白性 |
| D | 向含有少量FeBr2的FeCl2溶液中,加入适量氯水,再加CCl4萃取分液 | 除去FeCl2溶液中的FeBr2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
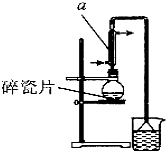 醇与氢卤酸反应是制备卤代烃的重要方法.实验室制备 1-溴丁烷的反应和实验装置如下:
醇与氢卤酸反应是制备卤代烃的重要方法.实验室制备 1-溴丁烷的反应和实验装置如下:| 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | |
| 正丁醇 | -89.53 | 117.25 | 0.81 |
| 1-溴丁烷 | -112.4 | 101.6 | 1.28 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 40.5% | B. | 60.6% | C. | 81.0% | D. | 100% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
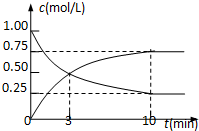 为实现“节能减排”和“低碳经济”的一项课题是如何将CO2转化为可利用资源.目前,工业上常用CO2来生产燃料甲醇.现进行如下实验:在体积为l L的密闭恒容容器中,充入l mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.
为实现“节能减排”和“低碳经济”的一项课题是如何将CO2转化为可利用资源.目前,工业上常用CO2来生产燃料甲醇.现进行如下实验:在体积为l L的密闭恒容容器中,充入l mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | m=2 | |
| B. | X 与 Y 的平衡转化率之比为 1:2 | |
| C. | 两次平衡的平衡常数相同 | |
| D. | 第二次平衡时,Z 的浓度为 0.2 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
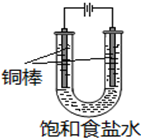 CuCl是应用广泛的有机合成催化剂,可采取不同方法制取.
CuCl是应用广泛的有机合成催化剂,可采取不同方法制取.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
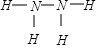 ,已知液态肼的标准燃烧热为-622kJ/mol,写出发生燃烧发生的热化学方程式:N2H4(l)+O2(g)=N2(g)+2H2O(l);△H=-622KJ/mol.
,已知液态肼的标准燃烧热为-622kJ/mol,写出发生燃烧发生的热化学方程式:N2H4(l)+O2(g)=N2(g)+2H2O(l);△H=-622KJ/mol.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com