
| 操作 | 现象 | 结论 | |
| A | 向某未知溶液中加入盐酸酸化的BaCl2溶液 | 生成白色沉淀 | 该溶液中一定含有SO42- |
| B | 用一束强光照射Na2SiO3溶液 | 溶液中出现一条光亮的通路 | 溶液中可能含有硅酸胶体 |
| C | 向盛有Fe(NO3)2溶液的试管中滴入几滴0.1mol/LH2SO4溶液 | 试管口出现红棕色气体 | 溶液中NO3-被Fe2+还原为NO2 |
| D | 淀粉溶液中加稀硫酸,加热片刻后再滴加银氨溶液,并用水浴加热 | 无银镜生成 | 淀粉未发生水解 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.白色沉淀可能为AgCl,原溶液中可能含有银离子;
B.胶体具有丁达尔效应,溶液不能产生丁达尔效应;
C.试管口出现红棕色气体,为一氧化氮与氧气反应生成红棕色的二氧化氮;
D.蔗糖水解后溶液为酸性,银镜反应应在碱性条件.
解答 解:A.原溶液中含有Ag+,也会有白色沉淀生成,则应先加盐酸酸化,排除干扰,再加氯化钡检验硫酸根离子,故A错误;
B.胶体具有丁达尔效应,溶液不能产生丁达尔效应,硅胶属于胶体,能产生丁达尔效应,硅酸钠溶液属于溶液,不能产生丁达尔效应,故B正确;
C.在酸性条件下,Fe2+与NO3-发生氧化还原反应,3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,对于该反应Fe2+为还原剂,NO3-为氧化剂,被还原成NO,试管口出现红棕色气体,为一氧化氮与氧气反应生成红棕色的二氧化氮,故C错误;
D.蔗糖水解后溶液为酸性,银镜反应应在碱性条件,则向稀硫酸与蔗糖共热后的溶液中滴加银氨溶液,水浴加热,无现象,是因没有加碱中和至碱性,故D错误;
故选B.
点评 本题考查实验方案评价,为高考高频点,涉及胶体性质、离子检验、蔗糖水解检验等知识,侧重实验操作和实验原理的考查,注意实验方案的操作性、可行性、评价性分析,易错选项是D.


科目:高中化学 来源: 题型:解答题
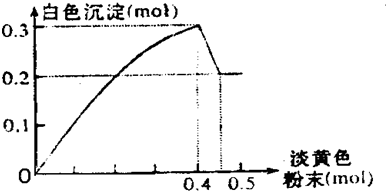
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12:7 | B. | 3:1 | C. | 1:3 | D. | 1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 装 置 | 现 象 |
 | Ⅰ.实验初始,未见明显现象 |
| Ⅱ.过一会儿,出现气泡,液面上方呈浅棕色 | |
| Ⅲ.试管变热,溶液沸腾 |
| 实 验 | 内 容 | 现 象 |
| 实验1 | 将湿润KI-淀粉试纸置于空气中 | 未变蓝 |
| 实验2 | 用湿润KI-淀粉试纸检验浅棕色气体 | 试纸变蓝 |
| 装置 | 现象 |
 | Ⅰ.实验初始,未见明显现象 |
| Ⅱ.过一会儿,出现气泡,有刺激性气味 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 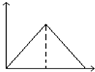 | B. | 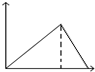 | C. | 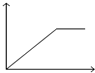 | D. | 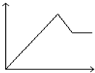 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
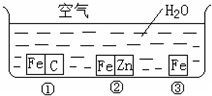 如何防止铁的锈蚀是工业上研究的重点内容.为研究铁的锈蚀,某同学做了探究实验,如图所示,铁处于①、②、③三种不同的环境中.请回答:
如何防止铁的锈蚀是工业上研究的重点内容.为研究铁的锈蚀,某同学做了探究实验,如图所示,铁处于①、②、③三种不同的环境中.请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com