
正丁醛经催化加氢可制备1-丁醇。为提纯含少量正丁醛杂质的1-丁醇,现设计如下路线:

已知:①正丁醛与饱和NaHSO3溶液反应可生成沉淀;②乙醚的沸点是34℃,难溶于水,与1-丁醇互溶;③1-丁醇的沸点是118℃。则操作1~4分别是( )
A.萃取、过滤、蒸馏、蒸馏 B.过滤、分液、蒸馏、萃取
C.过滤、蒸馏、过滤、蒸馏 D.过滤、分液、过滤、蒸馏
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源:2015届浙江省高三上学期期中联考化学试卷(解析版) 题型:选择题
同位素示踪法可用于反应机理的研究,下列反应或转化中同位素示踪表示正确的是
A.2Na218O2 + 2H2O = 4Nal8OH + O2↑
B.2KMnO4 + 5H218O2 + 3H2SO4 = K2SO4 + 2MnSO4 + 518O2↑+ 8H2O
C.NH4Cl + 2H2O NH3·2H2O + HCl
NH3·2H2O + HCl
D.K37ClO3 + 6HCl = K37Cl + 3Cl2↑+ 3H2O
查看答案和解析>>
科目:高中化学 来源:2015届河南郑州市高三上第一次(10月)月考化学试卷(解析版) 题型:选择题
取x g铜镁合金完全溶于浓硝酸中,若反应过程中HNO3被还原只生成NO、NO2,收集产生的气体,再通入0.56L氧气(标况),气体恰好可以被水吸收,在合金与HNO3反应后的溶液中加入足量的NaOH溶液可以生成3.9g沉淀,则x等于( )
A.1.2g B.2.2g C.3.2g D.无法计算
查看答案和解析>>
科目:高中化学 来源:2015届河南郑州市高三上第一次(10月)月考化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数,下列判断正确的是( )
A.在18 g 18O2中含有NA个氧原子
B.标准状况下,22.4 L空气含有NA个单质分子
C.1 mol Cl2参加反应转移电子数一定为2 NA
D.含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1 mol/L
查看答案和解析>>
科目:高中化学 来源:2015届河南省10月联考化学试卷(解析版) 题型:选择题
下列各组描述正确的是( )
A.化工生产要遵守三原则:充分利用原料、充分利用能量、保护环境。 ①燃烧时使用沸腾炉 ②制盐酸时将氯气在氢气中燃烧 ③制硫酸时使用热交换器 这3种化工生产分别符合以上某原则
B.①用燃烧的方法鉴别甲烷、乙烯和乙炔 ②用酒精萃取溴水中的溴 ③用水鉴别硝酸铵和氢氧化钠固体 ④用互滴法鉴别Na2CO3、盐酸、BaCl2、NaCl四种溶液 以上均能达到实验目的
C.①用硫粉覆盖地下撒有的汞 ②金属钠着火用泡沫灭火器或干粉灭火器扑灭 ③用热碱溶液洗去试管内壁的硫 ④用湿的红色石蕊试纸检验氨气是否集满 以上操作均合理
D.①过氧化氢:火箭燃料 ②碳酸氢钠: 食品发酵剂 ③钠:制氢氧化钠 ④硫酸:制蓄电池 以上物质的用途均合理
查看答案和解析>>
科目:高中化学 来源:2015届河南省10月联考化学试卷(解析版) 题型:选择题
将锌、铁、铜粉末按一定比例混合投入到一定量的硝酸中,微热,充分反应后过滤,弃去滤渣,滤液中金属阳离子情况不可能是( )
A.只含Cu2+、Fe2+、Zn2+ B.只含Zn2+
C.只含Fe2+、Zn2+ D.只含Cu2+、Fe3+、Zn2+
查看答案和解析>>
科目:高中化学 来源:2015届河南省洛阳市高三上学期期中考试化学试卷(解析版) 题型:实验题
为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验).
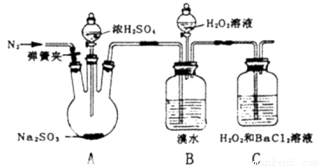
实验操作 | 实验现象 |
i.打开A中分液漏斗活塞,滴加浓硫酸 | A中有气泡产生,B中红棕色溴水褪色,C中有白色沉淀 |
ii.取C中沉淀加入盐酸 | C中白色沉淀不溶解 |
iii.打开B中分液漏斗活塞,逐滴滴加H2O2 | 开始时颜色无明显变化,继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
(1)A中发生反应的化学方程式是 .
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性:H2O2>SO2.
①乙同学认为不能得出此结论,认为在滴加浓硫酸之前应增加一步操作,该操作是 .
②丙同学认为还应该在B和C之间增加洗气瓶D,D中盛放的试剂是 .
③iii中滴入少量H2O2没有明显变化.提出假设:
观点1:H2O2的量少不能氧化Br-
观点2:B中有未反应的H2SO3
为验证观点2,应进行的实验操作及现象是 .
(4)通过上述全部实验,得出结论:H2O2、SO2、Br2氧化性由强到弱的顺序是 .
查看答案和解析>>
科目:高中化学 来源:2015届河南省洛阳市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列表示对应化学反应的离子方程式正确的是
A.漂白粉溶液通入SO2:Ca2++2ClO-+SO2+H2O=2HClO+CaSO3↓
B.向FeBr2溶液中通入过量氯气:2Fe2++Cl2=2Fe3++2Cl-
C.石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O
D.Na2O2溶于水产生O2:Na2O2+H2O=2Na++2OH-+O2↑
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市高三上学期第四次检测化学试卷(解析版) 题型:填空题
(14分)某混合物,可能含有以下几种离子:K+、Cl-、NH4+、Mg2+、CO32-、Ba2+、SO42-,若将该混合物溶于水可得澄清溶液,现取3份各100 mL该溶液分别进行如下实验:
实验 序号 | 实验内容 | 实验结果 |
1 | 加AgNO3溶液 | 有白色沉淀生成 |
2 | 加足量NaOH溶液并加热 | 收集到气体1.12 L(已折算成标准状况下的体积) |
3 | 加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 | 第一次称量读数为6.63 g,第二次称量读数为4.66 g |
试回答下列问题:
(1)根据实验1对Cl-是否存在的判断是____________(填“一定存在”“一定不存在”或“不能确定”);根据实验1~3判断混合物中一定不存在的离子是____________。
(2)试确定溶液中一定存在的阴离子及其物质的量浓度((可以不填满,也可以增加)):
阴离子符号 | 物质的量浓度(mol/L) |
(3)试确定K+是否存在?________,如果存在物质的量浓度为__________,如果不存在理由是__ _。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com