
| A、达到平衡时,抽出少量氯气,反应混合液颜色变深 |
| B、加入少量SCl2,平衡向逆反应方向移动 |
| C、单位时间内生成n mol S2Cl2,同时生成2n mol SCl2时,反应达到平衡 |
| D、达平衡时,升高温度,混合液的颜色将变浅 |


科目:高中化学 来源: 题型:
| A、①② | B、①③ | C、③④ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
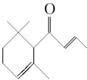 ,有关该化合物的下列说法不正确的是( )
,有关该化合物的下列说法不正确的是( )| A、分子式为C13H20O |
| B、该化合物可发生银镜反应 |
| C、该物质不属于醇类 |
| D、与溴的CCl4溶液反应生成的产物经水解、稀硝酸酸化后可用AgNO3溶液检验. |
查看答案和解析>>
科目:高中化学 来源: 题型:
 用如图装置电解硫酸钾溶液来制取氧气、氢气、硫酸和氢氧化钾.
用如图装置电解硫酸钾溶液来制取氧气、氢气、硫酸和氢氧化钾.查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、“加碘盐”、“高钙牛奶”、“富硒营养品”等食用品中的碘、钙、硒是指单质 |
| B、“酸可以除锈”,“热的纯碱溶液去油污”都是发生了化学变化 |
| C、医疗上进行胃部造影前,患者服用的“钡餐”是BaCO3等不溶于水的物质 |
| D、铝合金的大量使用归功于人们能用焦炭等还原剂从氧化铝中获取铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al2O3用作耐火材料 |
| B、Na2O常用于潜水艇或呼吸面具的供氧剂 |
| C、明矾溶于水形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
| D、FeCl3溶液可用于刻制印刷电路板 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com