
【题目】下列关于物质分类的叙述中,不正确的是
A.NO2属于氧化物B.H2SO4属于酸C.KOH属于碱D.氨水属于纯净物
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
【题目】【化学一选修5:有机化学基础】由羧酸A (C3H4O2) 经过如下合成路线获得药物中间体H。
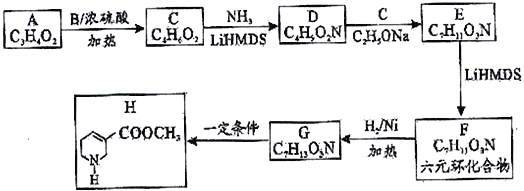
已知:Ⅰ.R1CH=CH1+RNH2 ![]() R1CH2CH2NHR(R可以是氢原子或烃基)
R1CH2CH2NHR(R可以是氢原子或烃基)
Ⅱ.R1COOR2+R3CH2COOR4![]()
![]() +R2OH
+R2OH
请回答:
(1)化合物A 的名称_________________,B的结构简式_______________。
(2)写出药物中间体H中两种官能团的名称_______________________。
(3)已知D的结构简式:H2N-CH2-CH2-COOCH3,D→E的反应类型________________,F→G的反应类型_________________。
(4)写出E→F的化学方程式______________________________________。
(5)写出化合物D符合下列条件的所有可能的同分异构体的结构简式_______(任写两种即可)
①分子中含六元环。
②红外光谱显示分子中含有碳氮单键。
③核磁共振氢谱显示分子中有3种化学环境不同的氢原子。
(6)设计由乙酸甲脂合成聚合物:![]() 的单体的合成路线(其他试剂任选)。(用流程图表示)____________________________。
的单体的合成路线(其他试剂任选)。(用流程图表示)____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液 体积的关系如图所示,由此确定,原溶液中含有的阳离子是( )
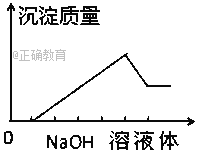
A. Mg2+、Al3+、Fe2+ B. H+、Mg2+、Al3+
C. H+、Ba2+、Al3+ D. 只有Mg2+、Al3+
【答案】B
【解析】根据图像,可以看出分为4个阶段:第一阶段无沉淀,第二阶段沉淀量逐渐增多到最大量,第三阶段有部分沉淀能和氢氧化钠继续反应,即部分沉淀溶解,第四阶段沉淀的量不再随着氢氧化钠量的增多而增加。第一阶段无沉淀,说明水溶液中一定含有氢离子,故AD错误,第三阶段有部分沉淀能和氢氧化钠继续反应,说明部分沉淀是氢氧化铝,原溶液中一定含有铝离子,第四阶段沉淀的量不再随着氢氧化钠量的增多而增加,说明一定有一种沉淀和氢氧化钠不反应,可推知该沉淀是氢氧化镁,原溶液中一定含有镁离子,铜离子有颜色,与溶液无色不符,故B正确,C错误;故选B。
【题型】单选题
【结束】
14
【题目】将适量铁粉放入FeCl3溶液中,完全反应后,溶液中的Fe2+和Fe3+浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是( )
A. 2∶3 B. 3∶2
C. 1∶2 D. 1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将①H+、②Cl-、③Al3+、④K+、⑤S2-、⑥OH-、⑦NO3-、⑧NH4+分别加入H2O中,基本上不影响水的电离平衡的是
A. ①③⑤⑦⑧ B. ②④⑦ C. ①⑥ D. ②④⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)2017年,宿迁市成功创建为全国文明卫生城市,城市生态环境明显改善。
①下列做法不利于改善空气质量的是_________。
a.工厂通过静电除尘减少悬浮颗粒物排放
b.以新能源公交车代替燃油公交车
c.夜间排放工业废气
② 公共场所安装直饮水设备,方便市民饮用。直饮水需要经过活性炭处理、超滤膜过滤、紫外灯照射等处理过程。其中活性炭作为_________。
a. 混凝剂 b. 吸附剂 c.杀菌、消毒剂
③ 宿迁40余处“落叶景观带”成为扮靓城市的秋冬美景,为保护落叶景观带设置的“严禁烟火”标志是_________。

a b c
(2)红薯含有丰富的淀粉、膳食纤维、胡萝卜素、维生素A、B、C、E以及钾、铁、钙等多种营养成分,是一种营养均衡的保健食品。
① 红薯中含有的_________可有效改善牙龈出血。
a.维生素A b.维生素B c.维生素C
② 以上成分中,_________(填元素符号)为人体必需的微量元素。
③ 红薯中含有丰富的淀粉,其在人体内完全水解的最终产物是____(填化学式)。实验室检验该水解产物所用的试剂是_________。
④ 红薯不宜过多食用,否则会产生较多胃酸。双羟基铝碳酸钠[NaAl(OH)2CO3]是一种常用的抗酸药,它和胃酸反应的化学方程式为:__________。
(3)2017年,世界最长的跨海大桥——港珠澳跨海大桥正式通车。建造大桥使用了大量钢材、水泥、玻璃、光导纤维、橡胶等材料。

① 工业上生产水泥、玻璃都用到的原料是_________。
② 深埋在海水中的钢管桩易发生_______腐蚀,下列保护钢管桩的措施不合理的是________。
a.使用抗腐蚀性强的合金钢
b.在钢材表面喷涂防腐涂料
c.钢管桩附着铜以增强抗腐蚀性
③ 港珠澳大桥工程使用了大量密封橡胶衬垫。为使橡胶性能更好,天然橡胶需经过__________处理以增强其机械性能。
④ 光导纤维是由高纯度SiO2于2000℃下拉制而成,工业上常用SiCl4与O2在高温条件下通过置换反应制得SiO2,该反应的化学方程式为:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于铜电极的叙述中不正确的是
A.用电解法精炼粗铜时,粗铜作阳极
B.在原电池中,铜电极只能作正极
C.在镀件上镀铜时,金属铜作阳极
D.锌铜原电池(稀硫酸为电解质溶液),铜极上发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温下,有浓度均为0.1mol/L的三种溶液:a.NaHCO3;b.NaClO;c.CH3COONa。
①三种溶液pH由大到小的顺序为:__________________填序号)。
②溶液a的pH大于8,则溶液中c(H2CO3)____c(CO32-) (填“>”、“<”或“=”)。
(2)已知25℃时,Ksp[AgCl]=1.8×10-10,现将足量氯化银分别放入:a.100mL蒸馏水中;b.100mL 0.2 mol/LAgNO3溶液中;c.100mL 0.1 mol/L氯化铝溶液中;d.100mL 0.1 mol/L盐酸溶液中。充分搅拌后,相同温度下银离子浓度由大到小的顺序是________ 。 (填写序号);b中氯离子的浓度为_______mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚氨酯类高分子材料PU用途广泛,其合成反应为:
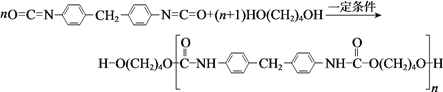
下列说法不正确的是
A. HO(CH2)4OH的沸点高于CH3CH2CH2CH3
B. 高分子材料PU在强酸、强碱中能稳定存在
C. 合成PU的两种单体的核磁共振氢谱中均有3个吸收峰
D. 以1,3-丁二烯为原料,可合成HO(CH2)4OH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com