
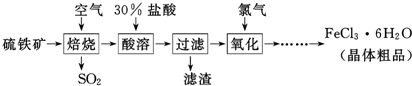
���� ����������Ҫ�ɷ�ΪFeS2��Ϊԭ���Ʊ��Ȼ������壨FeCl3•6H2O��������ʯͨ��������յõ��������Ͷ������������ϡ�������ܺ���˺�õ���Һ��������������������Ϊ�����ӣ�ͨ������Ũ������ȴ�ᾧ������ϴ�ӣ�����õ������Ȼ������壬
��1�������������������������Һ��Ӧ�������������ƣ�
��2��ԭ���е���������������ɵ��Ȼ�����Ŀ�����ʣ�����������������������ӵ�ˮ�⣬������ˮ�����������������
��3��������ǿ�����������������������ӣ�β����������ͼ�����жϣ�������������ӷ������Ȼ������壻
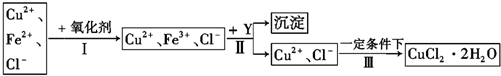
��CuCl2��Һ�к�����������FeCl2��Ϊ�Ʊ�������CuCl2•2H2O���壬ʵ��ԭ���ǣ�������Һ�м�������������������������Ϊ�����ӣ�����ѡ������������������������ӣ�Ȼ�����pH������������ȫ����������ͭ���Ӳ��������õ��Ȼ�ͭ��Һ��ͭ������ˮ�⣬Ȼ�������Ի����£�����Һ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ����T�ɵõ��Ȼ�ͭ���壬
��4��������Ҫ����Ӧ���������������ӣ�H2O2����ɫ���������ݴ˻ش�
��5��������Һ������Դ�ʹFe3+������ȫ������ͭ���Ӳ�������������Լ����Ժ������ӷ�Ӧ�����Dz��������������ӣ�
��6���Ȼ�ͭ��Һ��ͭ������ˮ�⣬Ӧ�������Ի����½��в������õ��Ȼ�ͭ���壮
��� �⣺��1�������������������������Һ��Ӧ�����������ƣ���Ӧ�Ļ�ѧ����ʽΪ��SO2+NaOH=NaHSO3��
�ʴ�Ϊ��SO2+NaOH=NaHSO3��
��2�����ܼ����������о��豣�������������Ŀ����ʹ�������ܽ�Ϊ�Ȼ��������������ӵ�ˮ�⣬
�ʴ�Ϊ��ʹ�������ܽ�Ϊ�Ȼ���������Fe3+ˮ�⣻
��3��ͨ����������ʱ������������������Ϊ�����ӣ���������Ҫ��Ӧ�����ӷ���ʽΪ��Cl2+2Fe2+=2Cl-+2Fe3+���ù��̲�����β�����ü���Һ���գ�β������Ⱦ����������Ϊ������������������Һ�лӷ������Ȼ������壻
�ʴ�Ϊ��Cl2+2Fe2+=2Cl-+2Fe3+��Cl2��HCl��
��CuCl2��Һ�к�����������FeCl2��Ϊ�Ʊ�������CuCl2•2H2O���壬ʵ��ԭ���ǣ�������Һ�м�������������������������Ϊ�����ӣ�����ѡ������������������������ӣ�Ȼ�����pH������������ȫ����������ͭ���Ӳ��������õ��Ȼ�ͭ��Һ��ͭ������ˮ�⣬Ȼ�������Ի����£�����Һ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ����T�ɵõ��Ȼ�ͭ���壬
��1��K2Cr2O7��NaClO����������������ͬʱ���������������ӣ�����H2O2����ɫ�����������������������ӣ�����ѡC����Ӧ��ԭ��Ϊ��2Fe2++H2O2+2H+�T2Fe3++2H2O��
�ʴ�Ϊ��C��2Fe2++H2O2+2H+�T2Fe3++2H2O��
��2���ڲ�����У�����Y��Ŀ����Ϊ�˵�����Һ������Դ�ʹFe3+������ȫ������ͭ���Ӳ���������Ӧ������Һ��pHΪ3.2��pH��4.7��������Լ����Ժ������ӷ�Ӧ�����Dz��������������ӣ�����������ͭ����ʽ̼��ͭ��̼��ͭ����������ͭ�ȣ�
�ʴ�Ϊ��3.2��pH��4.7��C��
��3���Ȼ�ͭ��Һ��ͭ������ˮ�⣬Ӧ�������Ի����£�����Һ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����õ��Ȼ�ͭ���壬
�ʴ�Ϊ������Һ�ڽϵ��¶��¼��������������壬ͬʱͨ���Ȼ��������ֹˮ�⣮
���� ���⿼�������̲����еIJ���Ŀ�ĺͷ�Ӧ����Ӧ����ķ����жϣ�β���ijɷ��жϺʹ�����������Ŀ�Ѷ��еȣ�����ʱע��ʵ�����֪ʶ��������ã�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Al2O3 | B�� | Fe2O3 | C�� | Al��OH��3 | D�� | Fe��OH��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ԭ�ӵĽṹʾ��ͼΪ�� ������ԭ�ӵĽṹʾ��ͼΪ�� ������ԭ�ӵĽṹʾ��ͼΪ��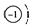 | |
| B�� | ����ԭ������һ��������ɵķ����Ӻ�һ��������ɵķ����� | |
| C�� | ����ԭ�ӵ�Ħ������Ϊ1g/mol | |
| D�� | 21H�ķ���ԭ������2��������ɵķ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
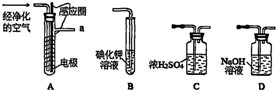
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
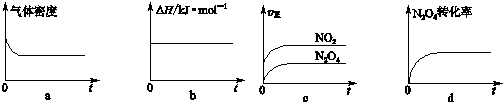
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶ȣ��棩 | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| ƽ����ѹǿ��kPa�� | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| ƽ��������Ũ�ȣ���10-3mol/L�� | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
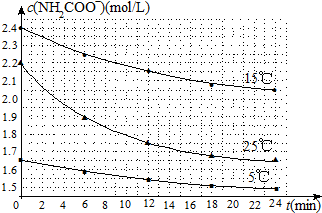
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
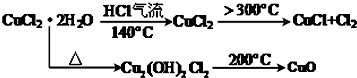
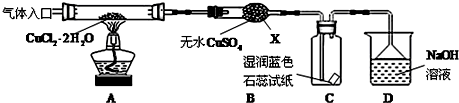
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com