
| c2(SO3) |
| c2(SO2)c(O2) |
| c2(SO3) |
| c2(SO2)c(O2) |


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源:2012-2013学年江西省高安中学高二上学期期末考试化学试卷(带解析) 题型:实验题
(共16分)
Ⅰ实验室制备1,2-二溴乙烷的反应原理如下:
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。
用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示:
有关数据列表如下: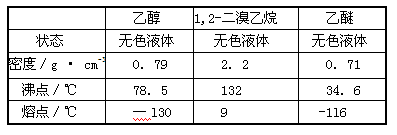
回答下列问题:
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是 ;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入 ,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)若产物中有少量副产物乙醚.可用 的方法除去;
(4)反应过程中应用冷水冷却装置D,其主要目的是避免溴大量挥发,但又不能过度冷却(如用冰水),其原因是 。
Ⅱ.已知烯烃与苯在一定条件下反应生成芳香烃。如:
丙烯是三大合成材料的基本原料,可用于合成应用广泛的DAP树脂单体和双酚等有机物,具有重要的工业用途。
(1)写出丙烯在一定条件下发生聚合反应的化学方程式 。
(2)丙烯在乙酸作用下与O2反应生成有机物A,其蒸气密度是相同状况下甲烷密度的6.25倍,元素的质量分数为:碳60%、氧32%。A的分子式为 。
(3)丙烯与苯在一定条件下反应可生成D、E、F等多种芳香烃。红外光谱、核磁共振是研究有机物结构的重要方法,根据下列数据,画出D、E的结构。
D:元素组成:C89.94%、H10.06%;1H核磁共振有5个信号。
E:元素组成:C88.82%、H11.18%;1H核磁共振有3个信号。
F:元素组成:C88.82%、H11.18%;1H核磁共振有4个信号。
D: 。 E: 。
查看答案和解析>>
科目:高中化学 来源:2014届江西省高二上学期期末考试化学试卷(解析版) 题型:实验题
(共16分)
Ⅰ实验室制备1,2-二溴乙烷的反应原理如下:

可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。
用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示:

有关数据列表如下:

回答下列问题:
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是 ;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入 ,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)若产物中有少量副产物乙醚.可用 的方法除去;
(4)反应过程中应用冷水冷却装置D,其主要目的是避免溴大量挥发,但又不能过度冷却(如用冰水),其原因是 。
Ⅱ.已知烯烃与苯在一定条件下反应生成芳香烃。如:

丙烯是三大合成材料的基本原料,可用于合成应用广泛的DAP树脂单体和双酚等有机物,具有重要的工业用途。
(1)写出丙烯在一定条件下发生聚合反应的化学方程式 。
(2)丙烯在乙酸作用下与O2反应生成有机物A,其蒸气密度是相同状况下甲烷密度的6.25倍,元素的质量分数为:碳60%、氧32%。A的分子式为 。
(3)丙烯与苯在一定条件下反应可生成D、E、F等多种芳香烃。红外光谱、核磁共振是研究有机物结构的重要方法,根据下列数据,画出D、E的结构。
D:元素组成:C89.94%、H10.06%;1H核磁共振有5个信号。
E:元素组成:C88.82%、H11.18%;1H核磁共振有3个信号。
F:元素组成:C88.82%、H11.18%;1H核磁共振有4个信号。
D: 。 E: 。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
当事人使用的液态洁污剂之一必定含氯,最可能的存在形式是___________和___________。当另一种具有___________(性质)的液态洁污剂与之混合时,可能发生如下反应而产生氯气:______________________。
(Ⅱ)当今世界存在着两大类环境问题。一类是在工业化过程中排放大量废水、废气、废渣带来的环境污染问题;另一类是由于不合理开发利用自然资源导致的森林锐减、水土流失、土地沙漠化和物种灭绝等生态破坏问题。据此,请回答下列问题:
(1)中国是发展中国家,上述两类问题兼而有之,你认为我国目前最严重的是哪一类问题?________________
(2)你认为(1)中这一类问题在很大程度上是由下列哪一项造成的( )
A.贫困 B.工业高度发展 C.生活富裕 D.农业发展
(3)工厂的产值不一定都是“正”产值,它还产生“负”产值。例如,炼钢厂生产钢铁,当然会给GDP(国民生产总值)增加正产值,但同时由于排放废气、废水、废物,污染了环境,弄脏了河水,又产生了负产值。下列哪种生产不会带来很高的负产值( )
A.接触法制硫酸 B.氨氧化法制硝酸
C.采用大棚培养反季蔬菜 D.五金电镀车间生产电镀零件
(4)森林的大幅度锐减,除了造成水土流失、土地沙漠化和物种灭绝外,还会带来什么危机?
____________________________________________________________________。
(5)在我国城市环境中,往往是重工业发达的地区污染也最严重。请写出几个我国工业发达的城市:(至少两个)________________________________________________________________。
(6)“保护环境,就是保护人类自己。”目前,在我国城市环境中主要的大气污染物是____________________________________________________________________。
(7)在全国各省、市、自治区的主要城市都设有大气监测站,主要工作是监测大气情况,且每天都公布空气质量情况下。下列各项的含量一定会进行监测的是___________。
①可吸入颗粒物 ②总悬浮颗粒物 ③氮氧化物 ④二氧化碳 ⑤二氧化硫 ⑥二氧化氮 ⑦一氧化碳 ⑧一氧化氮 ⑨氮气 ⑩臭氧
(8)我国政府已经注意到了环境污染的危害性,因此___________和计划生育是我国最基本的国策。并专门制订了一部法律称为___________。
(9)环境问题的重要性也成为各国申办奥运会的注意点。各国纷纷打出“环境”牌,并将其放在第一位,我国也不例外。北京为申办2008年奥运会除喊出“新北京”、“新奥运”外,还提出申办的三个理念:人文奥运,科技奥运,还有一个是什么? ___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com