
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年陕西省西安地区八校高三下学期联考三理综化学试卷(解析版) 题型:实验题
(14分)乙酰苯胺可用作止痛剂、退热剂、防腐剂和染料中间体,实验室制备乙酰苯胺反应原理和有关数据如下:
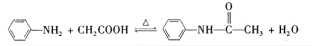
名称 | 相对分子质量 | 性状 | 密度(g/cm3) | 沸点/℃ | 溶解度 | |
苯胺 | 93 | 无色油状液体具有还原性 | 1.02 | 184 | 微溶于水 | 均易溶于乙醇、乙醚 |
乙酸 | 60 | 无色液体 | 1.05 | 118 | 易溶于水 | |
乙酰苯胺 | 135 | 白色晶体 | 1.22 | 304 | 微溶于冷水、溶于热水 | |
实验步骤:
在50ml圆底烧瓶中加入无水苯胺5ml.,冰醋酸7.5mL,锌粉0.lg,按下图安装仪器,加入沸石,给反应器均匀加热,使反应液在微沸状态下回流,调节加热温度,使柱顶温度控制在105℃左右,反应约60~ 80nun,当反应基本完成时,停止加热.
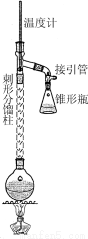
在搅拌下,趁热将烧瓶中的物料倒人盛有l00mL冰水的烧杯中,剧烈搅拌,并冷却烧杯至室温,粗乙酰苯胺结晶析出,抽滤、洗涤、干燥,得到乙酰苯胺粗品.将粗品重结晶,抽滤,晾干,称重,计算产率,注:D为刺形分馏柱,用于沸点差别不太大的混合物的分离.
请回答下列问题:
(1)仪器B的名称 。
(2)装置图中加热可用 (填“水浴”或“油浴”)。
(3)实验中加入锌粉的目的是 。
(4)为何要控制分馏柱上端的温度在105℃左右 。
(5)通过观察到 ,现象可判断反应基本完成,反应结束后须立即倒入事先准备好的冰水中的原因 。
(6)洗涤乙酰苯胺粗品最合适的试剂是 。
a.用少量冷水洗
b.用少量热水洗
c.先用冷水洗,再用热水洗
d.用酒精洗
(7)该实验最终得到纯品1.8 g,则乙酰苯胺的产率是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高二下学期期中考试化学试卷(解析版) 题型:选择题
己烯雌酚是一种激素类药物,结构如下。下列有关叙述中不正确的是
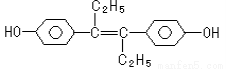
A.它易溶于有机溶剂
B.可与NaOH和NaHCO3发生反应
C.1mol该有机物可以与5mol Br2发生反应
D.该有机物分子中,一定有12个碳原子共平面
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省宝鸡市高二4月月考化学试卷(解析版) 题型:填空题
(16分)请根据官能团的不同对下列有机物进行分类。
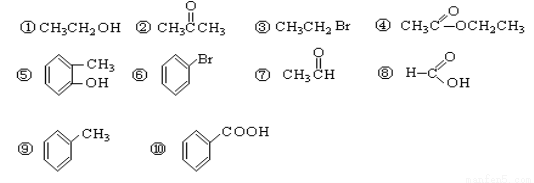
(1)芳香烃: ; (2)卤代烃: ;
(3)醇: ; (4)酚: ;
(5)醛: ; (6)酮: ;
(7)羧酸: ; (8)酯: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省宝鸡市高二4月月考化学试卷(解析版) 题型:选择题
根据下表中烃的分子式排列规律,判断空格中烃的同分异构体数目是
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
CH4 | C2H4 | C3H8 | C4H8 | C6H12 | C7H16 | C8H16 |
A.3 B.4 C.5 D.6
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省宝鸡市高二4月月考化学试卷(解析版) 题型:选择题
通过核磁共振氢谱可以推知(CH3)2CHCH2CH2OH有多少种化学环境的氢原子
A.6 B.5 C.4 D.3
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省德阳市高二下学期第一次月考化学试卷(解析版) 题型:简答题
(12分)二甲醚(CH3OCH3)是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上以CO和H2为原料生产二甲醚CH3OCH3的新工艺主要发生三个反应:
①CO(g) + 2H2(g)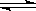 CH3OH(g) △H1=-Q1 kJ·mol-1
CH3OH(g) △H1=-Q1 kJ·mol-1
②2CH3OH(g)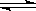 CH3OCH3(g)+ H2O(g) △H2=-Q2 kJ·mol-1
CH3OCH3(g)+ H2O(g) △H2=-Q2 kJ·mol-1
③CO(g)+ H2O(g)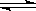 CO2(g) + H2(g) △H3=-Q3 kJ·mol-1
CO2(g) + H2(g) △H3=-Q3 kJ·mol-1
回答下列问题:
(1)新工艺的总反应3H2(g)+ 3CO(g)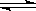 CH3OCH3(g)+ CO2(g)的热化学方程式为 。
CH3OCH3(g)+ CO2(g)的热化学方程式为 。
(2)工业上一般在恒容密闭容器中采用下列反应合成甲醇:CO(g) + 2H2(g) 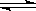 CH3OH (g) △H。下表所列数据是该反应在不同温度下的化学平衡常数(Κ)。
CH3OH (g) △H。下表所列数据是该反应在不同温度下的化学平衡常数(Κ)。
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
①由表中数据判断ΔH 0 (填“ >”、“=”或“<”)。能够说明某温度下该反应是平衡状态的是 。
A.体系的压强不变 B.密度不变
C.混合气体的相对分子质量不变 D.c(CO)=c(CH3OH)
②某温度下,将 2mol CO和 6mol H2 充入2L的密闭容器中,充分反应 10min后,达到平衡时测得c(CO)=0.2mol/L,计算此温度下的平衡常数K= 。
(3)工业生产是把水煤气中的混合气体经过处理后获得的较纯H2用于合成氨。合成氨反应原理为:N2(g)+3H2(g)  2NH3(g) ΔH=-92.4kJmol-1。实验室模拟化工生产,在恒容密闭容器中充入一定量N2和H2后,分别在不同实验条件下反应,N2浓度随时间变化如图1。请回答下列问题:
2NH3(g) ΔH=-92.4kJmol-1。实验室模拟化工生产,在恒容密闭容器中充入一定量N2和H2后,分别在不同实验条件下反应,N2浓度随时间变化如图1。请回答下列问题:
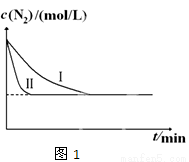
①与实验Ⅰ比较,实验Ⅱ改变的条件为 。
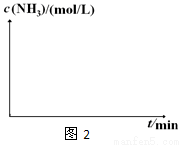
②在实验Ⅲ中改变条件为采用比实验Ⅰ更高的温度,请在图2中画出实验Ⅰ和实验Ⅲ中c(NH3)随时间变化的示意图。
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省德阳市高二下学期第一次月考化学试卷(解析版) 题型:选择题
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。其反应原理如下:
电池:Pb(s) + PbO2(s) + 2H2SO4(aq) = 2PbSO4(s) + 2H2O(l)
电解池:2Al + 3H2O = Al2O3 + 3H2↑
对该电解过程,以下判断正确的是
电 池 | 电 解 池 | |
A | H+ 移向Pb电极 | H+ 移向Pb电极 |
B | 每消耗3mol Pb | 生成1mol Al2O3 |
C | 正极:PbO2+4H++2e-=Pb2++2H2O | 阳极:2Al+3H2O-6e-=Al2O3+6H+ |
D | Pb电极反应质量不变 | Pb电极反应质量不变 |
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省宿迁市三校高一下学期4月月考化学试卷(解析版) 题型:选择题
下列化学或离子方程式正确的是
A.常温下,将铁片置于浓硝酸中:Fe+6HNO3(浓)==Fe(NO3)3+3NO2↑+3H2O
B.氢氧化铜与盐酸反应:H++OH–= H2O
C.利用腐蚀法制作印刷电路板:Fe3++Cu=Fe2++Cu2+
D.向浓硝酸中加入铜片:Cu+4H++4NO3–==Cu2++2NO2↑+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com