
 .
. .
. (任意2种)(任写两种).
(任意2种)(任写两种).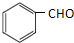 与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为
与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为 .
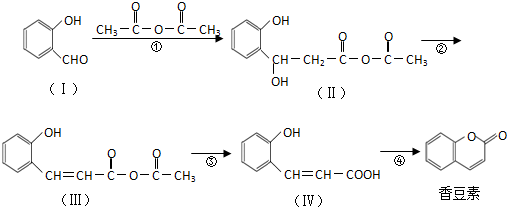
. 分析 (1)根据有机物I的结构简式判断含有的原子种类与个数,可确定分子式;
(2)反应①是乙酸酐中甲基与醛基发生加成反应;反应④发生酯化反应;
(3)反应②中醇羟基与相邻的氢原子脱去1分子式形成碳碳双键,发生消去反应;
(4)香豆素水解可生成酚羟基和羧基,二者都能与NaOH继续发生反应;
(5)苯环上含有两个邻位取代基,能发生银镜反应,说明含有-CHO,另一官能团为-COOH或酯基;
(5)反应①发生醛的加成反应,反应②发生醇的消去反应.
解答 解:(1)Ⅰ的分子中含有7个C、6个H、2个O,则分子式为C7H6O2,故答案为:C7H6O2;
(2)反应①是乙酸酐中甲基与醛基发生加成反应,反应④为酯化反应,故答案为:加成反应;酯化反应;
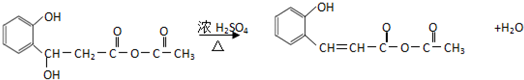
(3)反应②中醇羟基与相邻的氢原子脱去1分子式形成碳碳双键,发生消去反应,反应方程式为: ,
,
故答案为: ;
;
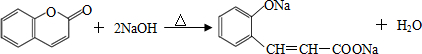
(4)香豆素水解可生成酚羟基和羧基,二者都能与NaOH反应,反应的方程式为 ,
,
故答案为: ;
;
(5)Ⅴ是Ⅳ的同分异构体,Ⅴ的分子中含有苯环且无碳碳双键,苯环上含有两个邻位取代基,能发生银镜反应,说明含有-CHO,另一官能团为-COOH或酯基,对应的醛基可为-CHO、-CH2CHO,另一取代基可为-CH2COOH、-COOH、-COOCH3、-OOCCH3、-OOCH等,则对应的同分异构体可能为 ,
,
故答案为: (任意2种);
(任意2种);
(6) 与CH3CHO发生加成反应生成
与CH3CHO发生加成反应生成 ,然后发生消去反应可生成
,然后发生消去反应可生成 ,
,
故答案为: .
.
点评 本题考查有机物的合成、有机物的结构性质、有机反应类型、限制条件同分异构体书写等,难度中等,熟练掌握官能团的性质与转化,注意(5)中有机物同分异构体的判断.


科目:高中化学 来源: 题型:解答题
 $→_{△}^{浓硫酸}$CH3COOCH(CH3)2+H2O.
$→_{△}^{浓硫酸}$CH3COOCH(CH3)2+H2O.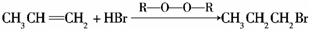 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 计算机芯片的组成元素位于第14纵行 | |
| B. | 第10纵行元素全部是金属元素 | |
| C. | 第3纵行元素的种类最多 | |
| D. | 只有第2纵行元素的原子最外层有2个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食醋的主要成分是醋酸,它是一种弱酸 | |
| B. | 苯酚有毒,但可用于杀菌消毒 | |
| C. | 聚乙烯塑料制品可用于食品的包装 | |
| D. | 福尔马林可作食品的保鲜剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12C、13C、14C、石墨都是碳元素的同位素 | |
| B. | 同种元素的原子,质量数一定相同 | |
| C. | 互为同位素的原子,质子数一定相同 | |
| D. | 由一种元素组成的物质,一定是纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
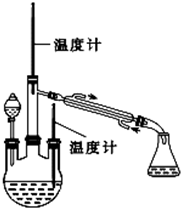 肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4•H2O).
肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4•H2O).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ④⑤⑥ | C. | ①③④ | D. | ②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
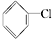 ②
②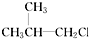 ③(CH3)3CCH2Cl ④CHCl2CHBr2⑤
③(CH3)3CCH2Cl ④CHCl2CHBr2⑤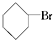 ⑥CH3Cl.
⑥CH3Cl.| A. | 全部 | B. | ②③⑤ | C. | ①③⑥ | D. | ②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com