
根据原子结构及元素周期律的知识,下列推断正确的是( )
A. 同主族元素含氧酸的酸性随核电荷数的增加而减弱
B. 核外电子排布相同的微粒化学性质也相同
C. Cl-、S2-、Ca2+、K+半径逐渐减小
D. 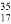 Cl 与
Cl 与 Cl 得电子能力相同
Cl 得电子能力相同
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2017届河北省张家口市高三第一学期期末教学质量监测化学试卷(解析版) 题型:推断题
A是重要的有机合成中问体,以A为原料合成香料M和线型高分子树脂N的路线如图所示(部分反应条件和物质略去):
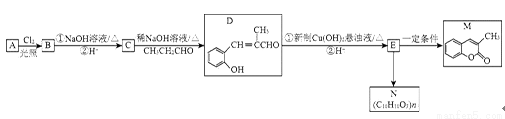
已知:
①A是芳香烃的含氧衍生物,其蒸气密度是相同条件下氢气密度的54倍。
②有机物分子中,同一个碳原子上连接两个—OH不稳定,会自动失水。
③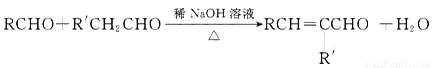 (R、R′表示烃基或氢原子)。
(R、R′表示烃基或氢原子)。
请回答:
(1)A的化学名称为________。N的结构简式为________。
(2)D中含氧官能团的名称为________。C的分子中最多有________个原子共平面。
(3)B→C时,第一步转化的反应类型为________。
(4)E→M的化学方程式为________。
(5)L是D的一种同系物,比D少1个碳原子且存在顺反异构;核磁共振氢谱中有6种吸收峰。则L的顺式结构简式为________。
(6)同时满足下列条件的E的同分异构体有________种(不考虑立体异构),任写其中一种的结构简式________。
①苯环连有两个取代基
②能发生银镜反应
③能与NaHCO3反应生成CO2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省南昌市、洪都中学、麻丘中学、十七中、桑海中学高二3月联考化学试卷(解析版) 题型:选择题
25℃时,某溶液中由水电离出的c(OH﹣)=1×10﹣13mol/L,该溶液中一定不能大量共存的离子组是
A. NH4+、Fe3+、SO42-、Cl- B. HCO3-、Na+、HSO3-、K+
C. Na+、SO42-、NO3-、Cl- D. CO32-、PO43-、K+、Na+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省枣庄市北校区高一下学期第一次月考化学试卷(解析版) 题型:填空题
下表是元素周期表的一部分,回答下列有关问题:

(1)在这些元素中,最活泼的金属元素和最活泼的非金属元素分别是____、______。(用元素符号作答)
(2)在这些元素的最高价氧化物对应水化物中,有一种呈两性的用来治疗胃酸过多反应的化学方程式______。
(3)在这些元素中,某元素的最高价氧化物对应的水化物可以和其气态氢化物反应,写出该化学方程式________。
(4)在⑤与④中,设计简单的实验(只要写出实验方案即可),证明其金属性的强弱,方案_______。
(5)如何验证元素⑦与⑧的非金属性强弱,写出可以验证该结论的一个离子反应方程式__________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省枣庄市北校区高一下学期第一次月考化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族。下列叙述中正确的是
A. 元素X的简单气态氢化物的热稳定性比W的强
B. 元素W的最高价氧化物对应水化物的酸性比Z的弱
C. 化合物YX、ZX2、WX3中化学键的类型相同
D. 原子半径的大小顺序:rY>rZ>rW>rX
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省枣庄市北校区高一下学期第一次月考化学试卷(解析版) 题型:选择题
依据元素周期表及元素周期律,下列推断正确的是
A. H3BO3的酸性比H2CO3的强
B. Mg(OH)2的碱性比Be(OH)2的强
C. HCl、HBr、HI的热稳定性依次增强
D. 若M+和R2-的核外电子层结构相同,则原子序数:R>M
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省枣庄市北校区高一下学期第一次月考化学试卷(解析版) 题型:选择题
已知碳有三种常见的同位素:12C、13C、14C,氧也有三种同位素:16O、17O、18O,由这六种原子构成的二氧化碳分子最多有
A. 18种 B. 6种 C. 9种 D. 12种
查看答案和解析>>
科目:高中化学 来源:2017届内蒙古赤峰市宁城县高三一模理科综合化学试卷(解析版) 题型:简答题
氮是地球上含量丰富的一种元素,“固氮”在工农业生产中有着重要作用,是几百年来科学家一直研究的课题。下表列举了不同温度下大气固氮和工业固氮的部分K值。
反应 | 大气固氮 N2(g)+O2(g) | 工业固氮 N2(g)+3H2(g) | |||
温度/℃ | 27 | 2000 | 25 | 400 | 450 |
K | 3.84×10-31 | 0.1 | 5×10-8 | 2×104 | 7×103 |
(1)①分析数据可知:大气固氮反应属于___________(填“吸热”或“放热”)反应。
②在一定温度下,将一定足的N2和O2通入到体积为1L的密闭容器中,当“大气固氮”反应达到平衡后,改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是_______。
a.增大压强 b.增大反应物的浓度 c.使用催化剂 d.升高温度
③ 从分子结构角度解释“大气固氮”和“工业固氮”反应的活化能都很高的原因:________。
(2)分析表格数据可知“大气固氮”的反应正向进行的程度小,不适合大规模生产,故世界各国均采用合成氨的方法进行工业固氮。
①从平衡移动角度考虑,工业固氮应该选择常温条件,但实际工业生产却选择500℃左右的高温,解释其原因_______________________。
②将0.1molN2和0.1molH2通入一容积可变的容器中进行工业固氮反应,则下图所示N2的平衡转化率在不同压强(P1,P2)下随温度变化的曲线正确的是____________(填“A” 或“B”);比较P1、P2的大小关系________;若300℃、压强P2时达到平衡,容器容积恰为100L,则此状态下反应的平衡常数K=______________ (计算结果保留2位有效数字)。

③合成氨反应达到平衡后,t1时刻氨气浓度欲发生图C变化可采取的措施是____________。

(3)近年近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,反应原理为:2N2(g)+6H2O(l)?4NH3(g)+3O2(g),则其反应热△H=____________。
(已知:N2(g)+3H2(g)?2NH3(g) △H1=-92.4kJ•mol-1;2H2(g)+O2(g)?2H2O(l) △H2=-571.6kJ•mol-1 )
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二2月联考化学试卷(解析版) 题型:选择题
2016年全国环境保护工作会议提出要“以改善环境质量为核心,实行最严格的环境保护制度,打好大气、水、土壤污染防治三大战役,确保2020年生态环境质量总体改善”。下列有关环境保护的说法中,正确的是
A. 纽扣银锌电池体型小,含有害物质少,用后可以随意丢弃
B. 化石燃料完全燃烧不会造成大气污染
C. 将煤气化后再燃烧可减少大气污染
D. “低碳”生活倡导节能减排,应禁止使用化石燃料,减少污水排放
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com