
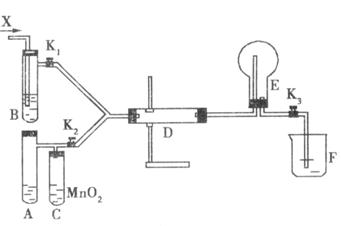
(1)实验前如何一次性检查BDEAC连接装置的气密性:___________________________。
(2)甲同学利用BDEF装置进行的实验,开关操作为打开_________,则B试管中通入的X是_________,发生反应时D管中的化学方程式为__________________。乙同学实验时选择与甲同学不同的试剂,然后打开K2、K3,则C管装入的液体是_________。为使实验成功A中除加入一种浓氨水外还需加入一种常见的氧化物(固体)为_________。其化学方程式为______
________________。
(3)甲、乙两同学的实验,在证明氨气具有还原性的现象时在E处有时会可观察到白烟,原因是__________________________________________________________________。
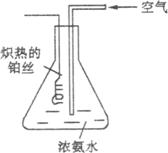
(4)丙同学总结甲、乙同学的实验特点,设计出更简单的实验来证明氨的还原性。如下图所示。
请简单说明操作原理。
(1)打开K1、K2,在B试管中加入适量的水并浸没管的下口,用酒精灯或热水浴给A试管微微加热,若B中的管内均形成水柱,并稳定不下降,说明装置气密性良好(其他合理答案均可)
(2)K1、K3 空气 4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
H2O2 CaO NH3·H2O+CaO====Ca(OH)2+NH3![]()
(3)氨气被氧化的产物中有NO、氨气、氧气、水汽存在,所以NO被氧化为NO2,NO2与水反应生成硝酸,硝酸再与氨反应产生白烟
(4)如图所示,通过导管向锥形瓶里不断鼓入空气,然后将红热的铂丝伸入锥形瓶中(不接触氨水)。可观察到铂丝保持红热,瓶中有红棕色气体产生。说明氨气被氧化为NO,最后被氧化为NO2


科目:高中化学 来源: 题型:
甲、乙两同学分别设计了如图所示的两套实验装置(所取的铁粉均为a g):

请回答下列问题:
(一)装置的评价
(1)在水蒸气的生成装置中乙同学在烧瓶底部放置了几片碎瓷片,其作用是___________;
(2)在反应装置中甲同学在硬质玻璃管中放入的是还原铁粉和石棉绒,石棉绒的作用是___
__________________;
(3)在收集装置中甲同学用的是排水集气法,这种方法存在的安全隐患是___________。
(二)实验过程
(4)甲同学可以证明两者发生反应的现象是______________________;
(5)从反应物元素的种类分析,生成的气体可能是氢气,进一步验证的方法是_________;
(6)当玻璃管中的铁粉充分反应后,停止实验,称量反应后固体产物质量为b,则固体产物的化学式为___________(用字母表示)。
(三)问题讨论
(7)酒精灯和酒精喷灯点燃的顺序是_____________。
(8)为了防止甲中气体收集装置发生的安全问题,可以在不增减仪器种类、数量,不改变其连接方式的前提下进行简单的改造,请在甲中画出你改造之处的示意图。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
某校兴趣小组对氢氧化钠溶液和稀盐酸混合后的有关问题,进行了如下探究:
Ⅰ.(1)甲同学为了证明氢氧化钠溶液与稀盐酸能够发生反应,设计并完成了如图所示
实验。
X溶液是 ,滴入的量一般为 。
(2)乙同学也设计完成了另一个实验,证明氢氧化钠溶液与盐酸能够发生反应。在盛有氢氧化钠溶液的试管中,用胶头滴管慢慢滴入稀盐酸,不断振荡溶液,同时测定溶液的pH,直至盐酸过量。
①写出测定溶液pH的方法: 。
②上图中哪个图像符合该同学的记录 (填序号)。
(3)你认为甲、乙两位同学的实验中, (填“甲同学”、“乙同学”或“甲、乙两同学”)的实验能充分证明氢氧化钠溶液与盐酸发生了反应,请说明理由: 。
Ⅱ.丙同学测出10mL 10%的NaOH溶液和不同体积的10%的盐酸溶液混合过程中,溶液的温度变化见下表(假设两溶液密度相同)。
| 加入盐酸的 体积( | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 |
| 溶液温度上升 | 5.2 | 9.6 | 12.0 | 16.0 | 18.2 | 16.7 | 15.7 | 14.7 | 13.7 |
就此实验回答:
(4)盐酸和氢氧化钠的反应是 (填“吸热”或“放热”)反应。
(5)请在图中绘制出溶液的温度上升与加入盐酸体积之间的变化关系图,并在曲线上画出能表示两者之间恰好完全反应的点,并用字母P表示。
Ⅲ.丁同学为测定标示质量分数为32%的盐酸的实际质量分数,用pH测定仪组成实验装置。实验时先在烧杯中加入20g 40%的氢氧化钠溶液,再逐滴加入该盐酸,pH测定仪打印出加入盐酸的质量与烧杯中溶液的pH关系如图所示。
(6)请以此次测定的结果为依据计算该盐酸的实际质量分数为 。
(7)请分析你的计算结果与标签标示的质量分数不一致的可能原因(若一致,此空可不填): 。
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古巴市高一上学期期末考试化学试卷(解析版) 题型:实验题
某课外活动小组的同学在实验室做锌与浓硫酸反应的实验时,甲同学认为产生的气体是二氧化硫;而乙同学认为除二氧化硫气体外,还可能产生氢气。为了验证甲、乙两同学的判断是否正确,丙同学设计了如图所示的实验装置(锌与浓硫酸共热时产生的气体为X,且该反应装置已略去):

试回答:
(1)上述实验中生成二氧化硫气体的化学反应方程式为
_________________________________________________________。
(2)乙同学认为还可能产生氢气的理由是____________________ _____________________________________。
(3)丙同学在安装好装置后,必不可少的一步操作___________________________________________。
(4)B中加入的试剂是________,其作用是___________________ _____________________________________。
(5)可以证明气体X中含有氢气的实验现象是:C中________,D中________。如果撤去装置B,是否还能根据D中的现象判断气体X中含有氢气?
答: ___________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年湖北省高三5月模拟(理综)化学部分 题型:填空题
某校兴趣小组对氢氧化钠溶液和稀盐酸混合后的有关问题,进行了如下探究:
Ⅰ.(1)甲同学为了证明氢氧化钠溶液与稀盐酸能够发生反应,设计并完成了如图所示
实验。
X溶液是 ,滴入的量一般为 。
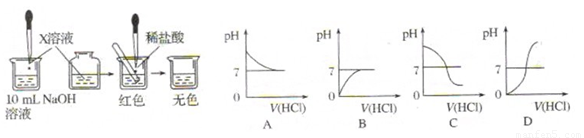
(2)乙同学也设计完成了另一个实验,证明氢氧化钠溶液与盐酸能够发生反应。在盛有氢氧化钠溶液的试管中,用胶头滴管慢慢滴入稀盐酸,不断振荡溶液,同时测定溶液的pH,直至盐酸过量。
①写出测定溶液pH的方法: 。
②上图中哪个图像符合该同学的记录 (填序号)。
(3)你认为甲、乙两位同学的实验中, (填“甲同学”、“乙同学”或“甲、乙两同学”)的实验能充分证明氢氧化钠溶液与盐酸发生了反应,请说明理由: 。
Ⅱ.丙同学测出10mL 10%的NaOH溶液和不同体积的10%的盐酸溶液混合过程中,溶液的温度变化见下表(假设两溶液密度相同)。
|
加入盐酸的 体积( |
2 |
4 |
6 |
8 |
10 |
12 |
14 |
16 |
18 |
|
溶液温度上升 |
5.2 |
9.6 |
12.0 |
16.0 |
18.2 |
16.7 |
15.7 |
14.7 |
13.7 |
就此实验回答:
(4)盐酸和氢氧化钠的反应是 (填“吸热”或“放热”)反应。
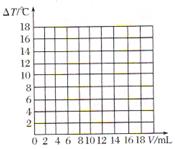
(5)请在图中绘制出溶液的温度上升与加入盐酸体积之间的变化关系图,并在曲线上画出能表示两者之间恰好完全反应的点,并用字母P表示。
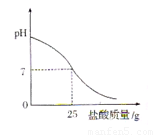
Ⅲ.丁同学为测定标示质量分数为32%的盐酸的实际质量分数,用pH测定仪组成实验装置。实验时先在烧杯中加入20g 40%的氢氧化钠溶液,再逐滴加入该盐酸,pH测定仪打印出加入盐酸的质量与烧杯中溶液的pH关系如图所示。
(6)请以此次测定的结果为依据计算该盐酸的实际质量分数为 。
(7)请分析你的计算结果与标签标示的质量分数不一致的可能原因(若一致,此空可不填): 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com