
| ||
| ||
| ||


科目:高中化学 来源: 题型:
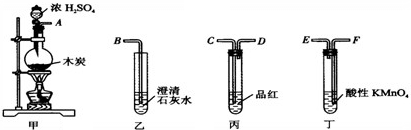
 合成氨工业对化学和国防工业具有重要意义.
合成氨工业对化学和国防工业具有重要意义.
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
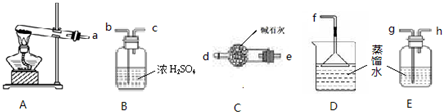
| 催化剂 |
| 高温高压 |
| c2(NH3) |
| c(N2)?c3(H2) |
| c2(NH3) |
| c(N2)?c3(H2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
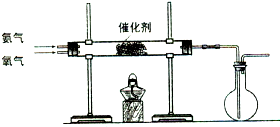 某课外小组在实验室制备氨气,并进行有关氨气的性质探究.
某课外小组在实验室制备氨气,并进行有关氨气的性质探究.查看答案和解析>>
科目:高中化学 来源: 题型:
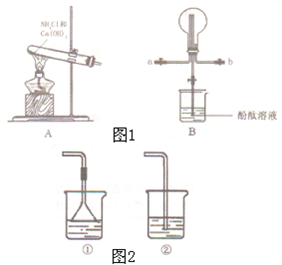 某化学实验小组同学利用如图1装置制备氨气,并探究氨气的性质(部分仪器已略去).
某化学实验小组同学利用如图1装置制备氨气,并探究氨气的性质(部分仪器已略去).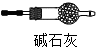 乙:
乙: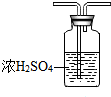 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com