
| A. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| B. | 100g质量分数为98%的浓硫酸中所含氧原子数为4NA | |
| C. | 常温常压下,92gNO2N2O4的混合气体含有的原子数为6NA | |
| D. | 44gN2O和CO2组成的混合气体中含有NA个分子 |
分析 A、NO2和CO2中均含2个氧原子;
B、浓硫酸中除了硫酸本身,水也含氧原子;
C、NO2和N2O4的最简式均为NO2;
D、N2O和CO2的摩尔质量均为44g/mol.
解答 解:A、NO2和CO2中均含2个氧原子,故当分子总数为NA个时,所含的氧原子的个数为2NA个,故A正确;
B、浓硫酸中除了硫酸本身,水也含氧原子,故溶液中的氧原子的个数大于4NA个,故B错误;
C、NO2和N2O4的最简式均为NO2,故92g混合物中含有的NO2的物质的量为2mol,则含6mol原子即6NA个,故C正确;
D、N2O和CO2的摩尔质量均为44g/mol,故44g混合物的物质的量为1mol,故含NA个分子,故D正确.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:选择题
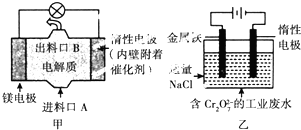
| A. | 图乙中Cr2O72-向惰性电极移动,与该极近的OH-结合转化成Cr(OH)3除去 | |
| B. | 图乙的电解池中,有0.084 g阳极材料参与反应,阴极会有336 mL的气体产生 | |
| C. | 图甲中发生的还原反应是Mg2++ClO-+H2O+2e-═Cl-+Mg(OH)2↓ | |
| D. | 若图甲中3.6 g镁溶液产生的电量用以图乙废水处理,理论可产生10.7 g氢氧化铁沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钻木取火 | |
| B. | 青铜器生锈 | |
| C. | 焰色反应检验Na+ | |
| D. | 2015年9月3日,中国在抗日战争暨世界反法西斯战争胜利70周年之际,燃放烟花爆竹,举国欢庆 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2 (g)+NaOH(aq)═NaHCO3(aq)△H=-(2y-x)kJ•mol-1 | |
| B. | CO2 (g)+NaOH(aq)═NaHCO3(aq)△H=-(2x-y) kJ•mol-1 | |
| C. | CO2 (g)+NaOH(aq)═NaHCO3(aq)△H=-(4x-y) kJ•mol-1 | |
| D. | 2CO2 (g)+2NaOH(aq)═2NaHCO3(aq)△H=-(8x-y) kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HNO3+KOH═KNO3+H2O | B. | 2HCl+Cu(OH)2═CuCl2+2H2O | ||
| C. | CH3COOH+NaOH═CH3COONa+H2O | D. | HCl+NH3•H2O═NH4Cl+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1mol/L | B. | 1.5mol/L | C. | 3mol/L | D. | 7mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
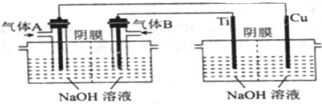 (1)工业上可利用CO2和H2生产甲醇,方程式如下:
(1)工业上可利用CO2和H2生产甲醇,方程式如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com