
【题目】常温下,将pH均为3,体积均为![]() 的HA和HB溶液,分别加水稀释至体积V,pH随
的HA和HB溶液,分别加水稀释至体积V,pH随![]() 的变化如图所示,下列叙述正确的是
的变化如图所示,下列叙述正确的是![]()
![]()
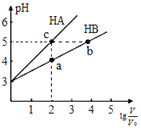
A.水的电离程度:![]()
B.溶液中离子总浓度:![]()
C.稀释相同倍数时:![]()
D.溶液中离子总物质的量:![]()
【答案】D
【解析】
根据图像当![]() 时,HA溶液的
时,HA溶液的![]() ,HB溶液的
,HB溶液的![]() ,HA为强酸,HB为弱酸。
,HA为强酸,HB为弱酸。
A.根据图像,溶液的pH:![]() ,酸溶液中
,酸溶液中![]() 全部来自水电离,水的电离程度:
全部来自水电离,水的电离程度:![]() ,故A错误;
,故A错误;
B.c点pH大于a点,c点溶液中![]() 点溶液中
点溶液中![]() ,溶液中离子总浓度:
,溶液中离子总浓度:![]() ,b、c点溶液的pH相等,b、c点两溶液中的电荷守恒分别为
,b、c点溶液的pH相等,b、c点两溶液中的电荷守恒分别为![]() 、
、![]() ,溶液中离子总浓度:
,溶液中离子总浓度:![]() ,溶液中离子总浓度:
,溶液中离子总浓度:![]() ,故B错误;
,故B错误;
C.根据图像,稀释相同倍数时,溶液的pH:![]() ,溶液中
,溶液中![]() ,故C错误;
,故C错误;
D.a、c点溶液体积相同,c点pH大于a点,c点溶液中![]() 点溶液中
点溶液中![]() ,溶液中离子总物质的量:
,溶液中离子总物质的量:![]() ,b点相对于a点加水稀释促进HB的电离,溶液中离子总物质的量:
,b点相对于a点加水稀释促进HB的电离,溶液中离子总物质的量:![]() ,溶液中离子总物质的量:
,溶液中离子总物质的量:![]() ,故D正确。
,故D正确。
故选D。


科目:高中化学 来源: 题型:
【题目】某课外活动小组对甲酸进行了如下的实验,以验证其含有醛基,并考察其化学性质。首先做了银镜反应:
(1)取少量甲酸加入NaOH溶液中和其酸性,反应的离子方程式为_________________。
(2)在(1)的溶液中加入足量银氨溶液,加热,产生了银镜。甲酸钠溶液与银氨溶液发生银镜反应的离子方程式为_______________________________________________。
(3)某同学很成功的做了银镜反应,他肯定没有进行的操作_________________(写字母):
A.用洁净的试管 B.向银氨溶液中加入硝酸酸化
C.用前几天配制好的银氨溶液 D.直接在银氨溶液里加入稍过量的甲酸;
E.在浓度为2%的NH3H2O中滴入稍过量的浓度为2%的硝酸银
然后,同学们对甲酸与甲醇的酯化反应进行了研究:
(4)写出![]() 和CH3-18OH进行酯化反应的化学方程式______________________。
和CH3-18OH进行酯化反应的化学方程式______________________。
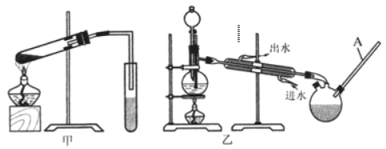
(5)你认为选择甲装置还是乙装置好?_______,原因是______________________。乙装置中长导管C的作用是_________________。
(6)实验中饱和碳酸钠溶液的作用是_____________________________。从饱和碳酸钠溶液中分离出酯需要用到的主要实验仪器是_______________。
(7)一同学用装有饱和氢氧化钠的三颈烧瓶接收甲酸甲酯,几乎没有收集到产物,请给予合理的解释_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计实验探究构成原电池的条件,装置如图所示:
甲. 乙.
乙.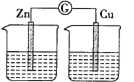
实验一:探究电极的构成。图甲中,①A、B两极均选用石墨作电极,发现电流计指针不偏转;②A、B两极均选用铜片作电极,发现电流计指针不偏转;③A极用锌片,B极用铜片,发现电流计指针向左偏转;④A极用锌片,B极用石墨,发现电流计指针向左偏转。
(1)结论一:________________________;
实验二:探究溶液的构成。图甲中,A极用锌片,B极用铜片,①液体采用无水乙醇,发现电流计指针不偏转;②改用硫酸溶液,发现电流计指针偏转,B极上有气体产生。
(2)结论二:________________________;
实验三:探究图乙装置能否构成原电池。将锌、铜两电极分别放入稀硫酸中,发现锌片上有气泡产生,铜片上无明显现象,电流计指针不发生偏转。
(3)结论三:________________________;
思考:对该同学的实验,有同学提出了如下疑问,请你帮助解决。
(4)在图甲装置中,若A为镁片,B为铝片,电解质溶液为![]() 溶液;负极为________(填“A”或“B”);电流计的指针应向________(填“右”或“左”)偏转。
溶液;负极为________(填“A”或“B”);电流计的指针应向________(填“右”或“左”)偏转。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某高分子材料的结构如图所示: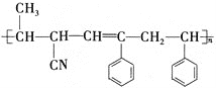 ,已知该高分子材料是由三种单体聚合而成的,以下与此高分子材料相关的说法正确的是
,已知该高分子材料是由三种单体聚合而成的,以下与此高分子材料相关的说法正确的是
A.合成该高分子的反应是缩聚反应
B.形成该高分子材料的单体![]() 中,所有原子可能处于同一平面内
中,所有原子可能处于同一平面内
C.三种单体中有两种有机物互为同系物
D.三种单体都可以使溴水褪色,但只有两种能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池是目前电池研究的热点之一。某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极下列叙述不正确的是( )

A.a极是负极,该电极上发生氧化反应
B.b极发生的电极反应是O2+4OH--4e-=2H2O
C.电池总反应方程式为2H2+O2=2H2O
D.氢氧燃料电池是一种具有应用前景的绿色电源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用“银-Ferrozine”法测室内甲醛含量的原理为:
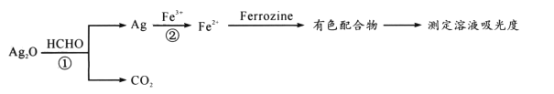
已知:吸光度与溶液中有色物质的浓度成正比
下列说法正确的是
A. 反应①中参与反应的HCHO为30g时转移电子2mol
B. 可用双氧水检验反应②后的溶液中是否存在Fe3+
C. 生成44.8 LCO2时反应②中参加反应的Ag一定为8mol
D. 理论上测得溶液吸光度越高,HCHO含量也越高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国劳伦斯·利弗摩尔国家实验室(LLNL)设计的以熔融的碳酸盐为电解液,泡沫镍为电极,氧化纤维布为隔膜的直接碳燃料电池结构如图所示,下列说法错误的是( )
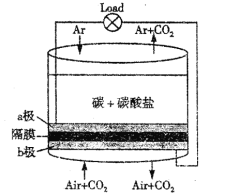
A. a极通气的目的是增强导电能力
B. a极的电极反应式为C+2CO32--4e-=3CO2↑
C. 电流由b极沿导线经负载再流向a极
D. CO32-由b极区透过隔膜流向a极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制氢气的一个重要反应是:CO(g)+H2O(g)=CO2(g)+H2(g)。
已知在25℃时:①C(s)+![]() O2(g)
O2(g)![]() CO(g) H4=-111kJ/mol
CO(g) H4=-111kJ/mol
②H2(g)+![]() O2(g)=H2(g) H2=-242kJ/mol
O2(g)=H2(g) H2=-242kJ/mol
③C(s)+O2(g)=CO2(g) H2=-394kJ/mol
下列说法不正确的是( )
A.25℃时,![]()
B.增大压强,反应①的平衡向逆反应方向移,平衡常数K减小
C.反应①达到平衡时,每生成![]() 的同时生成0.5molO2
的同时生成0.5molO2
D.反应②断开2molH2和1molO2中的化学键所吸收的能量比形成4molO-H键所放出的能量少484kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验问题处理方法正确的是( )
①用pH试纸测溶液pH时,将试纸用水润湿再蘸取待测液
②实验结束后,可将所有的废液倒入下水道排出实验室
③给试管中的液体加热时加入碎瓷片,以免暴沸伤人
④测定硫酸铜结晶水含量时,将晶体加热至白色,然后冷却、称重即可计算
⑤配制稀硫酸时,先在烧杯中加一定体积的水,再边搅拌边加入浓硫酸
A.①②B.③④⑤C.①③⑤D.③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com