
某元素R的原子序数小于18,该元素的原子得到1个电子后形成具有稀有气体元素原子的电子层结构的离子,该元素可形成含氧酸HRO3,下列说法中正确的是( )
①R元素的最高正价是+5价 ②R元素还可形成其他含氧酸 ③R元素原子的最外层电子数为7 ④R元素的原子序数为7
A.①② B.②③
C.③④ D.①④
 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
酒后驾车是引发交通事故的重要原因。交警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2O7酸性水溶液遇乙醇迅速生成蓝绿色的Cr3+。下列对乙醇的描述与此测定原理有关的是( )
①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性 ④乙醇是烃的含氧衍生物
A.②④ B.②③
C.①③ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
I.近年来全国各地都遭遇“十面霾伏”。其中,机动车尾气和燃煤产生的烟气对空气质量影响严重,这是目前重要的研究课题 。
(1)汽车尾气净化的主要原理为:2NO(g) + 2CO(g) 2CO2(g)+ N2(g) △H<0
2CO2(g)+ N2(g) △H<0
若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 (填代号)。(下图中υ正、K、n、w分别表示正反应速率、平衡常数、物质的量、质量分数)
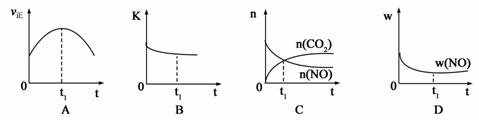
(2)机动车尾气和煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOX可以消除氮氧化物的污染。已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol
2NO2(g) N2O4(g) △H=-56.9 kJ/mol
N2O4(g) △H=-56.9 kJ/mol
H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式: 。
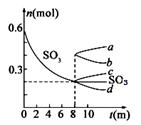 Ⅱ.利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关
Ⅱ.利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关
键步骤.T1℃时,在1L密闭容器中充入0.6molSO3,右图表
示SO3 物质的量随时间的变化曲线。
① 达到平衡时,用SO2表示的化学反应速率为 。
② 平衡时,SO3的转化率为 (保留小数点后一位);
T1℃时,反应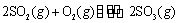 的
的
平衡常数为 ; 其他条件不变,在8min时压缩容器体积至0.5L,
则n(SO3)的变化曲线为 (填字母)。
③右表为不同温度(T)下,反应2SO2(g) + O2(g)  2SO3(g) (△H<0)
2SO3(g) (△H<0)
| T/℃ | T2 | T3 |
| K | 20.5 | 4.68 |
的化学平衡常数(K),由此推知,温度最低
的是 (填“T1”、“T2” 或 “T3)
查看答案和解析>>
科目:高中化学 来源: 题型:
某校课外活动小组为探究铜与稀硝酸反应产生的气体主要是NO,设计了下列实验。图中K为止水夹,F是装有一半空气的注射器,其中加热装置和固定装置均已略去。
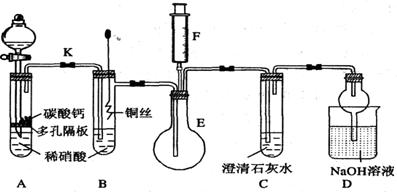
请回答有关问题:
(1)设计装置A的目的是 。
(2)在完成装置A的实验目的后,关闭K,再将装置B中的铜丝插入稀硝酸。 B中反应的离子方程式是 。
(3)将F中的空气推入E中,证明NO存在的实验现象是 ,此过程发生反应的化学方程式是 。
(4)装置D中NaOH溶液的作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
有X、Y、Z三种金属,把它们放在稀硫酸中,只有Y溶解放出气体。将Z放入X的盐溶液中,有X金属析出。已知X、Y、Z在化合物中均显+2价,则下列结论正确的是( )
A.金属性:Z>Y>X
B.还原性:X>Y>Z
C.氧化性:X2+>Z2+>Y2+
D.氧化性:X2+>Y2+>Z2+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述不正确的是( )
A.HClO4比H2SO4的酸性强,说明氯的非金属性比硫强
B.H3PO4为三元酸,H2SO4为二元酸,可推知磷的非金属性比硫强
C.HCl比HBr稳定,可推知非金属性氯大于溴
D.SiH4能自燃,H2S在300 ℃分解,说明硫的非金属性比硅强
查看答案和解析>>
科目:高中化学 来源: 题型:
根据碘与氢气反应的热化学方程式:
(ⅰ)I2(g)+H2(g)2HI(g)
ΔH=-9.48 kJ·mol-1
(ⅱ)I2(s)+H2(g)2HI(g)
ΔH=+26.48 kJ·mol-1
下列判断正确的是( )
A.254 g I2(g)中通入2 g H2(g),反应放热9.48 kJ
B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ
C.反应(ⅰ)的产物比反应(ⅱ)的产物稳定
D.反应(ⅱ)的反应物总能量比反应(ⅰ)的反应物总能量低
查看答案和解析>>
科目:高中化学 来源: 题型:
火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染。对燃烧废气进行脱硝、脱碳和脱硫等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝:利用甲烷催化还原NO2:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g)
ΔH=-574 kJ·mol-1
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g)
ΔH=-1 160 kJ·mol-1
甲烷直接将NO2还原为N2的热化学方程式为________________
_________________________________________________________。
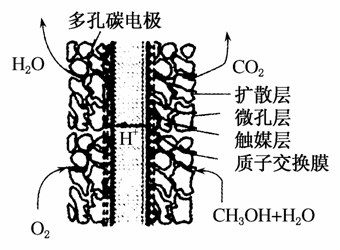
(2)某一甲醇燃料电池的结构如图所示。其工作时负极的电极反应式可表示为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
A是一种重要的化工原料,A的产量可以用来衡量一个国家的石油化工水平,E是具有果香气味的烃的衍生物。A、B、C、D、E在一定条件下存在如下转化关系(部分反应条件、产物被省略)。
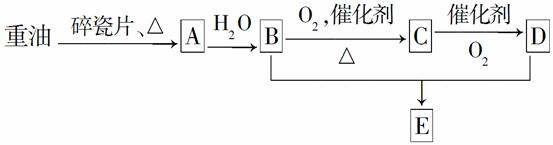
(1)工业上,由石油获得重油的方法是________,由重油获得A是________变化(填“物理”或“化学”)。A的名称为________。
(2)A—→B的反应类型是________;E的结构简式为________;写出C—→D的化学方程式:____________________________________。
(3)丁烷是由重油获得A的过程中的中间产物之一,写出它的两种同分异构体的结构简式:________________________________________,________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com