
分析 (1)依据配制溶液体积选择合适规格容量瓶;
(2)依据m=CVM计算需要溶质的质量;
(3)依据配制过程中溶解、移液操作时玻璃棒作用解答;
(4)定容时若俯视刻度线,导致溶液体积偏小,依据c=$\frac{n}{V}$进行误差分析;
(5)氢氧化钠能够吸收空气中的水和二氧化碳,依据c=$\frac{n}{V}$进行误差分析;
(6)定容时若加水超过刻度线,导致溶液体积偏小,依据c=$\frac{n}{V}$进行误差分析;
解答 解:(1)实验室需要0.2mol/L NaOH溶液480ml,实验室没有480mL容量瓶,应选择500mL容量瓶;
故答案为:500;
(2)配制0.2mol/L NaOH溶液500ml,需要溶质的质量m=0.2mol/L×40g/mol×0.5L=4.0g;
故答案为:4.0;
(3)配制过程中溶解时用玻璃棒搅拌加速固体溶解、移液操作时用玻璃棒引流;
故答案为:引流;
(4)定容时若俯视刻度线,导致溶液体积偏小,依据c=$\frac{n}{V}$可知,溶液浓度偏大;
故答案为:偏大;
(5)若称量NaOH固体的时间过长,因为氢氧化钠固体吸收空气中水、二氧化碳,导致称取的固体含有氢氧化钠的物质的量偏小,依据c=$\frac{n}{V}$可知,溶液浓度偏小;
故答案为:偏小;
(6)定容时若加水超过刻度线,导致溶液体积偏小,依据c=$\frac{n}{V}$可知,溶液浓度偏小;
故答案为:偏小.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理和操作步骤是解题关键,注意误差分析的方法,题目难度不大.


科目:高中化学 来源: 题型:填空题
 (1)已知在常温常压下:
(1)已知在常温常压下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:1 | B. | 5:1 | C. | 7:2 | D. | 8:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与浓硫酸共热消去 | B. | 与浓氢溴酸卤代 | ||
| C. | 铜催化氧化 | D. | 与戊酸催化酯化 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 二甲苯一溴水代物熔点(℃) | 234 | 206 | 213.8 | 204 | 211.5 | 205 |
| 对应二甲苯熔点(℃) | 13.3 | -47.9 | -25.2 | -47.9 | -25.2 | -47.9 |
| A. | 熔点234℃的一溴二甲苯是一溴对二甲苯 | |
| B. | 熔点204℃的一溴二甲苯是一溴邻二甲苯 | |
| C. | 熔点-47.9℃的二甲苯是对二甲苯 | |
| D. | 熔点205℃的一溴二甲苯是一溴间二甲苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
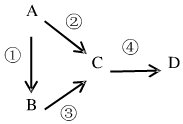 A、B、C、D均为中学化学常见物质,且均含有同一种元素,它们之间有如图转化关系,其中A是单质.
A、B、C、D均为中学化学常见物质,且均含有同一种元素,它们之间有如图转化关系,其中A是单质.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铁通常用作红色油漆和涂料 | |
| B. | 用铝制餐具长期存放碱性食物 | |
| C. | 过氧化钠可以用作潜水艇里氧气的来源 | |
| D. | 硅可用于制作电脑芯片 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com