
【题目】制取乙烯时,常因温度过高而发生副反应,部分乙醇跟浓H2SO4 反应生成SO2,CO2,水蒸气和炭黑。
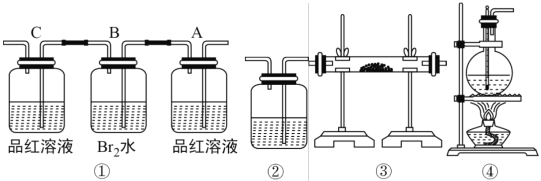
(1)用编号为①→④的实验装置设计一个实验,以验证上述反应混合气体中含CO2,SO2和水蒸气。写出装置的连接顺序(按产物气流从左到右的流向填写编号):______。
(2)实验的装置①中 A 瓶的现象是______;结论为__________。 B 瓶中的现象是__________; B 瓶溶液作用为__________。若 C 瓶中品红溶液不褪色,可得到结论为__________。
(3)装置③中加的固体药品是______以验证混合气体中有______。装置②中盛的溶液是_____以验证混合气体中有______。
(4)简述装置①在整套装置中位置的理由__________。
【答案】④③①② 品红溶液褪色 气体中含有SO2 溴水颜色变浅 将SO2完全吸收 混合气体中已经没有SO2 无水CuSO4 水蒸气 澄清石灰水 验证CO2的存在 ①要在③之后,否则气流会带出水蒸气,干扰水的检验,①要在②之前,否则SO2也会使石灰水变浑浊,干扰CO2的检验。
【解析】
在装置④中进行浓硫酸与乙醇混合加热制取乙烯的反应,制取得到的气体中含有SO2,CO2,水蒸气,根据水蒸气检验用无水硫酸铜,二氧化硫的检验用品红溶液,二氧化碳的检验用澄清石灰水,而二氧化碳、二氧化硫都能使澄清石灰水变浑浊,水蒸气检验一般放在最前面,接着检验二氧化硫,最后检验二氧化碳,同在检验二氧化碳之前用溴水除去SO2,再通过品红溶液不褪色确认SO2已除干净,最后用澄清石灰水检验二氧化碳。
(1)检验二氧化硫用品红溶液,检验二氧化碳用澄清的石灰水,检验水蒸气用无水硫酸铜,因溶液中有水,所以要先检验水蒸气,然后检验二氧化硫,同在检验二氧化碳之前用溴除尽SO2,再通过品红溶液不褪色确认SO2已除干净后再检验CO2气体,故装置连接序号为④③①②;
(2)实验的装置①中A瓶装的是品红溶液,当混合气体通过A瓶时,品红溶液褪色,说明产物中有二氧化硫;B瓶的溴水能和二氧化硫反应产生硫酸和氢溴酸,将SO2除去,所以二氧化硫能被溴水吸收,当混合气体再次通过C瓶的品红不褪色时,说明品红已全部被吸收;
(3)装置③的作用为检验水蒸气的存在,可根据白色无水硫酸铜与水反应产生硫酸铜晶体,物质的颜色由白色变为蓝色,说明有水蒸气存在,装置②的作用为检验二氧化碳的存在,当澄清石灰水变浑浊,说明有二氧化碳存在;
(4)因溶液中有水必须先检验水蒸气,所以①要在③之后,否则气流会带出水蒸气,干扰水的检验;二氧化碳和二氧化硫都能使澄清的石灰水变浑浊,二氧化硫能使品红褪色,二氧化碳不能,所以①要在②之前。


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】乙烯是重要的有机化工原料,以下是以乙烯为原料制备的常见有机物的示意图:
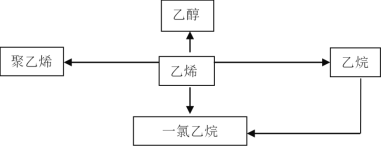
(1)乙烯的电子式为________________,其同系物的通式为_____________。
(2)工业上用乙烯制备乙醇的化学方程式为____________________________。
(3)聚乙烯薄膜常用作食品包装材料,写出由乙烯制聚乙烯的化学方程式:_______,此反应类型为_______反应。
(4)制备一氯乙烷常有两种方法:①用乙烷与氯气在光照条件下反应制取;②用乙烯在加热使用催化剂的条件下与氯化氢气体反应制取。比较两种制备方法,你认为比较好是哪一种?___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关原子结构与性质的说法正确的是( )
A.![]() 的基态原子的第一电离能依次递增
的基态原子的第一电离能依次递增
B.![]() 的基态电子排布式为
的基态电子排布式为![]()
C.![]() 有6种不同能量的电子
有6种不同能量的电子
D.化合物![]() 中S元素显-2价,说明C元素比S元素的电负性弱
中S元素显-2价,说明C元素比S元素的电负性弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种双室微生物燃料电池,以苯酚(C6H6O)为燃料,同时消除酸性废水中的硝酸盐的装置示意图如图1所示; 研究人员发现的一种“水”电池,其总反应为:5MnO2 +2Ag+2NaCl=Na2Mn5Ol0+2AgCl,用该“水”电池为电源电解NaCl溶液的实验装置如图2所示,电解过程中X电极上有无色气体逸出。下列说法正确的是( )
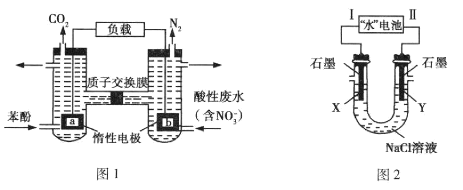
A.图1装置中若右池产生0.672 L气体(标准状况下),则电路中通过电子0.15 mol
B.图1装置中左池消耗的苯酚与右池消耗的![]() 的物质的量之比为28:5
的物质的量之比为28:5
C.图2装置的电路中每通过1 mol e-,U形管中消耗0.5 mol H2O
D.图2装置中“水”电池内每生成1 mol Na2Mn5O10,X电极上生成1 mol气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向25 mL 0.100 0 mol L-l的BOH溶液中逐滴滴入同浓度的一元弱酸HA的溶液,所得溶液PH与加入HA溶液的体积的关系曲线如图所示,则下列说法正确的是( )
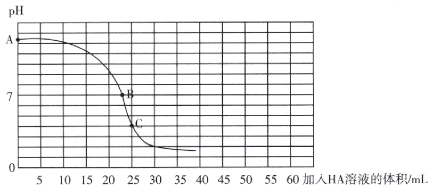
A.BOH的电离方程式为BOH =B++OH-
B.可选择酚酞作指示剂,滴定终点时,溶液恰好在B点从无色变为粉红色,且30秒内不恢复原色
C.Ka(HA)<Kb(BOH)
D.加入HA溶液的体积为50 ml时,c(B+)+2c(BOH)+c(OH-)=c(HA)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于Na2CO3 与NaHCO3的性质判断正确的是![]()
![]()
A.常温下溶解度:Na2CO3<NaHCO3
B.热稳定性:Na2CO3<NaHCO3
C.与同浓度盐酸反应的剧烈程度:Na2CO3>NaHCO3
D.与澄清石灰水反应,均有白色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳的捕集和转化是科学研究中的热点问题。我国科研人员提出了以Ni/Al2O3为催化剂,由 CO2(g)和H2(g)转化为CH4(g)和H2O(g)的反应历程,其示意图如下:
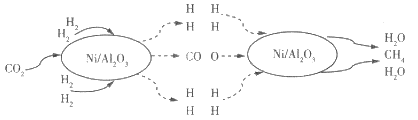
(1)该可逆反应的化学方程式为_________。使用催化剂Ni/Al2O3_________ (填“能”或“不能”)提髙CO2的平衡转化率。
(2)300℃下,在一恒容密闭容器中充入一定量的CO2与H2,发生上述反应,一段时间后反应达平衡,若其他条件不变,温度从300℃升至500℃,反应重新达到平衡时,H2的体积分数增加。下列说法错误的是_________(填标号)。
A.该反应的![]()
B.平衡常数大小:![]()
C.300℃下,减小![]() 的值,
的值,![]() 的平衡转化率升高
的平衡转化率升高
D.反应达到平衡时化![]()
(3)在一定条件下,反应体系中CO2的平衡转化率a( CO2)与L和X的关系如图所示,L和X表示温度或压强。
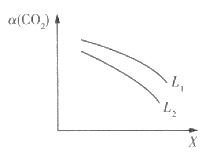
①X表示的物理量是___________。
②L1_____________L2(填“<”“>”),判断理由是______________________________________。
(4)向1 L恒容密闭容器中加入4.0 mol H2(g),1.0 mol CO2,控制条件(催化剂为 Ni/AI2O3、温度为T1)使之发生上述反应,测得容器内气体的压强随时间的变化如图所示。
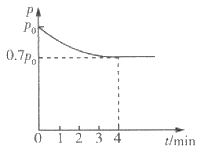
①4 min时CO2的转化率为___________。
②T1温度下该反应的化学平衡常数为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸钴可用于制备有机合成中间体。一种以铜钴矿为原料,生产草酸钴晶体(CoC2O4·2H2O)的工艺流程如图:

已知:①“浸出”液含有的离子主要有H+、Fe3+、Cu2+、Co2+、SO42-;
②pH增大,Fe2+被氧化的速率加快,同时生成的Fe3+水解形成更多的胶体;
③25℃时,Ksp[Co(OH)2]=1.6×10-15。
(1)①生产时为提高铜钴矿粉浸出率,常采取的措施有___(填字母)。
a.高温浸出 b.适当延长浸出时间 c.分批加入细菌浸取液并搅拌
②铜钴矿粉也可采用在90℃、酸性条件下,加入适当还原剂进行浸出。若用Na2SO3为还原剂,浸出钴的主要化学反应为Co2O3+2H2SO4+Na2SO3![]() 2CoSO4+2H2O+Na2SO4。除考虑成本因素外,还原剂不选用浸出率更高的NaNO2的原因是___。
2CoSO4+2H2O+Na2SO4。除考虑成本因素外,还原剂不选用浸出率更高的NaNO2的原因是___。
(2)“萃取”步骤中萃取除去的主要金属阳离子是___。
(3)“氧化”过程中,控制70℃、pH=4条件下进行,pH对除铁率和钴回收率的影响如图所示。
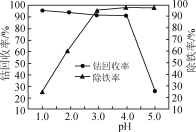
①“氧化”过程的离子方程式为___。
②pH为4~5时,钴的回收率降低的原因是___。
(4)300℃时,在空气中煅烧CoC2O4·2H2O可制得CO3O4,该反应的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO溶液是一种纺织工业用漂白剂,可用一定比例NaOH、Na2CO3的混合溶液和Cl2反应制备。
(1)NaHCO3的存在能增强NaClO溶液的稳定性。Cl2与混合溶液中Na2CO3反应制备NaClO,同时生成NaHCO3,其化学方程式为___。
(2)NaClO溶液中若含有NaClO3会影响产品的品质。测定碱性NaClO样品中NaClO3物质的量浓度的方法如下:取20.00mLNaClO溶液试样,加入过量H2O2,充分反应后,加热煮沸,冷却至室温,加入硫酸酸化,再加入0.1000mol·L-1FeSO4标准溶液30.00mL,充分反应后,用0.01000mol·L-1酸性K2Cr2O7溶液滴定过量的FeSO4溶液至终点(Cr2O72-被还原为Cr3+),消耗该溶液25.00mL。
已知:ClO3-在碱性条件下性质稳定,在酸性条件下表现出强氧化性;ClO3-+Fe2++H+—Cl-+Fe3++H2O(未配平)。
①加入过量H2O2的目的是__。
②实验中若缺少加热煮沸步骤,所测NaClO3物质的量浓度会有较大误差,原因可能是___(答出一个即可)。
③计算样品中NaClO3物质的量浓度___(写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com