
下列说法中正确的是
A.由不同原子构成的纯净物一定是化合物 B.非金属氧化物一定是酸性氧化物
C.含金属元素的离子一定都是阳离子 D.胆矾是纯净物,水泥是混合物
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2016届吉林省扶余市高三上学期第一次月考化学试卷(解析版) 题型:实验题
(12分)某兴趣小组拟制备K3[Fe(C2O4)3]·3H2O晶体
Ⅰ.查阅资料
K3[Fe(C2O4)3]·3H2O是翠绿色晶体,易溶于水,难溶于乙醇,具有光敏性,光照分解。
110℃失去结晶水,230℃时分解。K3[Fe(C2O4)3]·3H2O的摩尔质量是491g/moL
Ⅱ.制备产品
实验步骤如下:
① 取27.8gFeSO4·7H2O和K2C2O4反应生成草酸亚铁
② 将草酸亚铁(FeC2O4)和适量K2C2O4的混合溶液置于40℃的恒温水浴中,逐滴加入 6% H2O2,边加边搅拌,使Fe2+充分被氧化。反应体系中生成K3[Fe(C2O4)3]的同时还有部分Fe(OH)3沉淀
③ 向②所得浊液中加入1mol/LH2C2O4溶液,使溶液变为翠绿色
④ 加热浓缩,冷却结晶,过滤,洗涤,干燥,称量产品的质量为ag
请回答下列问题:
(1)第②步需要控制水浴40℃,温度不能太高的主要目的: ,若第④步冷却时间较长,需将溶液置于冷暗处,原因是: 。
(2)第②步中,为检验Fe2+是否已完全被氧化,可选用 。试剂(填字母)
A.NaOH溶液 B.K3Fe(CN)6溶液 C.苯酚溶液 D.KSCN溶液
(3)请写出第③步中加入H2C2O4溶液将Fe(OH)3沉淀反应生成K3[Fe(C2O4)3]的化学反应方程式: 。
(4)步骤④中的实验操作需要下列仪器中的 (填仪器的编号).
①酒精灯 ②燃烧匙 ③烧杯 ④广口瓶 ⑤研钵 ⑥玻璃棒
(5)有同学为提高产率,避免第④步加热浓缩过程中K3[Fe(C2O4)3]的少量分解,依据查阅的资料提出新的结晶方案:将步骤③得到的溶液中加入 ,过滤,洗涤,干燥,称量。
查看答案和解析>>
科目:高中化学 来源:2016届福建省四地六校高三上学期第一次联考化学试卷(解析版) 题型:实验题
(15分)甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究.
操 作 | 现 象 |
| I.A中溶液变红 Ⅱ.稍后,溶液由红色变为黄色 |
(1)B中反应的离子方程式是 .
(2)A中溶液变红的原因是 .
(3)为了探究现象Ⅱ的原因,甲同学进行如下实验.①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在 .②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液。甲同学的实验证明产生现象Ⅱ的原因是SCN﹣与Cl2发生了反应.
(4)甲同学猜想SCN﹣可能被Cl2氧化了,他又进行了如下研究.资料显示:SCN﹣的电子式为 。
。
①甲同学认为SCN﹣中碳元素没有被氧化,理由是 。
②取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,此证明SCN﹣ 中被氧化的元素是 .
③通过实验证明了SCN﹣中氮元素转化为NO3﹣,他的实验方案是 .
④若SCN﹣与Cl2反应生成1mol CO2,写出反应离子方程式 并计算转移电子的物质的量是 mol。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上学期第一次月考化学试卷(解析版) 题型:选择题
右图是恒温下某化学反应的反应速率随反应时间变化的示意图。下列叙述与示意图不相符合的是

A.反应达平衡时,正反应速率和逆反应速率相等
B.该反应达到平衡态I后,增大反应物浓度,平衡发生移动,达到平衡态II
C.该反应达到平衡态I后,减小反应物浓度,平衡发生移动,达到平衡态II
D.同一种反应物在平衡态I和平衡态II时浓度不相等
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省西安市高一上10月月考化学试卷(解析版) 题型:选择题
下列实验操作中:①过滤;②蒸发;③溶解;④取液体试剂;⑤取固体试剂。一定要用到玻璃棒的是
A.①②③ B.④⑤ C.①④ D.①③⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二上期中考试化学试卷(解析版) 题型:选择题
以NA代表阿伏加德罗常数,则关于反应:C2H2(g)+  O2(g) =2CO2(g)+H2O(1);△H=-1300kJ/mol下列说法中,正确的是
O2(g) =2CO2(g)+H2O(1);△H=-1300kJ/mol下列说法中,正确的是
A.有10NA个电子转移时,该反应吸收1300kJ的能量
B.有NA个水分子生成且为液态时,吸收1300kJ的能量
C.有NA个碳氧共用电子对形成时,放出1300kJ的能量
D.有8NA个碳氧共用电子对形成时,放出1300kJ的能量
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一上期中考试化学试卷(解析版) 题型:选择题
有一瓶质量分数为14%的KOH溶液,加热蒸发掉100g水后,变为28%的KOH溶液80mL,这80mL溶液中溶质的物质的量浓度为
A.5mol/L B.6mol/L C.6.25mol/L D.6.75mol/L
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期10月月考化学试卷(解析版) 题型:实验题
(13分)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
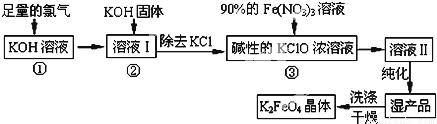
已知:①2KOH+Cl2=KCl+KClO+H2O(条件:温度较低)
②6KOH+3Cl2=5KCl+KClO3+3H2O(条件:温度较高)
回答下列问题:
(1)该生产工艺应在__________(填“温度较高”或“温度较低”)的情况下进行,在溶液I中加入KOH 固体的目的是_________________________。
(2)从溶液II中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为__________。
(3)洗涤除去K2FeO4晶体表面的杂质,应选择的最佳试剂为(填代号)______________。
a.水 b.KOH溶液 c.饱和K2FeO4溶液 d.异丙醇
(4)目前,人们针对K2FeO4的稳定性进行了大量的探索,并取得了一定的进展。下列物质中可能提高化合物K2FeO4水溶液稳定性的是(填代号)__________。
a.亚硫酸钠 b.KOH c.醋酸 d.Fe(NO3)2
(5)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,写出该反应的离子方程式:____________________________。
(6)请你设计一个实验,用化学方法区分KClO溶液与KClO3溶液,写出实验简要步骤,观察到的现象和结论____________________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古奋斗中学高二上9月质检化学试卷(解析版) 题型:选择题
某混合溶液中只含有两种溶质NaCl和H2SO4,且n(NaCl): n(H2SO4)=3:1。若以石墨电极电解该溶液,下列推断中不正确的是
A.整个电解的过程实质是电解水 B.阳极先析出Cl2,后析出O2
C.电解液的pH不断增大,最终大于7 D.阴极产物为H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com