
| A、向氯化铁溶液中加入稀氨水:Fe3++3OH-=Fe(OH)3↓ | ||||
| B、钠和水的反应:Na+H2O═Na++OH-+H2↑ | ||||
C、NH4Cl溶液与氢氧化钠溶液混合共热:NH4++OH-
| ||||
| D、硫酸与氢氧化镁混合:H++OH-=H2O |
| ||


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
| A、只有①和④ | B、只有②和③ |
| C、只有①和③ | D、①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,11.2L甲烷中含有的氢原子数为2NA |
| B、标准状况下,22.4L CCl4中含有的氯原子数为4NA |
| C、常温常压下,7.8g Na2O2与CO2完全反应转移电子数为0.1NA |
| D、通常状况下,2.7g Al与足量的稀盐酸反应,生成H2的分子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫化钠溶液呈碱性:S2-+2H2O?H2S+2OH- |
| B、亚硫酸溶液呈酸性:H2SO3═2H++SO32- |
| C、氯化铝溶液跟过量的氨水反应:Al3++4OH-═[Al(OH)4]- |
| D、FeCl3溶液呈酸性:Fe3++3H2O?Fe(OH)3+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
| B、用锌片作负极,铁片作正极,稀硫酸为电解质溶液一段时间后,溶液PH增大 |
| C、把铜片插入三氯化铁溶液中,在铜片表面出现一层铁 |
| D、铜的金属活泼性比铁的差,可在海轮外壳上装若干铜块以减缓海轮腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 它可通过不同化学反应分别制得B、C、D和E四种物质.
它可通过不同化学反应分别制得B、C、D和E四种物质.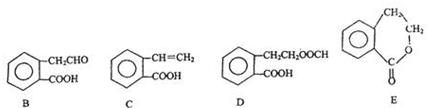
 、HCOOH、CH3COOC2H5
、HCOOH、CH3COOC2H5查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| 时间/mim | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com