
【题目】由CH3CH3→CH3CH2Cl→CH2=CH2→CH3CH2OH的转化过程中,经过的反应类型是( )
A.取代→加成→氧化
B.加成→取代→消去
C.取代→消去→加成
D.取代→消去→水解
科目:高中化学 来源: 题型:
【题目】现有pH为1的100mL 0.1moL/L 的AlCl3溶液,下列有关判断正确的是:
A.溶液显酸性,主要因为铝离子水解导致的
B.溶液显酸性,主要因为溶液中有盐酸
C.溶液显碱性,主要因为铝离子水解导致的
D.溶液显碱性,主要因为铝离子水解导致的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C10H10O2Br2的芳香族化合物X,符合下列条件:
①其核磁共振氢谱图中有四个吸收峰,吸收峰的面积比为1:2:6:1,
②其苯环上有四个取代基(其中两个为甲基);且苯环上的一卤代物只有一种;
③水解酸化后的产物 C能发生银镜反应,D遇FeCl3溶液显色且E能与浓溴水反应在一定条件下可发生下述一系列反应
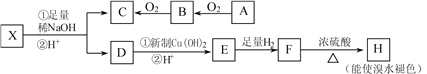
已知:①在稀碱溶液中,溴苯难发生水解
②
请回答下列问题
(1)X中含氧官能团的名称是______;
(2)E可能具有的化学性质______(选填序号)。
a.取代反应 b.消去反应 c.氧化反应 d.还原反应
(3)在上述反应中有机物发生还原反应的是______;
a.A →B b.D →E c.E →F d.F →H
(4)写出下列反应的化学方程式:
①A→B:_____________________________________________;
②F→H: ______________________________________________;
(5)同时符合下列条件的E的同分异构体共有______种,其中一种的结构简式为______。
a.能发生水解反应
b.遇FeCl3溶液显色
c.含有苯环,苯环上有两个取代基且苯环上有两种不同化学环境的氢原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题。
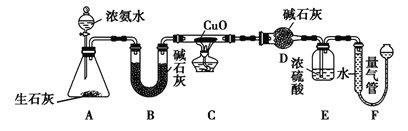
(1)写出A装置中发生反应的化学方程式__________。
(2)实验中观察到C装置中黑色CuO粉末变为红色固体,量气管中有无色无味的气体产生,上述现象证明NH3具有____性,写出相应的化学方程式______。
(3)读取气体体积前,对F装置进行的操作是慢慢上下移动右边的漏斗,使左右两管液面相平,其目的是________________。
(4)E装置的作用是___________;量气管中有空气,对实验______(填“有”或“无”)影响。
(5)实验完毕,若测得干燥管D增重mg,F装置测得气体的体积为VL(已折算成标准状况),则氨分子中氮、氢的原子个数比为______(用含m、V的代数式表示)。若拆掉B装置,测得的结果____(填“偏大”“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C,D 4种元素,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C.
(1)B元素的名称为;
(2)A,B形成的化合物的电子式为 .
(3)C的元素符号为 , C的最高价氧化物的化学式为 .
(4)D的最高价氧化物对应的水化物的化学式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A,B,C,D,E五种短周期元素,已知相邻的A,B,C,D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的单质可与酸反应,1mol E单质与足量酸作用,在标准状况下能产生33.6L H2;E的阳离子与A的阴离子核外电子层结构完全相同.
回答下列问题: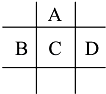
(1)A与E形成的化合物的化学式是 .
(2)B的最高价氧化物化学式为 , C的元素名称为 , D的单质与水反应的方程式为
.
(3)向D与E形成的化合物的水溶液中滴入烧碱溶液直至过量,观察到的现象是 , 有关反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.NO2与水的反应:3NO2+H2O═2NO3﹣+NO+2H+
B.氯气通入水中:Cl2+H2O═2H++Cl﹣+ClO﹣
C.向NH4HCO3溶液中加过量NaOH溶液并加热:NH4++OH﹣ ![]() NH3↑+H2O
NH3↑+H2O
D.向硅酸钠溶液中通入SO2:SiO32﹣+2H+═H2SiO3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2-硝基-1,3-苯二酚是橘黄色固体,易溶于水、溶液呈酸性,沸点为88℃,是重要的医药中间体。实验室常以间苯二酚为原料分以下三步合成:

具体实验步骤如下:
①磺化:称取5.5g碾成粉状的间苯二酚放入烧杯中,慢慢加入浓硫酸并不断搅拌,控制温度为60~65℃约15min。
②硝化:将烧杯置于冷水中冷却后加入混酸,控制温度(25±5) ℃左右继续搅拌15min。
③蒸馏:将反应混合物移入圆底烧瓶B中,小心加入适量的水稀释,再加入约0.1g尿素,然后用下图所示装置进行水蒸气蒸馏;将馏出液冷却后再加入乙醇-水混合剂重结晶。

回答下列问题:
(1)实验中设计Ⅰ、Ⅲ两步的目的是__________。
(2)烧瓶A中玻璃管起稳压作用,既能防止装置中压强过大引起事故,又能_______
(3)步骤②的温度应严格控制不超过30℃,原因是_____________。
(4)步骤③所得2-硝基-1,3-苯二酚中仍含少量杂质,可用少量乙醇-水混合剂洗涤。请设计简单的实验证明2-硝基-1,3-苯二酚已经洗涤干净:______________。
(5)本实验最终获得1.0g橘黄色固体,则2-硝基-1,3-苯二酚的产率约为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、下图表示一些晶体中的某些结构,它们分别是氯化钠、氯化铯、干冰、金刚石、石墨结构中的某一种的某一部分(黑点可表示不同或相同的粒子)。
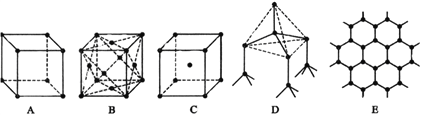
(1)其中代表金刚石的是_______(填编号字母,下同),金刚石中每个碳原子与_____个碳原子最接近且距离相等。
(2)其中代表石墨的是______,其中每个正六边形占有的碳原子数平均为____________个;
(3)其中表示氯化钠的是______,每个钠离子周围与它最接近且距离相等的钠离子有______个;
(4)代表氯化铯的是________,每个铯离子与________个氯离子紧邻;
II、(1)已知14gCO气体在氧气中完全燃烧可放出141.5 kJ的热量,写出CO燃烧的热化学方程式______________________________________________;
(2)土壤中的微生物可将大气中H2S经两步反应氧化成SO42﹣,两步反应的能量变化示意图如下:则1mol H2S(g)全部氧化成SO42﹣(aq)的热化学方程式为____________________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com