
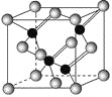
【题目】已知镓是铝同族下一周期的元素。砷化镓的晶胞结构如图所示。试回答:
(1)镓的基态原子的电子排布式是______。
(2)砷化镓晶胞中所包含的砷原子(白色球)个数为___,与同一个镓原子相连的砷原子构成的空间构型为____。
(3)N、P、As处于同一主族,其氢化物沸点由高到低的顺序是___ (用氢化物分子式表示)。
(4)砷化镓可由(CH3)3Ga和AsH3在700 ℃时制得。(CH3)3Ga中镓原子的杂化方式为____。
(5)比较二者的第一电离能:As____Ga(填“<”、“>”或“=”)。
(6)下列说法正确的是__(填字母)。
A.砷化镓晶胞结构与NaCl相同 B.电负性:As>Ga C.砷化镓晶体中含有配位键
【答案】1s22s22p63s23p63d104s24p1(或[Ar]3d104s24p1) 4 正四面体 NH3>AsH3>PH3 sp2 > BC
【解析】
(1)镓是31号元素,其原子核外有31个电子,根据构造原理书写其基态原子核外电子排布式;
(2)根据砷原子的位置,利用均摊法分析晶胞的结构;
(3)从氢键以及影响分子间作用力的因素比较氢化物熔沸点的高低;
(4)根据价层电子对数计算杂化类型;
(5)同周期元素从左到右,元素的第一电离能逐渐增大,
(6)从晶体类型以及原子结构的角度分析.
(1)镓位于周期表中第四周期第IIIA,故其核外电子排布式为1s22s22p63s23p63d104s24p1(或[Ar]3d104s24p1),
故答案为:1s22s22p63s23p63d104s24p1(或[Ar]3d104s24p1);
(2)根据“均摊法”:白色球个数为6×12+8×18)=4.由晶胞图可知与同一个镓原子相连的砷原子构成的空间构型为正四面体,故答案为:4;正四面体;
(3)由于NH3分子间存在氢键,所以NH3的沸点最高,由于AsH3的相对分子质量大于PH3,故AsH3的沸点高于PH3,
故答案为:NH3>AsH3>PH3;
(4)由于Ga原子周围只有3对成键电子对,故其杂化方法为sp2,故答案为: sp2;
(5)As和Ga处于同一周期,而处于VA的As外围电子处于半满的较稳定结构,故As的第一电离能大于Ga,
故答案为:>;
(6)A.NaCl晶体中阴阳离子的配位数为6,而砷化镓晶胞中中阴阳离子的配位数为8,二者晶体结构不同,故A错误;
B. 周期表同周期元素从左到右元素的电负性逐渐增大,则As>Ga,故B正确;
C .由于Ga原子最外层只有3个电子,而每个Ga原子与4个As原子成键,因此其中一个共价键必为配位键,故C正确。
故答案为:BC


科目:高中化学 来源: 题型:
【题目】已知:2KMnO4![]() K2MnO4+MnO2+O2↑,将0.1moKMnO4固体加热一段时间后,收集到amolO2;向反应后残留的固体中加入足量的浓盐酸,又收集到bmolCl2,此时Mn元素全部以Mn2+的形式存在于溶液中(注:KMnO4和K2MnO4以及MnO2都能与浓盐酸反应并生成Mn2+)。
K2MnO4+MnO2+O2↑,将0.1moKMnO4固体加热一段时间后,收集到amolO2;向反应后残留的固体中加入足量的浓盐酸,又收集到bmolCl2,此时Mn元素全部以Mn2+的形式存在于溶液中(注:KMnO4和K2MnO4以及MnO2都能与浓盐酸反应并生成Mn2+)。
(1)2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O反应中的还原产物是_____(填化学式),反应中若产生0.3mol的气体则有________mol的电子转移。
(2)a+b的最大值为________,a+b最小值为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将 2mol NO2 装入 5 L 带活塞的密闭容器中,当反应 2NO2(g) N2O4(g)ΔH=-60 kJ/mol 达到平衡时,恢复到原来的温度,测得此过程中体系向外界共释放了 40 kJ 的热量。 下列说法正确的是( )
A.温度升高,平衡常数 K 增大
B.慢慢压缩气体体积,平衡向右移动,混合气体颜色变浅
C.上述反应达到平衡时,NO2的转化率是 40%
D.若起始时向容器中充入 1.0 mol N2O4,保持温度不变,达到平衡时共吸收 20 kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2SO2(g)+O2(g)![]() 2SO3(g)ΔH<0。某温度下,将 2 mol SO2 和 1 mol O2 置于 10L 密闭容器中,反应达平衡后,SO2 的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )
2SO3(g)ΔH<0。某温度下,将 2 mol SO2 和 1 mol O2 置于 10L 密闭容器中,反应达平衡后,SO2 的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )
甲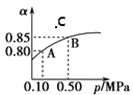 乙
乙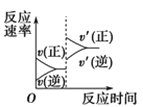 丙
丙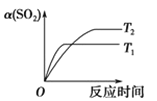
A.由图甲推断,B 点 SO3的平衡浓度为 0.3molL1
B.在图甲中,在此温度下,C 点 υ 正<υ 逆
C.达到平衡后,保持体积不变,充入氦气,压强增大,则反应速率变化图像可以用图乙表示
D.压强为 0.50 MPa 时,不同温度下 SO2 的平衡转化率与时间关系如图丙,则 T2>T1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10mol/L NaOH溶液滴定0.10mol/L HA溶液,滴定曲线如图a所示,混合溶液的pH与离子浓度变化的关系如图b所示,下列叙述错误的是
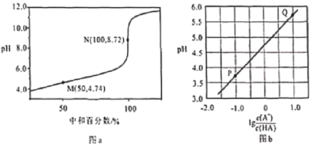
A. 当滴定至溶液呈中性时,c(A-)>c(HA)B. N点,c(Na+)·c(A-)=![]()
C. Ka(HA)的数量级为10-5D. P-Q过程中,水的电离程度逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。
I.K2Cr2O7曾用于检测司机是否酒后驾驶:Cr2O72-(橙色)+CH3CH2OH→Cr3+(绿色)+CH3COOH(未配平)
(1)基态Cr原子的价电子轨道表达式为__。
(2)CH3COOH分子中所含元素的电负性由大到小的顺序为__,碳原子的轨道杂化类型为__,所含σ键与π键的数目之比为__。
(3)已知Cr3+等过渡元素水合离子的颜色如表所示:
离子 | Sc3+ | Cr3+ | Fe2+ | Zn2+ |
水合离子的颜色 | 无色 | 绿色 | 浅绿色 | 无色 |
请根据原子结构推测Sc3+、Zn2+的水合离子为无色的原因为__。
II.ZnCl2浓溶液常用于除去金属表面的氧化物,例如与FeO反应可得Fe[Zn(OH)Cl2]2溶液。
(4)Fe[Zn(OH)Cl2]2溶液中不存在的微粒间作用力有__(填选项字母);
A.离子键 B.共价键 C.金属键 D.配位键 E.范德华力 F.氢键
溶液中[Zn(OH)Cl2]-的结构式为__。
III.锌是人体必需的微量元素之一,其堆积方式如图1,晶胞结构如图2。

(5)锌的堆积方式为__,配位数为__。
(6)若锌原子的半径为apm,阿伏加德罗常数的值为NA,则锌晶体的密度为___g/cm3(用含a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列“解释或结论”与“实验操作及现象”不相符的一组是
序号 | 实验操作及现象 | 解释或结论 |
A | 浓硫酸滴到纸张上,纸变黑 | 浓硫酸有脱水性 |
B | 向紫色石蕊溶液中加入氯水,溶液先变红,随后褪色 | 氯水中含有酸性物质和 漂白性物质 |
C | 向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的气体 | 该溶液中一定有CO32- |
D | 向某溶液中加入浓NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体 | 该溶液中一定含有NH |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】安全是顺利进行实验及避免伤害的保障.下列实验操作正确且不是从实验安全角度考虑的是( )
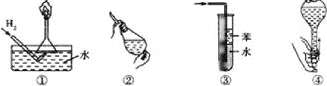
A. 操作①:使用稍浸入液面下的倒扣漏斗检验氢气的纯度
B. 操作②:使用CCl4萃取溴水中的溴时,振荡后需打开活塞使漏斗内气体放出
C. 操作③:吸收氨气或氯化氢气体并防止倒吸
D. 操作④:用食指顶住瓶塞,另一只手托住瓶底,把瓶倒立,检查容量瓶是否漏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019 年 11 月《Science》杂志报道了王浩天教授团队发明的制取H2O2 的绿色方法,原理如图所示(已知:H2O2 ![]() H+ + H2O , Ka = 2. 4×10一12 )下列说法不正确的是
H+ + H2O , Ka = 2. 4×10一12 )下列说法不正确的是
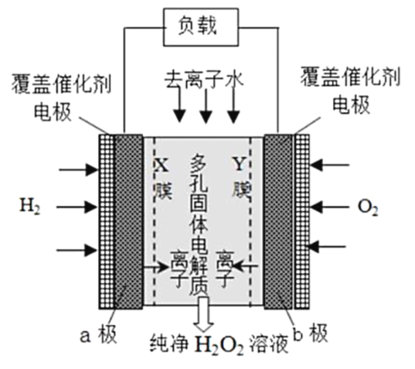
A.b 极上的电极反应为O2 +H2O +2e- =HO2 - +OH
B.X 膜为选择性阳离子交换膜
C.催化剂可促进反应中电子的转移,加快反应速率
D.每生成1 mol H2O2 电极上流过4 mole-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com